US Pharm. 2006;7:58-68.
Hjertesvikt er et stort helseproblem i Usa. Omtrent fem millioner mennesker har hjertesvikt, og 550 000 pasienter diagnostiseres med hjertesvikt hvert år.1,2 Hjertesvikt er generelt karakterisert som en sykdom hos eldre; ca 80% av pasientene innlagt med hjertesvikt er eldre enn 65 år. Dermed forventes forekomsten av hjertesvikt å vokse etter hvert som befolkningen blir eldre.2 Hjertesviktrelaterte sykehusinnleggelser økte med ca 25%, til mer enn en million, mellom 1990 og 1999. I 2001 forårsaket hjertesvikt direkte 53 000 dødsfall. Hjertesviktrelaterte dødsfall har steget de siste årene, noe som kan tilskrives en økning i overlevelse fra tidligere kardiovaskulære hendelser.
Hjertesvikt Er et klinisk syndrom hvor funksjonelle eller strukturelle endringer forekommer i hjertet, noe som resulterer i kliniske symptomer som dyspnø, tretthet, begrenset treningstoleranse, lungestopp og perifert ødem.1-3 mange kjente risikofaktorer, som koronararteriesykdom( CAD), diabetes, fedme, hypertensjon og familiehistorie av kardiomyopatier, er forbundet med utbruddet og progresjonen til hjertesvikt (Tabell 1).4 i tillegg er valvulær hjertesykdom fortsatt en vanlig årsak til hjertesvikt. Hypertensjon går foran hjertesvikt omtrent 90% av tiden og øker pasientens risiko for hjertesvikt tredoblet.5 CAD er den vanligste årsaken til systolisk hjertesvikt. Myokardinfarkt (MI) står for systolisk hjertesvikt hos nesten 70% av pasientene. Ytterligere etiologier forbundet med systolisk dysfunksjon og hjertesvikt inkluderer dilaterte kardiomyopatier og ventrikulær hypertrofi.2,4

Patofysiologi
Systolisk hjertesvikt er assosiert med nedsatt venstre ventrikulær kontraktilitet som resulterer i ineffektiv hjerteutgang, spesielt under anstrengelse. Hjertesvikt begynner vanligvis med noen skade eller stress på hjertemuskelen som resulterer i en endring i strukturen i hjertet; dette er kjent som hjerte remodeling. Cardiac remodeling forut for utbruddet av symptomer etter måneder eller år. Etter hvert som dilatasjonen endrer ventrikkelen til en mer sfærisk form, begynner hemodynamiske spenninger å legge til belastning på veggene i den sviktende ventrikkelen, noe som fører til deprimert mekanisk funksjon og økt regurgitantstrøm gjennom mitralventilen.1-3
det neurohormonale systemet har en aktiv rolle i akselerasjonen av kardial remodeling. Hjertesviktpasienter har økte nivåer av norepinefrin, angiotensin II, aldosteron, endotelin, vasopressin og cytokiner. Aktivering av renin-angiotensin-aldosteronsystemet øker perifer vasokonstriksjon, noe som resulterer i økt afterload og kardial remodeling. I tillegg forårsaker aktiveringen av sympatisk nervesystem takykardi, noe som fører til økt myokardisk oksygenbehov. Økt hjerteoksygenbehov uten endringer i tilbudet kan føre til økt myokardisk iskemi og ytterligere kardial remodeling. Neurohormonene kan utøve kardiotoksiske effekter på cellene, noe som ytterligere kan forandre arkitekturen og ytelsen til hjertet.2
Klinisk Presentasjon
Systolisk hjertesvikt er et syndrom diagnostisert basert på data samlet inn fra en grundig pasienthistorie, inkludert en evaluering av symptomatologi og fysiske funn. De fleste pasienter er tilstede på en av tre måter: med redusert treningstoleranse, med væskeretensjon eller uten symptomer.2,6 Dyspnø på anstrengelse og kortpustethet er kardinale symptomer på hjertesvikt. Ved fysisk undersøkelse kan perifert ødem, lungestopp eller begge symptomer være tilstede.2
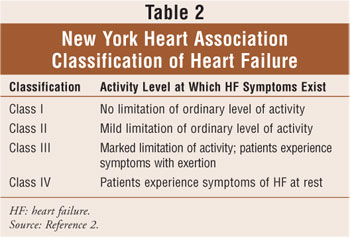
Klassifisering av hjertesvikt er basert på kombinasjonen Av American College Of Cardiology / American Heart Associations fire stadier av hjertesvikt (Tabell 1), som spenner fra risiko for hjertesvikt (stadium A) til ildfast hjertesvikt (stadium D), og på new York Heart Association (NYHA) retningslinjer.2,6 NYHA-klassifiseringen er den mest brukte metoden for å kvantifisere graden av funksjonsbegrensning ved hjertesvikt (Tabell 2). Samlet sett har den funksjonelle klassifiseringen av hjertesvikt en tendens til å avta over tid på grunn av utviklingen av kardial remodeling.2
den mest nyttige diagnostiske testen er det omfattende todimensjonale ekkokardiogrammet, som brukes sammen Med Doppler-strømningsstudier for å avgjøre om det er strukturelle og funksjonelle abnormiteter i hjertet. Transtorakal ekkokardiogram (tte) er en ikke-invasiv ultralydstudie som produserer bilder av hjertet ved hjelp av lydbølger. Den gir informasjon om estimering av VENSTRE ventrikulær ejeksjonsfraksjon (LVEF), ventrikulære dimensjoner og volumer, veggvolumer, hjertekammergeometri og regional veggbevegelse. HOS pasienter med systolisk hjertesvikt ER LVEF vanligvis mindre enn 40%.2 andre studier brukt i forbindelse MED TTE for å vurdere etiologi, alvorlighetsgrad og potensielle legemiddelrelaterte behandlingseffekter ved hjertesvikt inkluderer baseline brystrøntgen, 12-bly elektrokardiografi og målinger av natriuretisk peptid i hjernen, serumelektrolytter og nyrefunksjon. Disse studiene er viktige fordi helsepersonell kan bruke dem som en grunnlinje for å avgjøre om en pasient har opplevd en endring i klinisk status.2,6
BEHANDLING AV SYSTOLISK HJERTESVIKT
Ikke-Farmakologisk
Kontroll av risikofaktorer som hypertensjon, diabetes mellitus, dyslipidemi, aterosklerotiske vaskulære sykdommer og tyreoideaforstyrrelser kan bremse utviklingen av hjertesvikt og kardial remodeling.2,4,6 Hjertesviktpasienter bør få influensa-og pneumokokkvaksiner for å redusere risikoen for komorbiditeter som luftveisinfeksjoner.2 Den viktigste modifiserbare risikofaktoren vil være høyrisikoatferd som røyking, alkohol og ulovlig narkotikabruk.2,7
Natriumrestriksjon (?2 gram / dag) hjelpemidler i reduksjon av volum overbelastning og kan redusere bruken av diuretika. Videre gjør daglig veiing det mulig for pasienter å vurdere volumstatus, som diuretisk dosejustering kan baseres på. Ingen studier har imidlertid undersøkt effekten av natriumbegrensning i kosten på morbiditet eller mortalitet.7,8 Fysisk aktivitet har vist seg å redusere dødelighet og sykehusinnleggelser for stabile hjertesviktpasienter. Begrensning av trening fremmer fysisk dekondisjonering, noe som kan bidra til pasientens treningsintoleranse. Til slutt har overholdelse av diett og terapeutisk medisinbehandling en betydelig rolle i forebygging av akutte sykehusinnleggelser.2,7
Farmakologisk
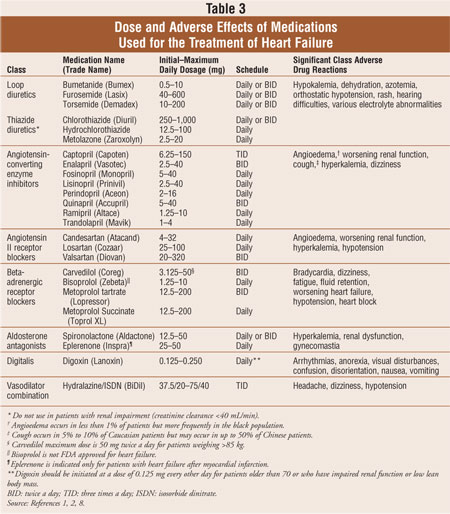
De fleste pasienter med hjertesvikt behandles med et standard kombinasjonsregime med tre legemidler: et loop-diuretikum, en angiotensinkonverterende enzym (ACE) – hemmer eller en angiotensin II-reseptorblokker (ARB) og en beta-adrenerge reseptorblokker.1,2 Diuretika er bærebjelken for reduksjon av symptomer på volumoverbelastning ved hjertesvikt, MENS ACE-hemmere, Arb og betablokkere har vist seg å redusere morbiditet og mortalitet.2 Aldosteronantagonister er indisert som tilleggsbehandling for pasienter MED symptomatisk NYHA klasse III eller IV hjertesvikt eller etter tidlig akutt HJERTEINFARKT hos pasienter med redusert venstre ventrikkelfunksjon og kliniske tegn på hjertesvikt. Hvis pasientene fortsetter å være symptomatisk, kan digoksin legges til standardmedisinregimet for å redusere symptomer, redusere sykehusinnleggelser og øke treningstoleransen. Legemidler som brukes til å behandle hjertesvikt er omtalt i Tabell 3. Livsstilsendringer og medikamentterapier for systolisk hjertesvikt er utformet for å redusere sykelighet og dødelighet, forhindre progresjon av kardial remodeling og forbedrepasienters livskvalitet.2
Diuretika:Støtten til symptomatisk behandling av volumoverbelastning ved hjertesvikt, diuretika reduserer væskeretensjon som forårsaker lungetetthet, perifert ødem, jugular venøs distensjon og/eller økt kroppsvekt. Loop diuretika som virker I loop Av Henle øker serumnatriumutskillelsen med 20% til 25%, øker eliminasjonen av fritt vann og opprettholder effekten hos pasienter med nedsatt nyrefunksjon.1,2 i kontrast reduserer tiaziddiuretika natriumutskillelsen med 5% til 10%, øker utskillelsen av fritt vann og mister effekten hos pasienter med kronisk nyresykdom (kreatininclearance <40 mL / min). Loop diuretika er de foretrukne midler for hjertesvikt behandling, men tiazider kan brukes hos pasienter med mild væskeretensjon og hypertensjon. Diuretika, SAMT ACE-hemmere og betablokkere, anbefales til bruk hos alle pasienter I Hjertesvikt I Fase c.2 Studier har vist at diuretika forbedrer hjertefunksjon, symptomer og treningsintoleranse hos pasienter med hjertesvikt. De langsiktige effektene av diuretika på dødelighet er imidlertid ukjente.1,2,8
ACE-Hemmere: ACE-hemmere reduserer aktiviteten til renin-angiotensin-aldosteronsystemet ved å blokkere omdannelsen av angiotensin I til angiotensin II, og forhindrer angiotensin II-indusert vasokonstriksjon. De hemmer også aldosteronfrigivelse, noe som fører til en reduksjon i natrium og væskeretensjon. Disse kombinerte effektene reduserer både forspenning og etterbelastning og reduserer progresjonen av kardial remodeling.1,2 ACE-hemmere kan også ha ytterligere aktivitet med økt kinin-og kininmediert prostaglandinproduksjon.2 Over 30 kliniske kontrollerte studier som evaluerte EFFEKTEN AV ACE-hemmere har vist AT ACE-hemmere reduserer risikoen for død og kombinert risiko for død og sykehusinnleggelser. ALLE pasienter med systolisk hjertesvikt i venstre ventrikkel bør gis EN ACE-hemmer med mindre DET er kontraindisert (angioødem, bilateral nyrearteriestenose, serumkalium > 5,5 mEq / L, graviditet, symptomatisk hypotensjon eller ustabil nyresvikt). ACE-hemmere bør initieres ved lave doser og titreres langsomt basert på tolerabilitet av bivirkninger.1,2,8
Arb: sammenlignet med STUDIER AV ACE-hemmere har færre kliniske studier studert Bruken Av Arb hos pasienter med hjertesvikt; dermed er disse midlene reservert for pasienter med påvist intoleranse AV ACE-hemmere. Arb blokkerer selektivt angiotensin II ved binding til angiotensinreseptoren. Arb reduserer alvorligheten av kininbivirkningene, som hoste og angioødem, selv om angioødem er rapportert med disse legemidlene. Tillegg AV EN ARB til standardbehandling, inkludert EN ACE-hemmer, kan redusere størrelsen på venstre ventrikel og antall sykehusinnleggelser, men bevis er utilstrekkelig for reduksjon av dødelighet.2,8 en studie viste at candesartan tilsatt TIL EN ACE-hemmer reduserte kardiovaskulære dødsfall.9 en annen studie med valsartan hos pasienter Med MIand hjertesvikt viste imidlertid ingen nytte av valsartan og EN ACE-hemmer gitt sammen sammenlignet med EN ACE-hemmer alene.10 Forskrivning av EN kombinasjon AV ACE-hemmere, Arb og aldosteronantagonister anbefales ikke på grunn av risikoen for hyperkalemi. Arb forblir et alternativ TIL ACE-hemmere ved behandling av hjertesvikt.2
Beta-Adrenerge Reseptorblokkere: Tre typer betablokkere har vist seg å redusere dødelighet: metoprolol og bisoprolol med vedvarende frisetting, som selektivt blokkerer beta-1-reseptorer, og karvedilol, som blokkerer alfa-1 -, beta-1-og beta-2-reseptorer.1,2,8 til sammenligning viste en studie at korttidsvirkende metoprolol hadde mindre effekt sammenlignet med karvedilol, men dosen av metoprolol som ble brukt var lavere enn anbefalt måldose.11 i tillegg til standardbehandling har betablokkere vist en kombinert reduksjon i død og sykehusinnleggelse for hjertesvikt. Betablokkere hemmer bivirkninger fra sympatisk nervesystem, oppveier de negative inotrope effektene.2 totalt sett bør betablokkere innledes med svært lave doser, titreres langsomt med minimum to ukers mellomrom og ikke brått seponeres på grunn av risiko for forverring av hjertesvikt og akutt dekompensasjon.1,2
Aldosteronantagonister: Aldosteronantagonister blokkerer aldosteronreseptoren i det distale tubuli i nevronet, noe som resulterer i kaliumretensjon, natriumutskillelse og mild diurese. Aldosteronantagonister anbefales hos pasienter med moderat alvorlig eller alvorlig hjertesvikt og nylig dekompensert eller hos pasienter med venstre ventrikkel dysfunksjon kort tid etter HJERTEINFARKT.2 når lavdose spironolakton ble gitt i TILLEGG TIL EN ACE-hemmer hos pasienter MED NYHA klasse III og IV hjertesvikt, opplevde pasientene 30% reduksjon i mortalitet uansett årsak.12 En annen studie viste at eplerenon førte til en reduksjon i dødelighet hos PASIENTER med LVEF mindre enn 40% innen 14 DAGER ETTER MI, selv om det ikke foreligger data om bruk av eplerenon ved behandling av hjertesvikt relatert til andre årsaker enn MI.13 den mest fremtredende begrensende faktoren for aldosteronantagonister er potensielt livstruende hyperkalemi.2,14 Hyperkalemi øker progressivt når serumkreatinin overstiger 1,6 mg / dL, selv om studier har undersøkt aldosteronantagonister hos pasienter med entry-level serumkreatinin på 2,0 til 2,5 mg / dL. I tillegg bør aldosteronantagonister unngås hos pasienter med serumkalium større enn 5,0 mEq per liter.2
Digoksin: Digoksin er et hjerteglykosid som arbeider for å øke kontraktiliteten i hjertet ved å hemme natrium-kalium adenosin trifosfatase (ATPase) pumpe, og dermed øke intracellulært kalsium. Digoksin anbefales for symptomatisk kontroll hos pasienter MED mild TIL moderat hjertesvikt NYHA KLASSE II eller III. 2 i en post hoc-analyse reduserte serumkonsentrasjoner av digoksin mellom 0,5 og 0,9 ng/mL sykehusinnleggelser.15 mens studier ikke har vist at digoksin reduserer dødeligheten, kan dette stoffet forbedre symptomer og utøve intoleranse, redusere sykehusinnleggelser og forbedre den generelle livskvaliteten.2,8,16
Vasodilatorkombinasjon: Anbefaling av hydralazin og isosorbiddinitrat (ISDN) i kombinasjon er reservert for pasienter som har vist manglende evne til å tolerere EN ACE-hemmer eller ARB. I en nylig studie med En kohort Av Afroamerikanske pasienter med symptomatisk NYHA III ELLER IV hjertesvikt, førte imidlertid tillegg av hydralazin og ISDN-kombinasjon til standardbehandling (DVS. ACE-hemmer, vanndrivende og betablokker) til en 43% forbedring i overlevelse og en 33% reduksjon i risikoen for første sykehusinnleggelse versus placebo.17 i teorien kan hydralazin-og ISDN-kombinasjonen øke biotilgjengeligheten av nitrogenoksid.2 kombinasjonen ISDN og hydralazin (BiDil) ER FDA godkjent bare For Afroamerikanere som tilleggsbehandling til standard hjertesvikt terapi.18 Hydralazin Er en arteriol vasodilator, som virker for å redusere afterload, MENS ISDN er en venøs vasodilator, som virker for å redusere forspenning. Denne kombinasjonen av vasodilatorer er ikke foretrukket over ACE-hemmere eller Arb, siden det kan ha utålelige bivirkninger som hodepine eller svimmelhet og compliance problemer som tapte doser, men det kan brukes som en tilleggsbehandling for Den Afroamerikanske befolkningen.2
Alternative Medisiner: Hagtorn blader med blomster, også kjent Som Crataegus ekstrakt, har vært talsmann for mild hjertesvikt (NYHA II). Gjennom in vitro-studier har hagtornblader vist positive inotrope effekter, vasodilaterende egenskaper og økt koronar blodstrøm. Studier har vist forbedring på subjektive symptomer hos pasienter med mild hjertesvikt. På grunn av digitalislignende effekter, bør pasienter som tar Både Crataegus ekstrakt og digitalis overvåkes nøye. Bivirkninger som ble rapportert var gastrointestinale symptomer, hjertebank, brystsmerter og svimmelhet.19,20
En annen alternativ medisin som har blitt brukt til behandling av hjertesvikt er coenyzme Q10, et fettløselige vitamin. Noen studier viste at koenzym Q10 førte til forbedring i hyppigheten av sykehusinnleggelser, dyspnø og ødem.21 en randomisert, dobbeltblind, placebokontrollert studie viste imidlertid ingen forskjell mellom coenyzme Q10 og placebo i LVEF, treningstoleranse eller maksimalt oksygenforbruk hos hjertesviktpasienter.22 Dokumenterte bivirkninger av koenzym Q10 var gastrointestinalt ubehag, hypoglykemi og hypotensjon.21 Kliniske kontrollerte studier Av Crataegus ekstrakt og coenyzme Q10 er i gang for å evaluere effekt og sikkerhet ved behandling av hjertesvikt.20,21
SKADELIGE MEDISINER I HJERTESVIKT
Flere klasser av medisiner kan forverre hjertesvikt og bør unngås. Antiarytmiske midler, unntatt amiodaron eller dofetilid, kan forårsake kardiodepressant og proarytmisk effekt på hjertet, noe som fører til akutt dekompensering.1,2 første generasjons kalsiumkanalblokkere har vært assosiert med økte kardiovaskulære hendelser og forverring av hjertesvikt. De nyere, langtidsvirkende kalsiumkanalblokkerne amlodipin og felodipin ser ut til å være trygge, men ingen studier har vist en statistisk signifikant reduksjon i dødelighet.2,8,23 tiazolidindionene har vært forbundet med vektøkning og væskeretensjon, noe som muligens fører til hjertesvikt eller fremskynder akutt hjertesvikt. Imidlertid er ødem mer sannsynlig når tiazolidindioner brukes i kombinasjon med insulinbehandling.24,25 tiazolidindioner anbefales derfor Ikke til pasienter med diabetes mellitus OG NYHA KLASSE III ELLER IV hjertesvikt.25-27 NSAIDs forårsaker natriumretensjon og perifer vasokonstriksjon, som utløser en akutt hjertesvikt forverring. I tillegg reduserer de effekten og øker risikoen for toksisitet fra ACE-hemmere og diuretika. Det er en mulighet for narkotikainteraksjon når aspirin brukes i kombinasjon med ACE-hemmere, men det forblir kontroversielt og krever videre studier.2
APOTEKETS ROLLE
en forståelse av fordelene med medisinering i hjertesvikt kan føre til optimal farmasøytisk behandling. Farmasøyter kan hjelpe pasienter med å identifisere og lindre høyrisiko atferd som røyking, alkoholforbruk, og ulovlig OG skadelig OTC narkotikabruk. I tillegg må farmasøyter overvåke pasienter for sykdomstilstandsprogresjon, inkludert tegn og symptomer på hjertesvikt, og oppmuntre pasienter til å kartlegge vekten.
Oppmuntre pasienter til å overholde kosttilskudd restriksjoner, trening retningslinjer, og medisiner regimer for hjertesvikt bør være en farmasøyt prioritet. Manglende overholdelse av terapeutiske medisiner har vært forbundet med økt dødelighet og kan være relatert til uønskede bivirkninger av medisiner. Farmasøyter bør overvåke og oppmuntre pasienter til å være i samsvar med sine medisiner for å redusere dødeligheten. Ved å overvåke og utdanne pasienter og annet helsepersonell om narkotikarelaterte bivirkninger, kan farmasøyter bidra til å øke medisinering etterlevelse. Videre må farmasøyter være oppmerksomme på alternativer til medisiner som ACE-hemmere og diskutere med andre helsepersonell fordelene i dødelighet forbundet med dem for å gi optimal farmasøytisk omsorg og redusere risikoen for dødelighet.
Pasienter og helsepersonell kan ikke være klar over sammenhengen mellom vanlige medisiner og forverring av hjertesvikt. Siden noen vanlige OTC medisiner, inkludert NSAIDs, er kontraindisert hos pasienter med hjertesvikt, utdanne pasienten om hvorfor han eller hun ikke bør ta disse medikamentene er en annen viktig rolle for farmasøyter. Farmasøyter må overvåke pasienter for og rådføre seg med helsepersonell og pasienter om skadelige legemiddel-og legemiddel-sykdom interaksjoner som kan resultere i sykehusinnleggelse.
1. Klein L, O ‘ Connor CM, Gattis WA, et al. Farmakologisk behandling for pasienter med kronisk hjertesvikt og redusert systolisk funksjon: gjennomgang av forsøk og praktiske hensyn. Am J Cardiol. 2003; 91 (suppl): 18F-40F.
2. Hunt SA, Abraham WT, Chin MH, et al. ACC / AHA 2005 retningslinje oppdatering for diagnose og behandling av kronisk hjertesvikt hos voksne: en rapport Fra American College Of Cardiology / American Heart Association Task Force On Practice Guidelines (Skrive Komiteen For Å Oppdatere 2001 Retningslinjer For Evaluering og Behandling Av Hjertesvikt). American College Of Cardiology (Engelsk). Tilgjengelig på: www.acc.org/clinical/guidelines/failure//index.pdf.
3. Francis GS, Gassler JP, Sonnenblick EH. Patofysiologi og diagnose av hjertesvikt. In: Jørgensen, et al., eds. Hurst Er Hjertet. 10.utg. New York, NY: McGraw-Hill; 2001: 655-686.
4. De Cas L, Metra M, Nodari S, et al. Forebygging og behandling av kronisk hjertesvikt hos pasienter i fare. Am J Cardiol. 2003; 91 (suppl): 10F-17f.
5. Chobanian AV, Bakris GL, Black HR, et al. Syvende rapport Fra Joint National Committee On Prevention, Detection, Evaluering Og Behandling Av Høyt Blodtrykk. Blodtrykk. 2003;42:1206-1252.
6. Fregerio M, Oliva F, Turazza FM, Bonow RO. Forebygging og behandling av kronisk hjertesvikt ved behandling av asymptomatiske pasienter. Am J Cardiol. 2003; 91 (suppl): 4F-9F.
7. Colonna P, Sorino M, D ‘ Agostino C, et al. Ikke-farmakologisk behandling av hjertesvikt: rådgivning, diettbegrensning, rehabilitering, behandling av søvnapnø og ultrafiltrering. Am J Cardiol. 2003; 91 (suppl): 41F-50F.
8. McConaghy JR, Smith SR. Poliklinisk behandling av systolisk hjertesvikt. Am Fam Lege. 2004;70:2157-2164.
9. Young JB, Dunlap MEG, Pfeffer MA, et al. Mortalitet og sykelighet reduksjon med candesartan hos pasienter med kronisk hjertesvikt og venstre ventrikkel systolisk dysfunksjon: resultater AV CHARM lav-venstre ventrikkel ejeksjonsfraksjon studier. Sirkulasjon. 2004;110:2618-2626.
10. Cohn JN, Tognoni G. en randomisert studie av angiotensinreseptorblokkeren valsartan ved kronisk hjertesvikt. N Engl J Med. 2001;345:1667-1675.
11. Poole-Wilson PA, Swedbery K, Cleland JG, et al. Sammenligning av carvedilol og metoprolol på kliniske resultater hos pasienter med kronisk hjertesvikt i carvedilol Eller metoprolol European trial (COMET): randomized controlled trial. Lancet. 2003;362:7-13.
12. Pitt B, Zannad F, Remme WJ, et al. Effekten av spironolakton på sykelighet og dødelighet hos pasienter med alvorlig hjertesvikt. N Engl J Med. 1999;341:709-717.
13. Pitt B, Remme W, Zannad F, et al. Eplerenon, en selektiv aldosteronblokker, hos pasienter med venstre ventrikulær dysfunksjon etter hjerteinfarkt. N Engl J Med. 2003;348:1309-1321.
14. Aldactone . Chicago, IL: Pharmacia Corporation; juli 2003.
15. Ahmed A, Rik MW, Kjærlighet TE, et al. Digoksin og reduksjon i dødelighet og sykehusinnleggelse i hjertesvikt: en omfattende post hoc-analyse AV DIG-studien. Eur Hjerte J. 2006;27: 178-186.
16. Digitalis Investigation Group. Effekten av digoksin på dødelighet og sykelighet hos pasienter med hjertesvikt. N Engl J Med. 1997;336:525-533.
17. Taylor AL, Ziesche S, Yancy C, et al. Kombinasjon av isosorbiddinitrat og hydralazin hos svarte med hjertesvikt. N Engl J Med. 2004;351:2049-2057.
18. BiDil . Lexington, MA, USA: Nitromed Inc.; August 2005.
19. De Smet PA. Urtemedisin. N Engl J Med. 2002;347:2045-2056.
20. Holubarsch CJ, Colucci WS, Meinertz T, et al. Overlevelse og prognose: undersøkelse AV Crataegus Ekstrakt WS 1442 i kongestiv hjertesvikt (SPICE) – begrunnelse, studiedesign og studieprotokoll. Eur J Hjerte Mislykkes. 2000;2:431-437.
21. Bonadkar RA, Guarneri E. Koenzym Q10. Am Fam Lege. 2005;72:1065-1070.
22. Khatta M, Alexander BS, Krichten CM, et al. Effekten av coenyzme Q10 hos pasienter med kongestiv hjertesvikt. Ann Intern Med. 2000;132:636-640.
23. De Vries RJM, Van Veldhuisen DJ, Dunselman PHJM. Effekt og sikkerhet av kalsiumkanalblokkere i hjertesvikt: fokus på nyere studier med andre generasjons dihydropyridiner. Am Hjerte J. 2000;139: 185-194.
24. Delea TE, Edelsberg JS, Hagiwara M, et al. Bruk av tiazolidindioner og risiko for hjertesvikt hos personer med type 2 diabetes. Diabetes Omsorg. 2003;26:2983-2989.
25. Hollenberg NK. Betraktninger for styring av væskedynamiske problemer forbundet med tiazolidindioner. Am J Med. 2003; 115:111S-115S.
26. Avandia . Forskning Trekant Park, NC: GlaxoSmithKline; August 2005.
27. Actos . Lincolnshire, IL: Takeda Pharmaceutical American Inc.; August 2004.
for å kommentere denne artikkelen, kontakt [email protected].