a kémiai indikátort a kémiai reakció lelassítására használják a szín megváltoztatásával, amíg a reakció vagy  befejeződött vagy elérte egyensúlyi pontját. . Az indikátorok olyan komplex molekulák, amelyek maguk is gyenge savak (például fenolftalein) vagy gyenge bázisok (például metil-narancs).a kémiai indikátoroknak hat fő típusa van. ezek a szerves vegyületek.
befejeződött vagy elérte egyensúlyi pontját. . Az indikátorok olyan komplex molekulák, amelyek maguk is gyenge savak (például fenolftalein) vagy gyenge bázisok (például metil-narancs).a kémiai indikátoroknak hat fő típusa van. ezek a szerves vegyületek.
savas és lúgos oldatokban különböző színűek. különböző specifikus funkciók teljesülnek különböző típusú mutatók használatával. A lakmusz közös mutató. A savas oldatokban piros, a lúgos oldatokban kék. amelyek a következők:
- timol kék
- brómtimol kék
- metilnarancs
- fenolftalein
- lakmusz
- brómkrezol zöld
minden indikátornak van egy meghatározott színe a savas közegben, amely meghatározott pH-érték mellett az alapközegben egy másik színre változik. Például a fenolftalein az erősen savas oldatban színtelen, az erősen bázikus oldatban pedig Vörös. Körülbelül 9-es pH-értéknél megváltoztatja a színét. Ez azt jelenti, hogy a fenolftalein színtelen 9-nél kisebb pH-értékű oldatban. Ha a pH 9 felett van, a fenolftalein piros.
- Types of Indicators
- Characteristics of a chemical indicator
- indikátor választása
- indikátorok használata és alkalmazása, valamint indikátorok típusai
- 20 példák a mutatókra
- Explanation of Indicators Behavior (types of Indicators)
- példa
- az indikátor viselkedése (metil-Narancs)
- alapvető közegben
- fontos kémiai indikátorok listája
- az oldat pH-jának mérése (indikátorok típusai)
- univerzális indikátor
- a pH-mérő
Types of Indicators
- Acid-Base Indicator
- Natural acid-base indicators
- Indicators of oxidation-reduction reactions (redox)
- Adsorption (precipitation) indicators
- Metallochromic or complexometric indicators
- Chemical indicators with luminescence capacity
- Chemical moisture indicators
- Chemical indicators of sterilization
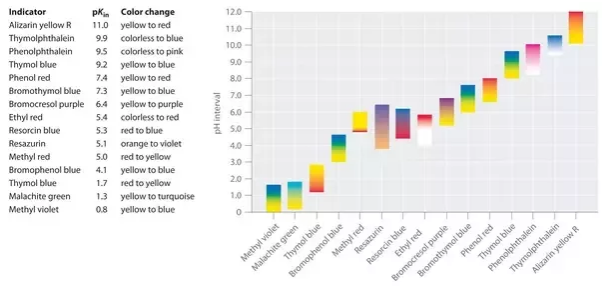
Characteristics of a chemical indicator
while you choose an indicator, meg kellett volna felelnie bizonyos jellemzőknek és egy sor követelménynek a megfelelő használat érdekében. a követelmények a következők:
- nem reagálhat anyagokkal, kémiailag tisztának kell lennie.
- nem bomlik le a teljes reakció során, és kémiailag inertnek kell maradnia.
- amikor a reakció eléri az egyensúlyi pontot vagy véget ér, a mutatónak észrevehető színűnek kell lennie.
- a fizikai integritás mértéke nem változhat, ha vastagabbá teszi.

indikátor választása
erős sav és gyenge bázis esetén metil-narancsot használnak. Erős bázis és gyenge sav esetén a fenolftaleint általában választják.
indikátorok használata és alkalmazása, valamint indikátorok típusai
a sav-bázis titrálás végpontjának megismerésére általában indikátorokat használnak.
| indikátorok | Szín savban | Szín Alapban | szín semleges állapotban |
| lakmusz | piros | Kék | Lila |
| metil-Narancs | piros | sárga | Narancs |
| fenolftalein | színtelen | Rózsaszín | színtelen |
| univerzális indikátor | piros | lila | Zöld |
20 példák a mutatókra
- Methyl Violet
- Azolythmine
- Leucomalachite green
- Methyl red
- Thymol Blue
- Bromocresol Green
- Methyl Yellow
- Methyl orange
- Bromophenol Blue
- Congo Red
- Bromocresol Purple
- Eriochrome Black
- Bromothymol Blue
- Alizarin Yellow
- Phenol Red
- Thymolphthalein
- Neutral Red
- Phenolphthalein
- Naphtholphthalein
- Cresol Red
Explanation of Indicators Behavior (types of Indicators)
az indikátor egy oldatban disszociál, és olyan iont ad, amely más színű, mint az indikátor nem disszociált molekulája.
példa
Tekintsük a metilnarancs példáját, amely vörös színű unionizált formában, sárga színű unionizált formában.
ha egy mutatót a ‘HIn’ általános képlettel ábrázolunk, akkor az indikátor disszociációja a következőképpen mutatható ki:
HIn = = = = = = H + + In–
az indikátor viselkedése (metil-Narancs)
- savas közegben
ha olyan savat adunk hozzá, amely növeli a H+ koncentrációját, akkor az egyensúly balra mozog, és az unionizált HIn dominál, és az oldat vörös lesz.
-
alapvető közegben
ha olyan bázist adunk hozzá, amely csökkenti a H+ koncentrációt, akkor az egyensúly jobbra mozog, és az ionizált ‘In’ dominál, és az oldat sárga lesz.
fontos kémiai indikátorok listája
Eriokróm Fekete: ez egy kékesfekete és komplexometrikus por indikátor, amelyet komplexometrikus titrálásokhoz használnak, és az alikvothoz adják az oldat sötétlila színének megszerzéséhez. ennek a mutatónak a leggyakoribb használata a víz keménységének meghatározása vagy a vízkeménység komplexometrikus meghatározása. kalcium-karbonát CaCO3-ból áll. amikor az összes kalcium feloldódik a víz titrálásában, az indikátor elektromos kék színt mutat.
metil-Narancs (MO): ez a legfontosabb és nagyon gyakori azoszínezékek vagy PH-indikátor a sav-bázis térfogatméréshez, amelyet gyakran használnak savval az alikvot bázisának meghatározására. ez egy gyakran használt titrálási mutató különböző iparágakban, például papír, nyomtatás, textilipar stb. nagy mennyiséget pazarolnak el és ürítenek az ipari vízhulladékba. magas PH-tartományban narancssárga színt mutat.
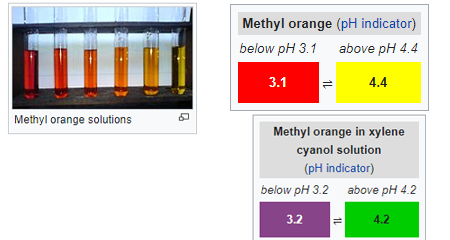
a PH-értékek megváltoztatásával külön színváltozást is mutat. bár a metilnarancs univerzális indikátorként is ismert, nem mutatja a színtartomány teljes spektrumát, és nagyon éles végpontja van.a túlzott használat ellenére bizonyos mutagén tulajdonságokkal rendelkezik, ezért kerülni kell a veszélyes anyagok közvetlen érintkezését.
metil-ibolya: a metil-ibolya a szerves vegyületekhez tartozó sav-bázis indikátorok családja (más néven gentian ibolya), amelyet széles körben használnak színezékekhez. sárga színűvé válik a metil-ibolya alacsony PH-értékén. a PH-érték 0,0-2,0 között változik kék-ibolya színben. az indikátorhoz csatolt metilcsoportok esetében könnyedén megváltoztathatjuk a festék színét.
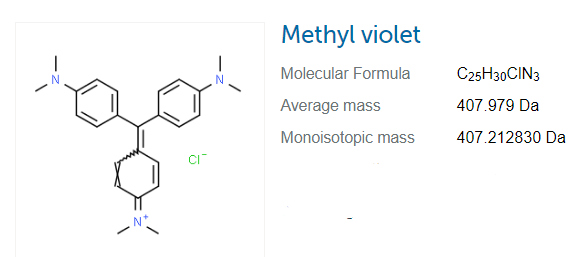
a metil-ibolya különböző színeit különböző célokra használják, például lila textíliákhoz és mély lila tintához és festékhez. a szilikagél hidratációs mutatót is tartalmaz. orvosi célokra is hasznos.
fenolftalein: egy másik fontos sav-bázis volumetria mutató, amelynek képlete C20H14O4. ez egy kémiai vegyület, amely a ftalein családba tartozik, rövid jelölésként “Hin” vagy “PHPH” néven is írható. laboratóriumi reagensként használják, és színtelen indikátor, amelynek PH-tartománya 8,5, amely rózsaszíntől sötétvörösig mutat, ha a PH-t 9,0 fölé emeli. titrálva, sav meghatározására használják alikvotban.
timol kék: a timol kék egy sav-bázis indikátor, amelyet timolszulfoneftaleinnek is neveznek, és a PH indikátorhoz használják. ez egy kristályos por, amelynek vörösesbarna vagy barnás-zöld színű, két vires vagy átmenet (savas PH és bázikus PH). a PH-érték 1,2-ről 2,8-ra változtatásával az első átmenet során sárga színűvé válik. míg a második átmenet során a PH-érték 8,0-ról 9,6-ra változik, ami kékre változik.
a timol kék univerzális indikátornak tekinthető, amely bizonyos toxikus tulajdonságokkal is rendelkezik, amelyek irritációt okozhatnak. ezért biztonságosan kell használni. sajnos nagyon veszélyes is, ha duzzadt. a fenti 10% – os érték használatakor veszélyes következményeket is okozhat.
Brómfenol Kék: brómfenol Kék is ismert, mint (tetrabromofenolftalein), és használják, mint egy közös PH indikátor. alacsony PH-értéknél sárga színt mutat, míg PH-értéknél 3,0-4,6 lilaként jelenik meg.
Kongói vörös: a Kongói Vörös egy szerves vegyület, amelyet közös sav-bázis indikátornak neveznek, amely alacsony PH-értékű oldatok kék-ibolya színévé válik. Ez válik piros pH 3,8-5,0, amely más néven Azo festék. molekuláris képlete C32H22N6Na2O6S2, amelynek molekulatömege 696,7 g/mol. A Kongói vöröset Paul Bottinger fedezte fel 1883-ban Németországban. A Kongói Vörös kolloid oldatban is vízben oldódik.
Metilvörös: a metilvörös egy sav-bázis indikátor, amelynek kémiai képlete C15H15N3O2 és moláris tömege 269,304 g/mol. C. I Acid Red 2-nek is nevezik, amely alacsony PH-érték mellett piros színt mutat, 4,4-6,2 PH-n sárgára változik. ez egy sötétvörös kristályos por és más néven Azo festék.
Bromokrezol zöld: a Bromokrezol zöld vagy BCG egy trifenil-metán festék, és sav-bázis indikátornak számít, amely alacsony PH-érték mellett sárga színt mutat. kék-zöld színűvé válik, ha a PH-értéket 3,8-5,4 között változtatja. széles körben használják titrálási célokra, mikrobiológiai növekedésre és DNS agaróz gélre, elektroforézisre. a BCG kémiai képlete C21H14Br4O5 és molekulatömege 698g / mol. jól oldódik benzolban és vízben.
az oldat pH-jának mérése (indikátorok típusai)
-
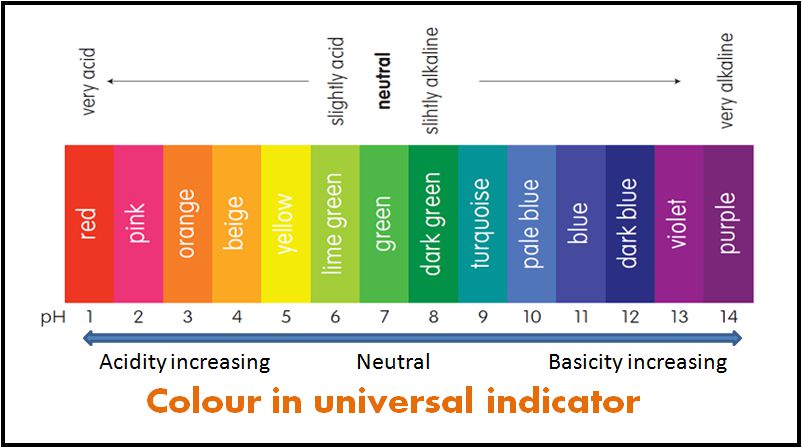
univerzális indikátor
egyes mutatókat a mutatók típusainak keverékeként használnak. A keverékjelzők különböző színeket adnak különböző pH-értékeken. Ezért az oldat pH-jának mérésére szolgál. Az ilyen vegyes mutatót univerzális mutatónak vagy egyszerűen pH-mutatónak nevezik.
az oldat pH-ját úgy lehet mérni, hogy egy darab univerzális Indikátorpapírt mártunk az oldatba. A pH-t ezután úgy találjuk meg, hogy összehasonlítjuk a kapott színt egy színdiagrammal.
-
a pH-mérő
az oldat pH-ja pH-mérővel mérhető. Ez egy mérőhöz csatlakoztatott pH-elektródból áll. Az elektródát az oldatba merítik, a mérő pedig skálán vagy digitálisan mutatja a pH-t. Ez egy sokkal megbízhatóbb és pontosabb módszer a pH mérésére, mint az univerzális Indikátorpapír, az utóbbi gyakran kényelmesebb.
ez is tetszik:
- kémcső funkció & használ
- reakciósebesség
- laboratóriumi berendezés és felhasználása