수동 수송
물질이 세포막을 가로 질러 수동적으로 움직이는 방식을 이해하기 위해서는 농도 구배와 확산을 이해해야합니다. 농도 구배는 공간에 걸쳐 물질의 농도에 차이입니다. 분자(또는 이온)는 그 공간에 똑같이 분포 될 때까지 더 집중된 곳에서 덜 집중된 곳으로 확산/확산됩니다. (분자가 이런 식으로 움직일 때,그들은 농도 구배 아래로 이동한다고합니다.)세 가지 일반적인 유형의 수동 수송에는 단순 확산,삼투 및 촉진 된 확산이 포함됩니다.
단순 확산은 입자가 고농도의 영역에서 저농도의 영역으로 이동하는 것이다. 이 개념을 설명하는 몇 가지 일반적인 예가 도움이 될 것입니다. 닫힌 욕실 안에 있다고 상상해보십시오. 향수의 병이 살포되면,냄새 분자는 병을 목욕탕의 모든 구석에 남겨둔 반점에서 자연적으로 확산할텐데,더 이상 농도 기온변화도가 남아 있을 까지 이 유포는 계속할텐데. 또 다른 예는 차 한 잔에 설탕 한 숟가락을 넣는 것입니다. 결국 설탕은 농도 기온변화도가 남아 있지 않을 때까지 차를 통하여 확산할 것이다. 두 경우 모두 방이 더 따뜻하거나 차가 더 뜨거우면 분자가 서로 부딪 히고 더 차가운 온도보다 빠르게 퍼지기 때문에 확산이 더 빨리 발생합니다. 98.6 주위에 내부 체온을 갖는 것은 또한 신체 내의 입자의 확산을 돕는다.
이 링크를 방문하여 확산 및 용액 내 분자의 운동 에너지에 의해 추진되는 방법을 확인하십시오. 온도는 확산 속도에 어떤 영향을 미치며 그 이유는 무엇입니까?
물질이 반투과성 막의 1 개의 측에 더 중대한 농도에서 원형질막과 같은 존재하다 언제든지 막의 맞은편에 그것의 농도 기온변화도의 아래 이동할 수 있는 어떤 물질든지 이렇게 할 것이다. 가스와 같은 세포막의 지질 이중층을 통해 쉽게 확산 될 수있는 물질을 고려하십시오. 이산화탄소는 일반적으로 세포 외부에 더 집중되어 있기 때문에 세포로 확산되고 이산화탄소는 일반적으로 세포 내부에 더 집중되어 있기 때문에 세포 밖으로 확산됩니다. 이 예들 중 어느 것도 세포 부분에 에너지를 필요로하지 않으므로 수동적 수송을 사용하여 막을 가로 질러 이동합니다. 계속 진행하기 전에 세포막을 가로 질러 확산 될 수있는 가스를 검토해야합니다. 세포가 급속하게 물질 대사 도중 산소높은 쪽으로 이용하기 때문에,전형적으로 외부 보다는 세포 안쪽에 산소의 더 낮은 농도가 있습니다. 그 결과로,산소는 막의 지질 이중층을 통해서 그리고 세포 내의 세포질로 간질 액체에서 직접 확산할 것입니다. 다른 한편으로는,세포가 물질 대사의 부산물로 이산화탄소를 생성하기 때문에,이산화탄소 농도는 세포질 안에 상승합니다;그러므로,이산화탄소는 세포에서 지질 이중층을 통해서 그리고 그것의 농도가 더 낮은 틈새 액체로 움직일 것입니다. 더 집중된 곳에서 더 적은 농도로 퍼지는 분자의 메커니즘은 단순 확산(그림 3.15)이라고 불리는 수동 수송의 한 형태입니다.
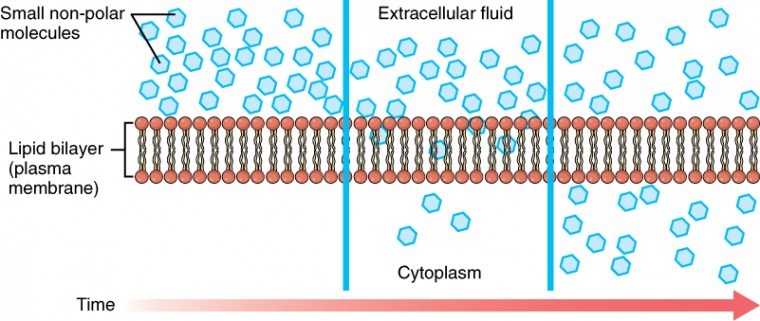
그림 3.15. 세포(플라즈마)막을 가로 지르는 단순 확산 지질 이중층의 구조는 산소 및 이산화탄소와 같은 작은 비극성 물질 만이 단순한 확산에 의해 농도 구배 아래로 세포막을 통과 할 수있게합니다.
삼투는 반투막을 통한 물 확산입니다(그림 3.16). 물 단백질 채널을 통해 또는 막 자체의 지질 꼬리 사이 미 끄 러 지 여 모든 세포의 세포 막에 걸쳐 자유롭게 이동할 수 있습니다. 그러나,그것은 물,또는 둘 다 물 세포,밖으로 이동 될 것입니다 여부를 결정 하는 물 내에서 용 질 농도.

그림 3.16. 삼투 삼투는 농도 구배 아래로 반투막을 통한 물 확산입니다. 막이 물 투과성 인 경우,물 아니지만 용질,물은 낮은 물 농도의 측면(따라서 높은 용질 농도의 측면)에 확산하여 자신의 농도를 균등화한다. 왼쪽의 비이커에서 막의 오른쪽에있는 용액은 고장 성입니다.
용액 내의 용질은 물 을 끌어 당기는 압력 인 삼투압을 생성합니다. 삼투는 세포 안쪽에 대 세포의 이상으로 용질의 불균형이 있을 때 생깁니다. 용액에 용질이 많을수록 용액이 갖는 삼투압이 커집니다. 다른 해결책 보다는 용질의 더 높은 농도가 있는 해결책은 고장성 이고 말한다. 물 분자는 더 높은 삼투압이 물(그림 3.17)을 끌어 오기 때문에 고장 성 용액으로 확산되는 경향이 있습니다. 세포가 고장성 해결책에서 두는 경우에,물 삼투를 통해 세포를 떠나는 때 세포는 주름잡거나 크레네이트할 것입니다. 반대로,다른 용액보다 용질의 농도가 낮은 용액은 저장성이라고 합니다. 저장성 용액의 세포는 너무 많은 물 을 섭취하고 팽창하여 결국 파열 될 위험이 있으며 용해 라고 불리는 과정입니다. 생물에 있는 항상성의 긴요한 양상은 바디의 세포 전부가 등장 해결책에 있는 내부 환경,2 개의 해결책에는 용질의 동일한 농도(동등한 삼투압)가 있는 환경을 창조하기 위한 것이다. 세포와 세포 외 환경이 등장 할 때,물 분자의 농도는 세포 외부와 내부에서 동일하므로 물 안팎으로 흘러 들어가고 세포는 정상적인 모양(및 기능)을 유지합니다. 다양한 장기 시스템,특히 신장은이 항상성을 유지하기 위해 작동합니다.

그림 3.17. 용액 농도 고장 성 용액은 다른 용액보다 높은 용질 농도를 갖는다. 등장 성 용액은 다른 용액과 동일한 용질 농도를 갖는다. 저장성 용액은 다른 용액보다 낮은 용질 농도를 갖는다.