Molekuly nebo ionty, které mohou buď darovat nebo přijímat proton, v závislosti na jejich situaci, se nazývají amphiprotic druhů. Nejdůležitějším amfiprotickým druhem je samotná voda. Když kyselina daruje proton do vody, molekula vody je akceptor protonů, a tedy báze. Naopak, když báze reaguje s vodou, molekula vody daruje proton, a proto působí jako kyselina.
další důležitou skupinou amfiprotických druhů jsou aminokyseliny. Každá aminokyselinová molekula obsahuje kyselou karboxylovou skupinu a bazickou aminoskupinu. Ve skutečnosti aminokyseliny obvykle existují ve zwitterionové (německy „double ion“) formě, kde se proton přenesl z karboxylu do aminoskupiny. V případě glycinu, například, zwitterion je
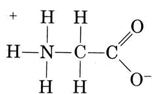
Na zwitterion mohou darovat jeden z protonů z N, stejně jako NH4+ iontů může darovat proton. Na druhou stranu, jeho COO-end může přijmout proton, stejně jako CH3COO-ion. Other common amphiprotic species are HCO3–, H2PO4–, HPO42–, and other anions derived from diprotic or triprotic acids.