Les molécules ou ions qui peuvent donner ou accepter un proton, selon leurs circonstances, sont appelées espèces amphiprotiques. L’espèce amphiprotique la plus importante est l’eau elle-même. Lorsqu’un acide donne un proton à l’eau, la molécule d’eau est un accepteur de protons, et donc une base. Inversement, lorsqu’une base réagit avec l’eau, une molécule d’eau donne un proton et agit donc comme un acide.
Un autre groupe important d’espèces amphiprotiques est les acides aminés. Chaque molécule d’acide aminé contient un groupe carboxyle acide et un groupe amino basique. En fait, les acides aminés existent généralement sous forme de zwitterion (« double ion » en allemand), où le proton est passé du groupe carboxyle au groupe amino. Dans le cas de la glycine, par exemple, le zwitterion est
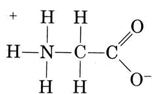
Le zwitterion peut donner l’un des protons du N, tout comme un ion NH4+ peut donner un proton. D’autre part, son extrémité COO peut accepter un proton, tout comme un ion CH3COO peut le faire. Other common amphiprotic species are HCO3–, H2PO4–, HPO42–, and other anions derived from diprotic or triprotic acids.