Un médicament biologique est défini par la législation européenne comme « un médicament qui contient une ou plusieurs substances actives fabriquées ou dérivées d’une source biologique. »1 Au sens le plus large, les médicaments biologiques comprennent toute substance fabriquée en laboratoire à partir d’un organisme vivant. Cette définition large comprend les vaccins, les immunothérapies, les biosimilaires, la thérapie génique et la thérapie par cellules souches ou tissus. Dans cet article, nous utiliserons le terme « médicaments biologiques » pour désigner les médicaments à base de protéines, tels que l’insuline.
Les sources biologiques ou naturelles comprennent les micro-organismes, les cellules animales ou les cellules humaines. Certains médicaments biologiques imitent les protéines produites naturellement dans le corps humain. Les exemples incluent l’insuline, l’hormone de croissance et les facteurs de croissance qui contrôlent la production de cellules sanguines.
Les autres médicaments biologiques ne sont pas des copies de protéines présentes naturellement dans le corps humain, mais sont améliorés en laboratoire pour améliorer la biodisponibilité, la spécificité et l’efficacité. Les exemples les plus connus sont les anticorps, qui se lient à la surface des cellules du corps et sont largement utilisés dans le traitement du cancer.
Les protéines biologiques sont des molécules beaucoup plus grandes et plus complexes que les médicaments chimiques traditionnels; cela signifie qu’elles ne peuvent pas être fabriquées sous forme de pilule, elles doivent donc être administrées par injection.
Les produits biologiques sont conçus pour avoir des effets très spécifiques et pour interagir avec des cibles spécifiques dans le corps du patient, principalement à l’extérieur des cellules. Un mécanisme d’action plus ciblé devrait conduire à une plus grande chance que le médicament ait l’effet souhaité contre la maladie et devrait entraîner moins d’effets secondaires que les médicaments traditionnels. Cependant, un effet secondaire courant des produits biologiques est le risque de réactions immunitaires (immunogénicité), le système immunitaire du patient reconnaissant le produit biologique comme une protéine « étrangère » et essayant de le détruire. Ce type de réaction immunitaire peut empêcher le produit biologique de fonctionner entièrement ou peut simplement provoquer une irritation au site d’injection.
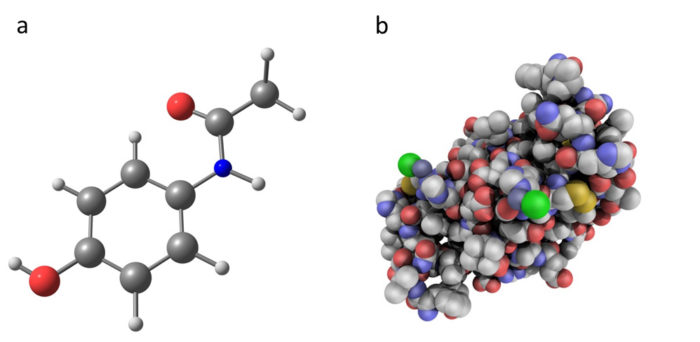 Comparaison du paracétamol (une molécule chimique) avec l’insuline (un médicament biologique). Le paracétamol, en tant que molécule chimique développée artificiellement, a une structure beaucoup plus simple que l’insuline, qui est un médicament biologique à base de protéines. Les médicaments biologiques contiennent des molécules plus grosses et plus complexes que les médicaments chimiques traditionnels.
Comparaison du paracétamol (une molécule chimique) avec l’insuline (un médicament biologique). Le paracétamol, en tant que molécule chimique développée artificiellement, a une structure beaucoup plus simple que l’insuline, qui est un médicament biologique à base de protéines. Les médicaments biologiques contiennent des molécules plus grosses et plus complexes que les médicaments chimiques traditionnels. Autres ressources
- États-Unis Food and Drug Administration (10 avril 2014). Qu’est-ce qu’un produit biologique? Extrait le 17 juin 2015 de:
http://www.fda.gov/AboutFDA/Transparency/Basics/ucm194516.htm