- Bevezetés
- anyagok és módszerek
- betegek és minták
- genetikai elemzés
- statisztikai elemzés
- etikai nyilatkozat
- eredmények
- a VHL-betegségben szenvedő betegek klinikai jellemzői
- a teljes túlélés és a CHB-specifikus túlélés VHL-betegségben szenvedő betegeknél
- egyváltozós és többváltozós Cox regressziós analízis a teljes túlélésre
- a különböző szervi érintettség hatása a CHB-specifikus túlélésre
- az RCC méretének hatása a beteg túlélésére
- megbeszélés
- Data Availability Statement
- etikai nyilatkozat
- szerzői hozzájárulások
- finanszírozás
- összeférhetetlenség
- Köszönetnyilvánítás
- Kiegészítő anyag
- rövidítések
Bevezetés
Von Hippel-Lindau (VHL) betegség (Mim 193300) egy autoszomális domináns tumor szindróma, amelyet a 3p25-en található VHL tumorszuppresszor gén csíravonal mutációi okoznak. Az incidencia ~1 a 36 000-40 000 élveszületésből, és magas penetranciával rendelkezik (1-3). Jóindulatú és rosszindulatú daganatok, beleértve a központi idegrendszer hemangioblastoma (CHB), retina hemangioblastoma (RA), vesesejtes carcinoma (RCC), pheochromocytoma (PHEO), hasnyálmirigy elváltozások, beleértve a hasnyálmirigy cisztás elváltozás, és a hasnyálmirigy neuroendokrin tumorok (PCL/PNET), endolymphatic sac tumor (ELST) és papilláris cystadenomas a mellékhere vagy széles ínszalag a fő megnyilvánulása ez a betegség (4-11). Mind az intra -, mind az interfamiliális fenotípusos heterogenitás megfigyelhető a VHL-betegségben szenvedő betegeknél (12, 13).
számos tanulmány kimutatta, hogy a VHL-betegségben szenvedő betegek túlélése rosszabb volt, mint az általános populáció. Egy 1990-es tanulmány kimutatta, hogy a medián túlélés 49 év (14) volt. Egy nemrégiben készült tanulmány szerint a férfiak és a nők várható élettartama 67, illetve 60 év volt (15). 2012-ben egy tanulmány arról számolt be, hogy a VHL-betegségben szenvedő betegek várható élettartama 52 év volt (16). A VHL-betegségben szenvedő betegek túlélésének korábban jelentett kockázati tényezői a következők voltak: korai születési év, kevesebb ellenőrző látogatás, női nem, pozitív családi anamnézis, korai betegség kezdete, csonka mutáció típusa és 3 cm-nél nagyobb RCC (15, 17, 18). Korábbi kutatások azonban nem vizsgálták az egyes szervek nagy betegcsoportban való részvételének hatásait.
a különböző szervek bevonásának a túlélésre gyakorolt hatását más szisztémás betegségekben vizsgálták. Például a méh érintettsége rosszabb túlélést jelez diffúz nagy B-sejtes limfómában szenvedő betegeknél, mint más szervek bevonásával (19). Yuda et al. beszámoltak arról, hogy a pericardialis folyadékgyülem és a több szerv érintettsége a szisztémás könnyű láncú amyloidosisban szenvedő betegek mortalitásának előrejelzői voltak (20). Bár néhány korábbi tanulmány genotípus-fenotípus összefüggést állapított meg a VHL-betegségben: a missense mutációkkal rendelkező betegeknél nagyobb valószínűséggel alakul ki pheochromocytoma, a csonka mutációkkal rendelkező betegeknél pedig nagyobb valószínűséggel alakul ki RCC és CHB (21-23). A meglévő genotípus-fenotípus korrelációk nem magyarázhatnak más komplex fenotípusokat. Ezért létfontosságú a VHL-betegség prognózisának tanulmányozása szervi részvétel szempontjából (23, 24).
ebben a tanulmányban arra törekedtünk, hogy tanulmányozzuk a teljes túlélést és a CHB-specifikus túlélést egy nagy VHL-betegségben szenvedő betegcsoportban, amely magában foglalja a tünetmentes mutációs hordozókat, és megvizsgáljuk a CHB, RCC, RA, PCL/PNET és PHEO hatását a VHL-betegségben szenvedő betegek genetikai tanácsadásának és klinikai kezelési stratégiáinak javítása érdekében.
anyagok és módszerek
betegek és minták
a Pekingi Egyetem Első Kórházában a VHL-betegségben szenvedő betegek adatbázisában tárolt összes beteginformációt felvettük. A diagnózist akkor állapították meg, amikor a betegről kiderült, hogy csíravonal VHL génmutációt hordoz, vagy teljesítette a korábban leírt klinikai kritériumokat (25, 26). Minden családban legalább egy beteget diagnosztizáltak VHL mutációs teszttel, kivéve azokat, akik elutasították a tesztet. Összesen 376 beteget diagnosztizáltak 134 családból. A klinikai adatokat, beleértve a nemet, a családi anamnézist, a mutáció típusát, az egyes szervek kezdeti életkorát és a halál okát, orvosi feljegyzések áttekintésével vagy családtagok megkérdezésével szerezték meg. Negyven beteget kizártak a vizsgálatból a nem egyértelmű adatok miatt. Végül összesen 336, 125 családból származó beteget vontak be ebbe a kohorszba, amelyben a betegek közül 298-nak volt legalább egy VHL-betegséggel összefüggő léziója, 38 beteg pedig tünetmentes mutációhordozó volt.
rögzítettük a 336 beteg túlélési állapotát születéstől halálig vagy a nyomon követés végéig 2017 júniusában. A medián követési idő 37 év/fő volt (1-75 év), összesen 12 966 személyév.
genetikai elemzés
egy QIAamp DNS vér Mini készletet (QIAGEN, Németország) használtak a genomi DNS kivonására a gyanús betegek perifériás véréből. Három kódoló exont és azok határoló intronikus régióit amplifikáltuk PCR-rel a korábban leírt primerek alkalmazásával (27). A Missense mutációkat, a splicing mutációkat és a kis indeleket közvetlen szekvenálással detektálták. Multiplex ligációtól függő szonda amplifikációs készletet (MLPA, P016-C2, MRC-Holland, Amszterdam) használtunk a nagy deléciók kimutatására. A nagy exon törléseket valós idejű kvantitatív PCR-rel igazoltuk az ebenazer által leírt primerekkel et al. (28). A betegeket egy missense mutációs csoportra (n = 162) és egy csonka mutációs csoportra (n = 174) osztották a korábban leírt kritériumok alapján (18).
statisztikai elemzés
a betegek demográfiai adatait és az alapvető klinikai adatokat leíró statisztikák segítségével elemezték. Kruskal-Wallis teszttel hasonlították össze a különböző szervekben kialakuló léziók életkorát; páronkénti összehasonlításokat végeztek, és a P értéket Bonferroni-korrekció után határozták meg. A központi idegrendszeri csoportban és a hasi csoportban a kezdeti életkorot Mann-Whitney U teszttel hasonlították össze.
mivel a nyomon követést a születéstől kezdve végezték, a betegek a betegség kezdete előtt és a betegség megjelenése után eltérő túlélési kockázattal rendelkeznek. Ez a helyzet nem felel meg az arányos veszély modell követelményeinek, így a Cox regresszióanalízis nem megfelelő. Ehelyett minden szerv bevonását időfüggő kovariánsként kezelték a Cox regressziós modellben. Egyváltozós és többváltozós Cox regressziós analízist alkalmaztak a CHB, RCC, RA, PCL/PNET és PHEO teljes túlélésre gyakorolt hatásainak értékelésére. Ezután egyváltozós és többváltozós Cox regressziós analíziseket használtunk az RCC, RA, PCL/PNET és PHEO CHB-specifikus túlélésre gyakorolt hatásának meghatározására, mivel a CHB a leggyakoribb halálok a VHL-betegségben szenvedő betegeknél.
a statisztikai elemzést SPSS 22.0 és GraphPad Prism szoftver (6-os verzió) segítségével végeztük. P < 0.05 statisztikailag szignifikánsnak tekinthető. A páros összehasonlításokhoz Bonferroni kiigazítását végeztük.
etikai nyilatkozat
ezt a tanulmányt a Pekingi Egyetem Első Kórházának (Peking, Kína) intézményi felülvizsgálati testülete hagyta jóvá, és minden beteg írásbeli beleegyezését beszerezték.
eredmények
a VHL-betegségben szenvedő betegek klinikai jellemzői
vizsgálatunkban a CHB volt a leggyakoribb elváltozás, és a betegek több mint felének volt CHB-elváltozása (62,2%). A PCL/PNET volt a második leggyakoribb lézió (46,4%). Az elhunyt betegek közel kétharmada (66,2%) halt meg CHB-ben. A CHB és a RCC prevalenciája ebben a vizsgálatban általában összhangban volt a korábbi vizsgálatok eredményeivel (1.Kiegészítő táblázat). A medián életkor a CHB és RA kialakulásakor 30 év volt, és >30 év volt az RCC, a PHEO és a PCL/PNet kialakulásakor (1.táblázat). A CHB-t és az RA-t egy központi idegrendszeri (CNS) csoportba, az RCC-t, a PHEO-t és a PCL/PNET-t pedig egy hasi csoportba egyesítettük. A kezdeti életkor eloszlását a két csoportban az 1. ábra mutatja. A daganatok megjelenésekor a medián életkor a hasi és a központi idegrendszeri csoportokban 34, illetve 29 év volt. A Mann-Whitney U teszt azt mutatta, hogy a kezdeti életkor szignifikánsan fiatalabb volt a központi idegrendszeri csoportban, mint a hasi csoportban (P < 0,001).
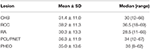
táblázat 1. Életkor a VHL-vel kapcsolatos elváltozások megjelenésekor.
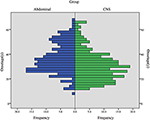
1. ábra. A kezdeti életkor gyakorisága központi idegrendszeri csoportban (beleértve a CHB & RA betegeket) és hasi csoportban (beleértve az RCC-t, a PHEO & PCL/PNET betegeket).
a teljes túlélés és a CHB-specifikus túlélés VHL-betegségben szenvedő betegeknél
a teljes túlélés és a CHB-specifikus túlélés a 2A., B. ábrán látható. a VHL-betegségben szenvedő betegek átlagos túlélési ideje 66 év volt. A CHB és az RCC együttesen az összes haláleset 95,6% – át tette ki. A betegek közel kétharmada halt meg CHB-vel kapcsolatos betegségekben, a betegek több mint egyharmada pedig RCC-ben halt meg. 209 CHB-ben szenvedő beteg közül 45 beteg halt meg CHB-ben, 10 beteg RCC-ben. 138 RCC-ben szenvedő beteg közül 16 beteg halt meg RCC-ben, 4 beteg halt meg CHB-ben. 86, mindkét elváltozásban szenvedő beteg közül a CHB és az RCC egyaránt hozzájárult az elhunyt betegekhez, mindkettő 8 halált okozott. Vizsgálatunkban a CHB volt a leggyakoribb halálok, mint az RCC (2.táblázat).
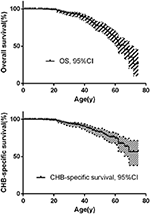
2. ábra. A) a VHL betegek teljes túlélése. (B) a VHL-betegek CHB-specifikus túlélése.
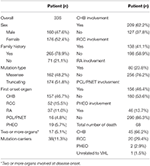
2. táblázat. A VHL-betegségben szenvedő betegek kiindulási klinikai jellemzői.
egyváltozós és többváltozós Cox regressziós analízis a teljes túlélésre
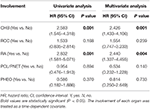
3. táblázat. Egyváltozós és többváltozós Cox regressziós analízis a teljes túlélésre.
a különböző szervi érintettség hatása a CHB-specifikus túlélésre
mert a CHB a halálozás közel kétharmadát tette ki (66.2%, 45/68) és a CHB a teljes túlélés jelentős kockázati tényezője volt mind az egyváltozós, mind a többváltozós Cox regressziós analízisekben, tovább tanulmányoztuk más szervek érintettségének a CHB-specifikus túlélésre gyakorolt hatását. Minden szerv bevonását időfüggő kovariánsként kezelték.
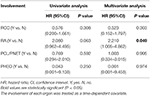
4. táblázat. Egyváltozós és többváltozós, időfüggő Cox regressziós analízis a különböző szervek érintettségének a CHB-specifikus túlélésre gyakorolt hatásáról.
az RCC méretének hatása a beteg túlélésére
adatbázisunk csak 51 beteget tartalmazott, akiknek teljes kórtörténetében RCC volt. Ezeket a betegeket további 2 csoportba soroltuk: az első csoport, az RCC átmérője <3 cm a természetük során történelem (n = 15), a második csoport, az RCC átmérője >3 cm a természetes kórtörténetük időszakában (n = 36). Az első csoport összes betege életben maradt, a második csoport három betege a nyomon követés végére meghalt; az egyik CHB-vel kapcsolatos betegségben halt meg, a másik kettő metasztatikus RCC-ben halt meg, amelynek RCC átmérője 7 és 8,5 cm volt a diagnózis idején.
megbeszélés
ebben a vizsgálatban még mindig a CHB és az RCC volt a vezető halálok a VHL-es betegeknél, együttesen az összes halálozás 95,6% – át okozták. Elemeztük az összes érintett szerv hatását a teljes túlélésre és a CHB-specifikus túlélésre a VHL-betegségben szenvedő betegeknél. A CHB és az RA a teljes túlélés független kockázati tényezői voltak. Meglepő módon az RCC nem volt jelentős kockázati tényező a teljes túlélés szempontjából. Az RA volt a CHB-specifikus túlélés egyetlen kockázati tényezője. Az elmúlt évtizedekben a VHL-betegségben szenvedő betegek halálának oka nagymértékben eltolódott. A korai években a VHL-betegséggel kapcsolatos vizsgálatokban a CHB és az RCC megközelítőleg egyenlő mértékben járult hozzá a betegek halálához; egyes vizsgálatokban az RCC okozta halálozások száma még kétszerese volt a CHB okozta halálozásnak (29). A legújabb tanulmányokban azonban a CHB-vel összefüggő halálozás aránya szignifikánsan magasabb volt, mint az RCC-vel kapcsolatos halálozás (1.Kiegészítő táblázat). Ez az eltérés részben magyarázható a fejlett képalkotó technológiák és kezelési stratégiák kifejlesztésével, beleértve a célzott terápiát, a minimálisan invazív műtétet és az RCC-k aktív megfigyelését, hozzájárulva a korai diagnózishoz és a hatékony kezeléshez az RCC-k metasztázisa előtt. Másrészt a CHB farmakológiai és sebészeti kezelését tovább kell javítani.
bár a VHL-betegség RCC-je általában kevésbé rosszindulatú és kevésbé valószínű, hogy áttétet képez, és magasabb a rák-specifikus túlélés a szórványos tiszta sejtes RCC-hez képest (30), az RCC továbbra is fontos halálok a VHL-betegeknél. A legtöbb haláleset a tumor metasztázisának és a tumorral kapcsolatos szövődményeknek köszönhető. Meglepő módon ebben a tanulmányban az RCC hatása a teljes túlélésre nem volt szignifikáns. Egy koreai tanulmány, amelyben 24 VHL-betegségben szenvedő beteg vett részt, 2009-ben hasonló eredményeket mutatott (31). Korábbi tanulmányok kimutatták, hogy az RCC átmérője >3 cm a metasztázis és a teljes túlélés kockázati tényezője (17, 32). A VHL-betegség betegadatbázisában ebben a tanulmányban elemeztük, az 51 beteg között, akiknek teljes kórtörténetében RCC tumor méret, csak 3 beteg halt meg a nyomon követés során, lehetetlenné téve a túlélési elemzés elvégzését. Jilg et al. számolt be arról, hogy a metasztázis nélküli betegek átlagos tumorátmérője szignifikánsan kisebb volt, mint a metasztázisos betegeknél (33). Duffey et al. 2004-ben arról számoltak be, hogy a 3 cm-nél kisebb RCC-ben szenvedő betegeknél alacsony volt a távoli metasztázis kockázata, és 3 cm-t ajánlott a műtéti beavatkozás határértékeként (34). Az RCC továbbra is fontos halálok a VHL-betegségben szenvedő betegeknél. A Tumor mérete és növekedési üteme nagyobb jelentőséggel bírhat a prognózis szempontjából. Nagyobb, hosszabb követési periódusú vizsgálatokra van szükség a túlélés és az RCC közötti kapcsolat tanulmányozásához.
bár a CHB jóindulatú daganatnak tekinthető, súlyos neurológiai rendellenességeket okozhat, mint például a hydrocephalus, a herniáció és az agytörzs kompressziója, és ritka esetekben intrakraniális vérzés (14, 29). A perioperatív / posztoperatív szövődmények halálhoz is vezethetnek CHB betegeknél. A CHB részvétel gyakorisága a vizsgálati mintában befolyásolhatja a túlélési elemzést. Vizsgálatunkban a betegek 62,2% – ánál (209 a 336-ból) volt CHB, ami alacsonyabb, mint a CHB-ben szenvedő betegek átlagos száma az 1.Kiegészítő táblázatban felsorolt vizsgálatokban. A CHB 66-ot tett ki.Ebben a kohorszban az összes halálos beteg 2% – a, ami magasabb, mint 6 Az 1.Kiegészítő táblázatban felsorolt 7 vizsgálat közül. Ezt a születés okozhatjaa betegek éve. Egy 2016-ban közzétett Dán tanulmányban a CHB-vel kapcsolatos halálozási arány 42% – ról (születési év 1901-1955, 18/50) 83% – ra (születési év 1956-2010, 5/6) emelkedik a születési év növekedésével, a teljes CHB-vel kapcsolatos halálozási arány 51%. A szerző ezt az eltérést az RCC diagnózisának és kezelésének előrehaladásának tulajdonította (15). Vizsgálatunkban azonban 83,3% (280 336) beteg született 1955 után, csak 16,7% (56 336)beteg született 1955 előtt. A CHB-vel kapcsolatos halálozási arány 60,1% volt az 1955 előtt született betegeknél, de 70,1 és 75% – ra nőtt az 1955-1975 között és 1975 után született betegeknél. Az RA vakságot okoz; vizsgálatunkban azonban az RA a teljes túlélés és a CHB-specifikus túlélés jelentős kockázati tényezője volt. A Retina embriológiailag az agyból származik, és mind a CHB, mind az RA ugyanazokkal a kórszövettani struktúrákkal rendelkezik (7). A hemangioblastoma onkogenezise összefügg a HIF útvonal diszregulációjával, amely a vascularis endothelialis növekedési faktor és az eritropoetin növekedéséhez vezet (35, 36). Franke et al. arról számoltak be, hogy a VHL gén deléciós mutációinak nagyobb a CHB és RA kockázata (37). Így feltételezzük, hogy az RA a CHB nagyobb terhét tükrözheti, ami a VHL-betegségben szenvedő betegek kedvezőtlen túléléséhez vezet.
a Hemangioblastoma a túlélés jelentős kockázati tényezője. Ennek másik lehetséges magyarázata a daganat korábbi kezdete. Korábbi kutatásaink azt mutatták, hogy a korai életkor a teljes túlélés és a VHL-betegség-specifikus túlélés kockázati tényezője (18). A medián életkor a CHB és RA kialakulásakor 28 volt.5, illetve 30 év volt a legkorábbi az összes VHL-vel kapcsolatos elváltozás között. Amikor a CHB-t és az RA-t központi idegrendszeri csoportként kombinálták, ez a csoport is korábban jelentkezett, mint a hasi csoport. Kruskal-Wallis tesztet végeztünk, hogy összehasonlítsuk az elváltozások kezdeti életkorát 5 szervben, és a p < 0,001 szignifikáns különbséget jelez. Továbbá páronkénti összehasonlításokat végeztünk, és a P értéket a Bonferroni-korrekció után értékeltük, és szignifikáns különbségeket találtunk Az RA-PCL/PNET, RA-RCC, CHB-PCL/PNET és CHB-RCC között (2.Kiegészítő táblázat). Ezért, bár a hemangioblastoma jóindulatú daganatnak tekinthető, korai megjelenése ronthatja a VHL-betegségben szenvedő betegek túlélését.
számos korábbi tanulmány, amely csak tüneti betegeket tartalmazott, elfogult eredményeket mutathat, amelyek túlbecsülik az érintett szervek arányát és az érintett szervek hatását a beteg túlélésére (31, 38). Először az időfüggő Cox regresszióanalízist használtuk minden érintett szerv hatásának értékelésére a VHL-betegségben szenvedő betegek túlélésére. Egy korábbi tanulmányban a teljes túlélést a betegség diagnózisától a halálig számították; a tünetmentes mutációs hordozók azonban később daganatokat alakíthatnak ki, és nem felelnek meg az arányos veszély modell követelményeinek (17).
ez a nagy retrospektív vizsgálat a VHL-betegségben szenvedő betegek túlélésének különböző szervi részvételére összpontosított klinikai szempontból. A VHL-betegségben szenvedő betegek várható élettartama 66 év volt. A teljes túlélés független kockázati tényezői a CHB és az RA jelenléte voltak. Az RCC nem volt jelentős kockázati tényező a teljes túlélés szempontjából. Az RA a CHB-specifikus túlélés kockázati tényezője volt. Az RA-ban szenvedő betegeknek gondos aktív megfigyelést kell végezniük a CHB okozta halálozás magasabb kockázata miatt. A jövőben nagyobb, hosszabb követési periódusú vizsgálatokra van szükség az RCC hatásának tanulmányozásához a VHL-betegek túlélése. Ezek az eredmények segíthetnek a jövőbeli genetikai tanácsadás és a klinikai döntéshozatal irányításában.
Data Availability Statement
az ehhez a tanulmányhoz létrehozott adatkészletek kérésre rendelkezésre állnak a megfelelő szerző számára
etikai nyilatkozat
az emberi résztvevőket érintő vizsgálatokat a Pekingi Egyetem Első Kórházának intézményi felülvizsgálati testülete (Peking, Kína) felülvizsgálta és jóváhagyta. Írásban tájékozott beleegyezés a tanulmányban való részvételhez a résztvevők törvényes gyámja/legközelebbi hozzátartozója.
szerzői hozzájárulások
KG és LC voltak felelősek a tanulmány koncepciójáért és kialakításáért. BZ és JW foglalkozott a klinikai adatokkal. Az SL és az XP végezte a statisztikai munkát. BH és JZho oltotta be a kéziratot. KM és JZha biztosítja az ábrákat és táblázatokat. Minden szerző felülvizsgálta a kéziratot.
finanszírozás
ezt a munkát a központi egyetemek alapkutatási alapjai támogatták (BMU2018JI002 támogatás).
összeférhetetlenség
a szerzők kijelentik, hogy a kutatást olyan kereskedelmi vagy pénzügyi kapcsolatok hiányában végezték, amelyek potenciális összeférhetetlenségnek tekinthetők.
Köszönetnyilvánítás
a szerzők köszönetet mondanak Li Xue-yingnek a Pekingi Egyetem Első Kórházának statisztikai osztályán a statisztikai elemzésekben nyújtott segítségért, valamint Bu Ding-fangnak, a Pekingi Egyetem Első Kórházának orvosi kísérleti Központjának technikai segítségért.
Kiegészítő anyag
rövidítések
CHB, központi idegrendszeri hemangioblastoma; RA, retina hemangioblastoma; RCC, vesesejtes carcinoma; PHEO, pheochromocytoma; PCL/PNET, hasnyálmirigy cisztás lézió és hasnyálmirigy neuroendokrin daganatok.
7. Webster AR, Maher ER, Moore AT. Az okuláris angiomatosis klinikai jellemzői von Hippel-Lindau-kórban és korreláció a csíravonal mutációval. Arch Ophthalmol. (1999) 117:371–8. doi: 10.1001 / archopht.117.3.371
PubMed Absztrakt / CrossRef Teljes Szöveg / Google Tudós
10. Wanebo JE, Lonser RR, Glenn GM, Oldfield EH. A központi idegrendszer hemangioblastómáinak természetes története von Hippel-Lindau betegségben szenvedő betegeknél. J Idegsebész. (2003) 98:82–94. doi: 10.3171 / jns.2003.98.1.0082
PubMed Absztrakt / CrossRef Teljes Szöveg / Google Tudós
13. Webster AR, Richards FM, MacRonald FE, Moore AT, Maher ER. A fenotípusos variáció elemzése a családi rák szindróma Von Hippel-Lindau-kórban: bizonyíték a módosító hatásokra. Am J Hum Genet. (1998) 63:1025–35. doi: 10.1086/302037
PubMed absztrakt / CrossRef teljes szöveg / Google Tudós
19. El-Galaly TC, Cheah CY, Hutchings M, Mikhaeel NG, Savage KJ, Sehn LH, et al. A diffúz nagy B-sejtes lymphoma esetén a méh, de nem a petefészek, a női reproduktív szervek részvétele a bemutatáskor rossz kimenetelű és a másodlagos központi idegrendszeri érintettség magas gyakoriságával jár. Br J Haematol. (2016) 175:876–83. doi: 10.1111 / bjh.14325
CrossRef Teljes Szöveg / Google Scholar
20. Yuda S, Hayashi T, Yasui K, Muranaka A, Ohnishi H, Hashimoto a, et al. A pericardialis folyadékgyülem és a több szerv érintettsége a szisztémás könnyű láncú amyloidosisban szenvedő betegek mortalitásának független előrejelzői. Gyakornok Orvos. (2015) 54:1833–40. doi: 10.2169 / belsőgyógyszer.54.3500
PubMed Absztrakt / CrossRef Teljes Szöveg / Google Tudós
27. Wu P, Zhang N, Wang X, Ning X, Li T, Bu D, et al. A von Hippel-Lindau-kór családi anamnézisében nem volt gyakori a kínai betegeknél: arra utal, hogy ezeknél a betegeknél a VHL génben a de novo mutációk nagyobb gyakorisággal fordulnak elő. J Hum Genet. (2012) 57:238–43. doi: 10.1038 / jhg.2012.10
PubMed Absztrakt / CrossRef Teljes Szöveg / Google Scholar
30. Neumann HP, Bender BU, Berger DP, Laubenberger J, Schultze-Seemann W, Wetterauer U, et al. A vesesejtes karcinóma prevalenciája, morfológiája és biológiája von Hippel-Lindau betegségben a sporadikus vesesejtes karcinómához képest. J Urol. (1998) 160:1248–54. doi: 10.1016 / S0022-5347(01)62509-6
PubMed absztrakt / CrossRef teljes szöveg / Google Tudós
31. Kim WT, Ham WS, Ju HJ, Lee JS, Lee JS, Choi YD. A vesesejtes karcinóma klinikai jellemzői von Hippel-Lindau betegségben szenvedő koreai betegeknél a sporadikus bilaterális vagy multifokális vesesejtes karcinómához képest. J Koreai Med Sci. (2009) 24:1145–9. doi: 10.3346 / jkms.2009.24.6.1145
CrossRef Teljes Szöveg / Google Scholar
35. Wizigmann-Voos S, Breier G, Risau W, lemez KH. A vascularis endothel növekedési faktor és receptorainak Up-szabályozása von Hippel-Lindau betegséggel összefüggő és szórványos hemangioblastomákban. Rák Res. (1995) 55:1358-64.
PubMed Absztrakt / Google Scholar
36. Krieg M, Marti HH, lemez KH. Az eritropoetin és a vascularis endothel növekedési faktor együttes expressziója idegrendszeri tumorokban a Von Hippel-Lindau tumorszuppresszor gén funkcióvesztésével jár. Vér. (1998) 92:3388–93.
PubMed Absztrakt / Google Scholar
37. Franke G, Bausch B, Hoffmann MM, Cybulla M, Wilhelm C, Kohlhase J, et al. Az Alu-Alu rekombináció a nagy VHL csíravonal-deléciók túlnyomó többségének alapja: molekuláris jellemzés és genotípus-fenotípus korreláció VHL betegeknél. Hum Mutat. (2009) 30:776–86. doi: 10.1002 / humu.20948
PubMed Absztrakt / CrossRef Teljes Szöveg / Google Tudós