切除療法の目標は、腸の化生を排除し、扁平上皮の再増殖を可能にするのに十分な深さまでBarrett上皮を破壊することである。 いくつかの様相は医学か外科療法を伴って巧妙な切除が制酸剤の環境を要求するようであるので、通常試みられました。
人間の調査はレーザーの無線周波数の切除(RFA)、光力学療法(PDT)、アルゴン血しょう凝固(APC)、多重極electrocoagulation(MPEC)、ヒーターの調査、さまざまな形態、endoscopic粘膜の切除(EMR)、およびcryotherapyと行われ
切除療法は、バレット食道の高悪性度異形成を有する患者のための外科的切除または食道切除術の実行可能な代替として浮上している。 実際には、ほとんどの主要な医療センターでアブレーションは、第一選択療法です。 Prasadによる調査はPdtおよびEMRと扱われたBarrettの食道の高度の異形成の患者のための5年の残存率がesophagectomyと扱われた患者のそれと対等だったことが分った。
異形成性バレット食道を有する166人の患者のレトロスペクティブコホート研究は、内視鏡的粘膜切除とアブレーションを組み合わせた管腔内療法がバレット食道の安全で効果的な治療法であることを示した。
無線周波数の切除
RFAはBarrettの食道の高級な異形成の根絶のために承認されるFDAである。 それはまた危険および利点が患者と完全に論議されれば、Barrett esophgusの低悪性度の異形成のための処置の選択である。 RFAは気球ベースの、両極無線周波数の切除システムである。 この技術は食道の目標とされた部分の内部の直径を定めるサイジングの気球の使用を要求する。 これは極性で交互になる堅く間隔をあけられた、両極電極を組み込む3cmの長い処置区域が付いている気球ベースの電極の配置に先行している。 電極は無線周波数の発電機にそれから付し、エネルギーの前もって選択された量は350Wの1秒以下に提供されます。
Shaheenらは、RFAが異形成および腸上皮化生の完全な根絶の高い割合および異形成バレット食道を有する患者における疾患進行のリスクの低下と関連してい
研究では、完全な根絶は、無線周波数アブレーションを受けた低悪性度異形成を有する患者の90.5%において、22と比較して発生した。対照群の患者の7%であり、偽の処置を受けた。 高悪性度異形成を有する患者の間では、完全な根絶は、対照群の患者のわずか19%で発生したのに対し、アブレーション群のそれらの81%で発生した。
切除群の患者は、対照群の患者よりも疾患の進行が少なく(それぞれ3.6%対16.3%)、対照群の患者よりも癌が少なかった(それぞれ1.2%対9.3%)。
バレット食道および低悪性度異形成を有する136人の患者の無作為化研究では、Phoaらは、内視鏡サーベイランスと比較して、内視鏡的無線周波数アブレーション(RFA)が有意に高悪性度異形成または腺癌への腫瘍性進行の速度を減少させることを見出した。
3年間のフォローアップで、RFAは高悪性度異形成または腺癌への進行のリスクを26.5%から1.5%に減少させた(P<。001)および腺癌への進行のリスクを8.8%から1.5%に低下させた(P=。03). アブレーション群の患者の間で、完全根絶率は、異形成のための92.6%と腸化生のための88.2%であり、サーベイランス群の患者の間で異形成のための27.9%と腸化生のための0%と比較した。
RFA前の内視鏡的粘膜切除術の使用は、barrett食道関連異形成およびBarrett食道関連粘膜内腺癌の治療失敗のリスクを有意に減少させるようであるが、治療失敗の有意な予測因子は、指標検査で柱状metapastic領域の50%以上を含む粘膜内腺癌の存在であるようである。
PDT
PDTは、特定の波長の光に曝された後に細胞内フリーラジカルを産生することにより、組織に蓄積し、局所壊死を誘導する光増感剤の使用を含む。 典型的には、ヘマトポルフィリンは、新生物組織に対してより大きな親和性を有するので、光増感剤として使用される。
内因性プロトポルフィリンIXを誘導し、より深い粘膜下層上の粘膜のための選択性を有する別の薬剤、5-アミノレブリン酸(ALA)も使用されている。 これらの結果はBarrett食道の退行,異形成および表在癌の治療に有望であった。
PTDを使用して、100人の患者(高悪性度異形成を有する73人および表在性腺癌を有する13人を含む)を治療するために、Overholtらは、Barrett粘膜が43人の患者で完全に排除され、異形成が78人の患者で排除されたことを発見した。
他の研究でも同様の奏効率が示されているが、表在扁平上皮層の下にあるバレット上皮が観察されており、より深く配置された多能性細胞が保存されている可能性があることを示している。 さらに、PDTは高く、時間のかかる努力であり、早い使用は患者の58%の膨張を要求する食道の狭窄によって複雑にされました。 PDTは切除を行うほとんどの医療センターのRFAによって主として取り替えられました。
APCアブレーション
APCは、非接触の高周波電流凝固法であり、その領域がアブレーションされるとすぐに組織の燃焼が停止する。 高出力APCを使用した一つの研究は、平均1.96セッションの後に33人の患者のうち33人の扁平上皮粘膜の完全な回復をもたらすことが報告された。 主な合併症は、患者の57.5%で発生し、3-10日間続いた胸痛および嚥下痛であった。 狭窄を経験したのは3人の患者だけであり、拡張で容易に治療された。 唯一の1内視鏡だけでなく、組織学的に、再発は10.6ヶ月の平均フォローアップで観察されたが、これは無効なニッセンfundoplicationを持つ患者であった。
他の研究では、22-29%の新扁平上皮ライニングの下のバレット上皮の残留病巣の持続性で、あまり奨励されていない;大規模な出血、穿孔、さらには死を伴う深食道潰瘍が報告されている。
MPECアブレーション
MPECは、電気焼灼プローブと直接接触することによって粘膜をアブレーションする方法です。 Samplinerらは、この技術を使用して、患者自身の食道の半分を内部統制として使用して、LSBEを有する10人の患者を治療し、10人の患者すべてが6ヶ月で視覚および生検基準によって除去された治療セグメントを有していたことを発見した。 治療は平均2.5セッションを要し、5人の患者は75セッション(一過性の嚥下障害2回、一過性の嚥下障害1回、胸痛1回、上部消化管出血1回)で合併症を有していた。
バレット食道を有する10年のフォローアップ研究139人の患者のMPECアブレーション療法は、患者の5%未満で合併症(すべてのマイナー)と関連していた。 再発バレット食道は、患者の5%未満で発生しました。 いずれの患者にも食道の腺癌または高悪性度異形成は発症しなかった。 これらの結果は,Barrett食道における粘膜切除の長期的有効性と安全性を示唆した。
レーザーの切除
レーザーはBarrettの食道の根絶のために多数の小さい調査で使用されました。 結果は、上記のものよりもこのモダリティとあまり一致していませんでした。 内視鏡的に完全または部分的な退行を示した研究は、症例の三分の一として多くの新へん平上皮の下の腺要素の持続によって混乱した。
クライオアブレーション
新しいアブレーション技術の一つは、著者の機関で開拓された液体窒素を用いた低圧クライオスプレーアブレーションです。 低圧のスプレーのcryoablation装置の部品は次の通りあります:
-
液体窒素タンク
-
電子コンソール-cryogen解放を監視し、制御するための…
-
二重フィートのペダル-カテーテルの制御のcryogen解放そして暖房のための…
-
カテーテル-多層、7-9F、上部の内視鏡を通したsupercold窒素のガスのスプレーのためのオープン先端のカテーテル
傷害のメカニズムは他のablativeの技術に関連して独特です。 凍結破壊はアポトーシスを誘導し、超低温(-76℃–196℃)で凍結壊死を引き起こし、一過性の虚血をもたらし、免疫刺激を引き起こす可能性がある。 バレット上皮はアポトーシスに抵抗性であり,したがって,凍結切除による治療に一意に適している可能性がある。
著者の施設でのパイロット研究は、異形成なしから多巣性、高悪性度の異形成に至るまでの異形成の程度とバレット食道の凍結切除を使用して、78%の症例でバレット食道の完全な内視鏡的逆転を達成し、6ヶ月のフォローアップで亜扁平上皮SIMまたは異形成はなかった。 これらの結果は、他の機関で確認する必要があります。 (下の画像を参照してください。)
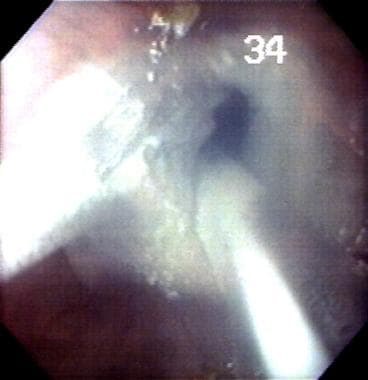 バレット食道(B E)における食道内層の凍結切除。 これは著者の研究室で行われた食道に対する最新の実験的切除療法の一つである。
バレット食道(B E)における食道内層の凍結切除。 これは著者の研究室で行われた食道に対する最新の実験的切除療法の一つである。  バレット食道(B E)における凍結切除後の食道粘膜層の水疱形成。
バレット食道(B E)における凍結切除後の食道粘膜層の水疱形成。