Molekyler Eller Ioner som enten kan donere eller akseptere et proton, avhengig av deres omstendigheter, kalles amphiprotiske arter. Den viktigste amfiprotiske arten er vann selv. Når en syre donerer et proton til vann, er vannmolekylet en protonacceptor, og dermed en base. Omvendt, når en base reagerer med vann, donerer et vannmolekyl et proton, og virker dermed som en syre.
en annen viktig gruppe amfiprotiske arter er aminosyrene. Hvert aminosyremolekyl inneholder en sur karboksylgruppe og en basisk aminogruppe. Faktisk finnes aminosyrene vanligvis i zwitterion (tysk for «dobbel ion») form, hvor protonen har overført fra karboksyl til aminogruppen. I tilfelle av glycin, for eksempel, er zwitterion
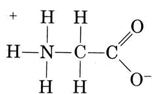
zwitterion kan donere en av protonene Fra N, akkurat som EN NH4 + ion kan donere en proton. PÅ DEN annen side kan DENS COO– end akseptere en proton, akkurat som EN CH3COO– ion kan. Other common amphiprotic species are HCO3–, H2PO4–, HPO42–, and other anions derived from diprotic or triprotic acids.