de tekniske detaljer: Kemi
atomer, som er den grundlæggende, grundlæggende enhed af alt stof, kan afvige meget fra hinanden. Selvom atomer er for små til at se uden at bruge kraftige mikroskoper, er de sammensat af endnu mindre partikler: protoner, neutroner og elektroner.
elektroner, som er ekstremt lette, negativt ladede partikler, kredser omkring en central masse-kernen i et atom. Atomer kan vinde eller miste elektroner, som ændrer atomets ladning (skaber ioner). Atomet forbliver imidlertid det samme element, uanset om det har en positiv, negativ eller neutral ladning.
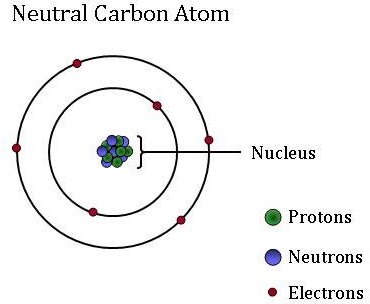
atomets lille, tætte kerne (eller center) indeholder de andre komponenter–protoner og neutroner. Protoner er positivt ladede partikler, og antallet af protoner er altid fastgjort til et bestemt element. Med andre ord er antallet af protoner det, der giver hvert element sin unikke, individuelle identitet. For eksempel har et carbonatom seks protoner, men et atom med kun fem protoner er Bor, mens et atom med syv protoner er elementet nitrogen.
neutroner er neutrale – de har ingen afgift. Isotoper er atomer af det samme element, der har et andet antal neutroner. Selvom isotoper af det samme element er tvillinger, når det kommer til reaktivitet, betyder det forskellige antal neutroner, at de har en anden masse. Visse isotoper er mere rigelige i nogle materialer end andre, da nogle fysiske og kemiske processer “foretrækker” en isotop frem for en anden. Disse forskelle i isotopisk overflod bruges som “etiketter” til at identificere de forskellige kilder til CO2, der findes i en atmosfærisk CO2-prøve. NOAA atmosfæriske forskere bruger disse isotopiske mærker til at bestemme, hvilken procentdel af det kulstof der stammer fra fossile brændstoffer, den jordiske biosfære, eller fra havet.
isotoper af kulstof
carbonisotoper kommer i tre former. Langt den mest almindelige isotop af kulstof er carbon-12 (12c), som indeholder seks neutroner ud over sine seks protoner. Den næste tungeste carbonisotop, carbon-13 (13C), har syv neutroner. Både 12C og 13C kaldes stabile isotoper, da de ikke henfalder til andre former eller elementer over tid. Den sjældne carbon-14 (14C) isotop indeholder otte neutroner i sin kerne. I modsætning til 12C og 13C er denne isotop ustabil eller radioaktiv. Over tid vil et 14C atom henfalde til et stabilt produkt.

langt størstedelen af alt kulstof, der findes på jorden, er 12c. næsten 99% af alt kulstof på jorden er af denne form. 1% af alt kulstof på jorden er af 13C isotopformen, er 14C stadig meget sjældnere. Kun en ud af hver billion carbonatomer er 14C.
for at få en ide om, hvor få 14C atomer der er sammenlignet med 12c, lad os sammenligne en til en billion. En billion er en million millioner. Hvis du linet op en billion en dollar regninger, ville det strække næsten fra jorden til solen!