- Comment une minuscule molécule comme l’éthanol peut-elle être à l’origine de tant de misère humaine? Nous proposons ici d’aller au fond des conséquences chimiques d’une nuit de fête à l’excès.
- 2.1 Métabolisme de l’éthanol
- Éthanol ⇒ Acétaldéhyde
- Acétaldéhyde ⇒ Acide acétique
- 2.2 Des changements métaboliques supplémentaires
- Prof. Klaus Roth
Comment une minuscule molécule comme l’éthanol peut-elle être à l’origine de tant de misère humaine?
Nous proposons ici d’aller au fond des conséquences chimiques d’une nuit de fête à l’excès.
2.1 Métabolisme de l’éthanol
L’éthanol (CH3CH2OH) est oxydé dans le foie en acétaldéhyde (CH3CHO, éthanal), qui dans une deuxième étape est encore oxydé en acide acétique (CH3COOH, acide éthanoïque) (Fig. 2). L’acide acétique est finalement décomposé en dioxyde de carbone et en eau dans le cycle de l’acide citrique.
Dans le procédé, l’éthanol fournit une quantité d’énergie considérable: 450 kcal / 100g, une valeur entre celles du glucose (400 kcal / 100g) et des graisses (930 kcal / 100g). Les boissons alcoolisées doivent donc être classées parmi les denrées alimentaires.
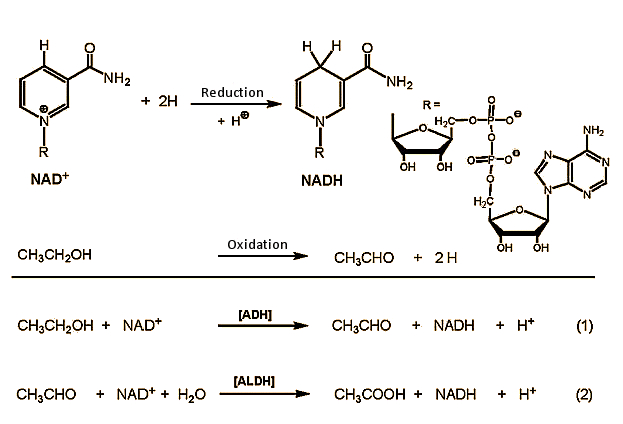
Figure 2. Métabolisme de l’éthanol dans le corps.
Éthanol ⇒ Acétaldéhyde
Dans la première étape, l’éthanol est oxydé dans les cellules du foie en acétaldéhyde, avec NAD + (nicotinamide adénine dinucléotide) comme agent oxydant. Cette réaction est catalysée par les enzymes de l’alcool déshydrogénase (ADH), dont le corps humain dispose de nombreuses. Ils sont tous structurellement très similaires et se composent toujours de deux sous-unités contenant chacune 374 acides aminés. Les sous-unités α, β et γ adaptées à l’oxydation de l’éthanol sont codées dans trois gènes de notre chromosome 4 et peuvent être combinées à volonté avec l’un des six dimères ADH (αα, ββ, γγ, αβ, αγ, βγ). Les activités catalytiques des différentes combinaisons ne diffèrent que légèrement.
En outre, il existe également diverses variétés des sous-unités β et γ. L’ADH contenant des sous-unités β1 – courantes chez les Européens – oxyde le ca. 110 mg d’éthanol par heure et kg de poids corporel, alors que la version β2, plus fréquente chez les Asiatiques, est nettement plus active catalytiquement, à 130 mg/kg/h.
Une mauvaise utilisation chronique de l’alcool induit une régulation à haut niveau dans les cellules hépatiques d’un mécanisme normalement subordonné de l’oxydation de l’éthanol: le système oxydant à l’éthanol microsomique (MEOS). Dans ce cas, une monooxygénase spéciale du cytochrome P450 est synthétisée dans une mesure accrue, qui à son tour métabolise l’éthanol indépendamment de l’ADH. Dans la séquence de réaction MEOS, l’éthanol est oxydé directement par l’oxygène moléculaire, c’est-à-dire qu’il n’y a pas de couplage énergétique avec la chaîne respiratoire dans les mitochondries. L’énergie libérée par l’oxydation de l’éthanol par MEOS est simplement rejetée sous forme de chaleur et, contrairement au métabolisme « normal » de l’ADH, elle n’est pas stockée chimiquement.
Ceci a été démontré de manière impressionnante chez l’homme: Dans une étude contrôlée, l’apport calorique quotidien normal a été doublé avec une quantité supplémentaire d’éthanol ou de chocolat. Le résultat: en utilisant de l’éthanol, le poids corporel après deux semaines est resté inchangé, mais les mangeurs de chocolat ont gagné 3 kg.
Acétaldéhyde ⇒ Acide acétique
Deux aldéhyde déshydrogénases (ALDH) sont prêtes pour une oxydation ultérieure de l’éthanol. L’oxydation rapide est également importante, car l’acétaldéhyde est toxique. Les ALDH remplissent leur tâche de manière exemplaire: l’acétaldéhyde toxique est oxydé en acide acétique inoffensif selon deux voies: une petite fraction est oxydée dans les cellules hépatiques du cytosol par l’aldéhyde déshydrogénase ALDH1, tandis que la fraction principale est oxydée dans les mitochondries par ALDH2.
Dans l’oxydation de l’alcool et de l’acétaldéhyde, le NAD + (nicotinamide adénine dinucléotide) est l’agent oxydant réel. La concentration sanguine d’acétaldéhyde reste généralement inférieure à 2 µmol /L, par rapport à une concentration typique d’éthanol de 5 mmol /L.
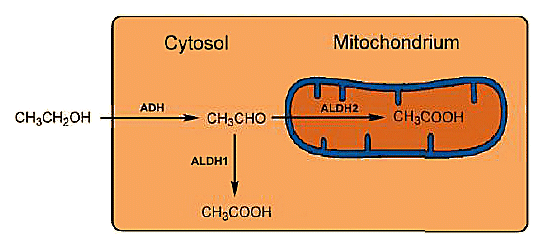
Figure 3. Métabolisme intracellulaire de l’éthanol.
Chaque ALDH se compose de quatre sous-unités identiques, chacune avec 500 acides aminés, qui dans le cas de l’ALDH1 — trouvé dans le cytosol — est localisé sur le chromosome 9, tandis que l’ALDH2 des mitochondries est localisé sur le chromosome 12. La correspondance de séquence entre les deux ALDH n’est que de 68% et leurs effets catalytiques diffèrent en conséquence: ALDH2 des mitochondries est beaucoup plus actif que ALDH1 du cytosol (Fig. 3).
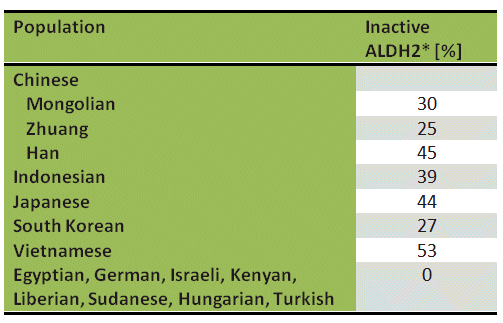
La sensibilité inhabituelle à l’alcool affichée par une partie de la population mondiale, en particulier celles d’Asie, est due à une altération de l’ALDH2. Contrairement aux Européens et aux Africains, 44% des Japonais (Tab. 1) ont une variante de l’enzyme ALDH2 dans les mitochondries de leurs cellules hépatiques. Cette modification porte la désignation ALDH2*, où un acide glutamique en position 487 a été remplacé par une lysine. La mutation est catalytiquement inactive et les personnes atteintes d’ALDH2* ne sont capables de métaboliser l’acétaldéhyde que lentement, en utilisant la voie ALDH1 moins active.
La conséquence: en quelques minutes après la consommation d’éthanol, leur concentration d’acétaldéhyde dans le sang augmente considérablement. Alors que pour un Européen (ALDH2) avec un taux d’alcoolémie de 0,5 ‰, le taux d’acétaldéhyde dans le sang reste inférieur à 2 µmol/L, pour un Japonais avec ALDH2*, cette valeur peut atteindre 35 µmol/L.
L’acétaldéhyde a un puissant effet vasodilatateur, provoquant le rougissement du visage, ou « rinçage » (syndrome de rinçage). Dans le même temps, de violents symptômes de gueule de bois apparaissent (maux de tête, tremblements, sensation de malaise).
Tableau 1. Prévalence de l’aldéhyde déshydrogénase inactive (ALDH2*) dans diverses populations ethniques.
Les symptômes identiques sont observés chez les Européens avec ALDH2 actif si l’enzyme se bloque. Cet effet peut être induit à volonté avec la préparation pharmaceutique Antabuse®, un composé qui bloque complètement ALDH2. La secousse ascendante qui en résulte dans la concentration d’acétaldéhyde, avec ses symptômes graves de gueule de bois qui l’accompagnent, afflige les toxicomanes au stade du sevrage qui suivent un traitement, après toute consommation d’alcool.
De même, après avoir savouré un plat qui se trouve contenir le champignon Coprinus atramentarius, généralement connu sous le nom de « bouchon d’encre commun » ou de « fléau de tippler », il faut, pendant les trois prochains jours, éviter strictement toutes les boissons alcoolisées (Fig. 4). Sinon, après seulement quelques minutes, des symptômes majeurs de gueule de bois se développeront tels que bouffées vasomotrices, palpitations cardiaques et pouls élevé, maux de tête, nausées, vomissements, attaques de transpiration et tremblements des membres. Les cas particulièrement graves peuvent même entraîner un effondrement. Ce tableau clinique est connu sous le nom de syndrome de Coprinus. Il peut persister plusieurs heures, bien que jusqu’à présent aucun cas de décès n’ait été enregistré.
.gif)
Figure 4. Syndrome de Coprinus.
La cause du syndrome de Coprinus est une concentration sanguine considérablement accrue d’acétaldéhyde due à un composant du champignon qui bloque l’oxydation de l’acétaldéhyde en acide acétique. Les symptômes observés sont identiques à ceux observés après la consommation d’alcool pendant le traitement par Antabuse (disulfirame). Le coupable peut être la coprine, la N5-(1-hydroxycyclopropyl)-L-glutamine (2), qui a été isolée de ce champignon. Il a été montré plus récemment que ce n’est pas la coprine elle-même qui bloque l’aldéhyde déshydrogénase ALDH2, induisant ainsi les symptômes, mais plutôt l’un de ses métabolites, probablement le 1-aminocyclopropanol (3) ou l’hydrate de cyclopropanone (4).
2.2 Des changements métaboliques supplémentaires
L’éthanol et sa dégradation — cette dernière se déroulant à une vitesse vertigineuse — entraînent des changements physiologiques qui persistent bien au-delà de la période d’intoxication. D’un point de vue chimique, l’éthanol est un agent réducteur riche en calories, dont le traitement engloutit des quantités considérables de l’agent oxydant NAD + et abaisse le rapport NAD + / NADH de 4: 1 à 2: 1. Cet abaissement du potentiel d’oxydation de la cellule provoque une altération massive et profonde du métabolisme, par exemple une diminution de la synthèse du glucose, une accumulation d’acide lactique, une production accrue de lipides et une diminution de la dégradation des graisses et des protéines.
Une synthèse du glucose diminuée à son tour abaisse le taux de sucre dans le sang, avec une faiblesse physique générale qui en résulte. Dans le cas d’un diabétique habitué aux médicaments, cela peut produire l’hypoglycémie redoutée. Pendant ce temps, l’accumulation d’acide lactique peut diminuer le pH du sang en dessous de 7,36 (acidose).
Une synthèse accrue des acides gras associée à une diminution du métabolisme des lipides (lipides) et des protéines entraîne un dépôt de graisses et de protéines dans le foie. Il s’agit d’un processus réversible en cas d’abus d’alcool occasionnel, mais dans une situation chronique, il conduit directement à un « foie gras » qui, associé à d’autres lésions du métabolisme hépatique induites par l’alcool, peut se terminer par une cirrhose du foie ou un carcinome.
La consommation d’éthanol n’est cependant pas seulement sujette à des inconvénients. La concentration plasmatique de cholestérol HDL (« bon cholestérol ») augmente et la capacité de coagulation du sang diminue. Les deux offrent une protection contre les crises cardiaques et les accidents vasculaires cérébraux, ce qui peut aider à expliquer la prévalence plus faible des maladies circulatoires mortelles dans certains pays méditerranéens (régime méditerranéen). Dans certains cas, cependant, le vin rouge y est consommé en si grandes quantités que bien que les maladies coronariennes et les accidents vasculaires cérébraux soient moins fréquents, les maladies du foie — du foie gras jusqu’au carcinome — sont d’autant plus fréquentes.
Comme toujours – librement adapté de Paracelse — la modération représente probablement le juste milieu.
-
Chimie d’une gueule de bois – L’alcool et ses conséquences Font partie 1
► En savoir plus sur la chimie d’une gueule de bois dans la partie 3
K. Roth, Chem. Unserer Zeit 2005, 39, 348. DOI: 10.1002/ ciuz.200590067
Détails de la structure et du mécanisme catalytique de l’oxydation de l’éthanol par l’ADH: www.chemie.tu-darmstadt.de/akplenio/moproc/zink/alkoholdehydrogenase / Adh_commencer.htm
C.s. Lieber, Nouvelle-Angleterre. J. Med. 1973, 288, 356. DOI: 10.1056/NEJM197302152880710
Hsu et al., Proc. Natl. Acad. Sci. 1985, 82, 3771. Lien
H. W. Goedde, D. P. Argawal, Alcoolisme, Pergamon Press, New York, 1989.
D. Crabb et al., J. Clin. Investir. 1989, 83, 314. DOI: 10.1172/ JCI113875
T. L. Wall et al., J. Stud. Alcool 2000, 61, 13. Lien
D. Michelot, Toxines naturelles 1992, 1, 73. DOI: 10.1002/nt.2620010203
G. M. Hatfield, J. P. Schaumberg, Lloydia 1975, 38, 489. IDP: 1241098
P. Lindberg et al., Chem. Comm. 1975, 946. DOI: 10.1039/C39750000946
P. Lindberg et al., J. Chem. Soc. Perkin I 1977, 684. DOI: 10.1039/P19770000684
J. S. W. Wiseman, R. H. Abeles, Biochimie 1979, 18, 427. DOI: 10.1021/bi00570a006
K. Roth, Chem. Unserer Zeit 2004, 38, 426. DOI: 10.1002/ ciuz.200490092
Prof. Klaus Roth
Freie Universität Berlin, Allemagne.
L’article a été publié en allemand dans:
- Chem. Unserer Zeit, 2007, 41, 46 – 55.
DOI: 10.1002/ciuz.200700409
et a été traduit par W. E. Russey.
Autres articles de Klaus Roth publiés par ChemViews magazine:
- Dans Espresso — Une préparation en trois étapes
Klaus Roth prouve qu’aucun chef-d’œuvre culinaire ne peut être réalisé sans une connaissance de base de la chimie
DOI: 10.1002 /chemv.201000003 - Dans Le chocolat — Le Polymorphisme Le plus noble
Klaus Roth prouve que seule la chimie est capable de produire un tel plaisir céleste
DOI:10.1002/chemv.201000021 - Dans le Vin mousseux, le Champagne & Co
Klaus Roth montre que seule la chimie peut être ce picotement
DOI:10.1002/chemv.201000047 - Dans La peur du Fugu par le chimiste
Klaus Roth montre que la peur du fugu par le chimiste ou poisson-globe s’étend jusqu’à la poision distinctive et intrigante qu’il porte
DOI:10.1002/chemv.201000104