폴리실리케이트
오르토 실리케이트 이온,시오 44-
오르토 실리케이트 이온은 다양한 미네랄에 존재하지 않는다. 수용액에서 지속하지 않을 아주 강한 기초입니다. 자연에서 그것은 불용성 염에서 산성 양이온과 함께 발견됩니다.
| |
|||
| & | |||
| & | |||
| 지 르 콘 | & | ||
| 가닛 | |||
올리고머 폴리실리케이트
고분자 실리케이트 구조는 브리징(2-좌표)산소를 필요로 한다. 브리징 산소를위한 공간을 만들기 위해,산화물은”수신”실리콘에서 제거해야합니다.
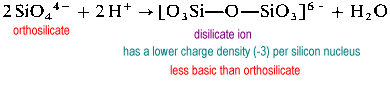
디 실리케이트 이온은 자연에서 흔하지 않습니다. 그것은 단지 희귀 한 광물에서 발견된다. 트리 실리케이트 및 테트라 실리케이트와 같은 더 큰 구조는 매우 빠릅니다.
사이 클릭 올리고머 폴리 실리케이트
긴 개방 사슬 구조를 형성하는 대신,사슬의 단부는 산화물 이온을 제거하는 링크 될 것이다.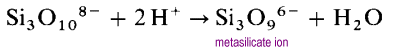
메타규산 이온은 미지의 시오 32 이온의 올리고머이다. 이러한 구조에서 각 실리콘은 두 개의 브리징 및 두 개의 말단 산소 원자를 보유합니다. 실리콘 원자 당 -2 전하 밀도가 있습니다. 가장 일반적인 순환 폴리 실리케이트는 순환 트리머이며,(시오 3)36-및 순환 헥사 머(시오 3)612-입니다.

이 경우,순환 삼량 체는 미네랄 베니토이트,바티(시 3 영 9)에서 발견된다.

| |
|
| 엔스타타이트 | |
| 디오 프 사이트 | |
선형 사슬은 산화물 이온이 다른 브리징 산소 원자로 대체되는 경우 나란히 연결될 수 있습니다. 이 연결은 각 체인의 대체 그룹 3 에서 발생하면 이중 체인 구조(시 4 영형 11)엔 6 엔-결과. 이러한 구조에서는 실리콘 원자 당 전하 및 산소 원자 수가 감소합니다.
화학식 22 의 석면광물인 크로시돌라이트가 그 예이다. 이 미네랄은 본질적으로 섬유질이며 음이온의 긴 사슬 구조에서 비롯된 화재 및 내열성 특성을 가지고 있습니다.
시트 폴리실리케이트
사슬의 좌우간 연결이 무한정 계속되면,더 많은 산화물이 제거되고 2 차원 중합체가 생성된다. 이 2 차원 폴리머는 시트 실리케이트라고하며 엔 4 엔-음이온을 포함합니다. 이 구조를 포함하는 미네랄은 얇은 시트로 쉽게 절단됩니다.
| |
|
| 미카스 | 백운모 및 흑운모 |
| 점토 광물 | 몬모릴로나이트,카올리나이트, 중국 점토 및 질석 |
| 활석 | & |
| 동석 | & |
| 크리 소 타일 석면 | & |
3-모든 산화물 이온이 삭제될 때 중합체 규산염
장은 3 차원 중합체로 연결됩니다(전부 구조에 있는 산소는 다리를 놓고 있습니다). 이 구조에는 충전되지 않은 산화물 실리카 엔 더 이상 염기성이 아니라 산성 산화물입니다. 많은 일반적인 미네랄은 석영,부싯돌,벽옥,오닉스,자수정,황수정,마노 및 옥수와 같은 구조를 포함합니다.
연속 중합 단계:
- 4:1 오르토 실리케이트에서
- 2:1 실리카에서

 중합 정도가 증가하는 순서로 다음 미네랄을 배치하십시오. 이를 위해,오/시 비율을 계산(비율이 낮을수록 더 중합 구조.2014 년 11 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년)2
중합 정도가 증가하는 순서로 다음 미네랄을 배치하십시오. 이를 위해,오/시 비율을 계산(비율이 낮을수록 더 중합 구조.2014 년 11 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년 12 월 15 일-2015 년)2 유리
산성 실리카가 매우 높은 온도(~1700 0 기음)에서 염기성 산화물과 반응 한 다음 폴리 실리케이트 이온이 너무 빠르게 냉각되어 미네랄에서 발견되는 질서있는 폴리 실리케이트 이온이 형성 될 수 있습니다. 그 결과 비정질 고체 또는 유리가 형성됩니다. 안경은 명확한 빙점이 없다는 특징이 있습니다.
단순 유리는 모래를 중탄산 나트륨 및 석회석(염기성 산화물의 원천)과 용융(융합)하여 제조된다. 이 과정에서 실리콘-산소 브리지가 파손됩니다.
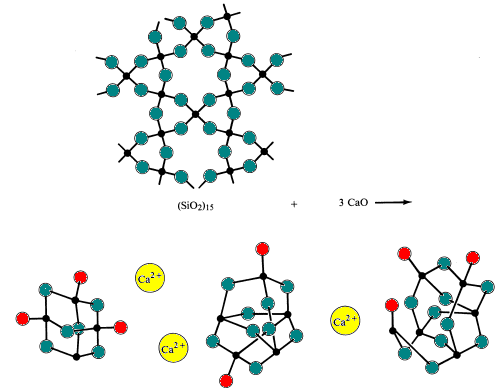
특수 유리는 유리의 산성 및 염기성 산화물의 구성을 변경하여 만들어집니다.
- 파이렉스 유리는 열충격에 매우 강합니다. 그것을 만들기 위해 10-25%비 2 탄소 3,산성 산화물,구조에 통합됩니다.
- 색깔의 안경을 통합 d-block 금속 산화물의 일부분으로 산화물을 기본 구성 요소
- 법인의 스트론튬의 산화물을 흡수하는 유리 x-선 emittd 여 컬러 텔레비젼 세트
- 미세 광학 품질에 필요한 카메라 렌즈에 의해 얻을 수 있습의 설립 La2O3
에 대해 더 알아경기에서 Corning 박물관의 유리제 리소스 사이트입니다.
토양 화학
점점 더 중합 된 폴리 실리케이트 이온이 실리콘 당 전하를 감소시켜 염기도가 낮아진다는 사실은 토양 화학에서 중요한 결과를 초래합니다.
무기물의 더 기본적인 폴리 규산 음이온,더 즉시 약한 산과 반작용하고 풍화를 겪을 것입니다.
빗물은 황 및 질소 산화물이 없더라도 용해 된 이산화탄소로 인해 다소 산성이다.
시간이 지남에 따라 빗물은 덜 중합된 규산염 음이온과 반응하여 산화물 이온을 보다 높은 중합 규산염을 생성하는 브리징 산소로 대체할 것이다. 산화물은 물 분자로 제거됩니다.
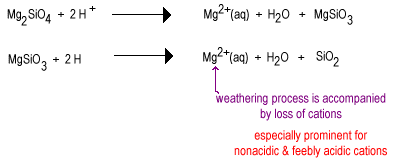
풍화의 중간 단계는 점토와 같은 많은 양의 규산염과 일부 석영을 가지고 있습니다. 이 토양은 풀이나 나무 덮개 아래 온대 지역에서 발견되는 경향이 있습니다. 이러한 토양은 비 산성 식물 영양소의 손실로 인해 새로 관개 된 사막화 토양보다 비옥하지 않습니다. 중간 토양에 존재하는 층 규산염은 식물이 필요로 하는 때 풀어 놓일 수 있는 그들의 음으로 하전된 표면에 아직도 양이온을 붙들 수 있습니다 그(것)들을. 이 토양은 여전히 비옥 한 옥수수와 밀 벨트에서 발견됩니다.
이성질 치환
폴리실리케이트 이온은 적절한 양이온에 의해 균형을 이루어야 하는 음전하를 갖는다. 터미널 산소는 음전하의 근접 포장 표면에 근접하는 음전하를 띤 표면을 가지고 있습니다. 폴리실리케이트의 음전하를 중화하기 위하여 필요한 양이온은 사슬 또는 층 사이 또는 3 차원 격자에서 존재하는 4 면체 팔면체 구멍에서 층에서 있습니다.
폴리실리케이트의 특정 형태에서 발견되는 양이온의 종류는”
- 양이온의 크기
- 양이온의 전하
같은 전하와 매우 유사한 반경을 갖는 꽤 많은 이온 세트가 존재하기 때문에,용융 된 마그마의 냉각에서 광물이 형성 될 때 이러한 일치 된 유형의 이온 중 하나가 다른 이온보다 선호되는 이유는 거의 없다.
예를 들어,이상적인 조성을 갖는 감람석은,동일한 수의 감람석 2+이온(반지름 86 분)대신에,감람석 2+(반지름 92 분)의 이소정질 자막의 다양한 백분율을 포함할 수 있다.
등형 서브시티튜션의 첫 번째 원리
등형 치환의 두 번째 원리
동형 치환은 실리케이트에서 가능한 치환의 수를 증가시킨다.또한,본 발명의 실시예에 따르면,상기 제 1 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,상기 제 2 실시예에 따르면,대부분의 규산염 광물의 양이온은 광범위하게 치환되어 대부분의 원소에 대해 비 경제적 광석을 만든다. 요소의 대각선 관계가 있습니다(특히 두 번째 기간)요소에 대한 하나의 그룹은 오른쪽에 있고 한 기간은 테이블에 있습니다.
 다음 광물 중 어느 것이 루사이트에서 이성질 치환 공정에 의해 발생할 수 있는가?
다음 광물 중 어느 것이 루사이트에서 이성질 치환 공정에 의해 발생할 수 있는가?
- K(YSi2O6)
- Rb(AlSi2O6)
- Ba(BeSi2O6)
- Ba(AlSi2O6)
힌트:두 개의 기본 원리의 이오니아는 화합물을 준수해야합니다 isomorphous 대체:
- 총 충전의 모든 양이온과 동일해야 합 총 요금의 모든 음이온.
- 치환이 등형이되기 위해서는,들어가는 양이온의 총 수가 대체되는 모든 양이온의 총 전하와 거의 같아야 한다.