Poliszilikátok
az Ortoszilikát Ion, SiO44-
az ortoszilikát ion nincs jelen sokféle ásványi anyagban. Ez egy nagyon erős bázis, amely nem marad fenn vizes oldatban. A természetben oldhatatlan sókban savas kationokkal kombinálva található meg.
| |
||
| fenacit | Be2SiO4 | & nbsp |
| willemite | Zn2SiO4 | & nbsp |
| cirkon | ZrSiO4 | & nbsp |
| gránát | (M2+) 3(M3+)2 (SiO4) 3 | M2 + = Ca, Mg, Fe M3+ = Al, Cr, Fe |
az oligomer Poliszilikátok
a polimer szilikát szerkezetek áthidaló (2-koordináta) oxigéneket igényelnek. Annak érdekében, hogy helyet biztosítson az áthidaló oxigénnek, egy oxidot el kell távolítani a “befogadó” szilíciumból.
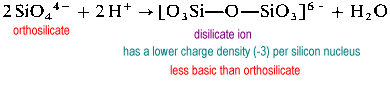
a diszilikát ion ritka a természetben. Csak a ritka thortveitit ásványi anyagban, az Sc2Si2O7-ben található meg. A nagyobb szerkezetek, például a triszilikát és a tetraszilikát rendkívül gyorsak.
ciklikus oligomer Poliszilikátok
hosszú nyitott láncszerkezetek kialakítása helyett a láncok végei összekapcsolják az oxidionokat.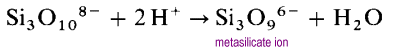
a metaszilikát ion az ismeretlen SiO32 – ion oligomerje. Ezekben a szerkezetekben minden Szilícium két áthidaló és két terminális oxigénatommal rendelkezik. Szilícium atomonként -2 töltési sűrűség van. A leggyakoribb ciklikus poliszilikátok a ciklikus trimerek (SiO3)36-és a ciklikus hexamerek (SiO3) 612 -.

a ciklikus trimer az ásványban található benitoit, BaTi (Si3O9.

Láncpoliszilikátok
lineáris (1-D) polimerek (SiO3)N2N – áthidaló oxigéneken keresztül képződhet. Ezekben a szerkezetekben Szilícium atomonként -2 töltés van. A piroxén ásványi anyagoknak nevezett ásványok csoportja ilyen típusú szerkezetű.
| |
|
| enstatit | MgSiO3 |
| diopsite | CaMgSi2O6 |
| spodimén | LiAlSi2O6 |
| pollucit | CsAlSi2O6 |
a lineáris láncok összekapcsolhatók egymás mellett, ha egy oxidiont egy másik áthidaló oxigénatommal helyettesítenek. Ha ez az összekapcsolás történik alternatív SiO3 csoportok minden láncban, egy kettős lánc struktúra (Si4O11)n6n – eredmények. Ilyen szerkezetekben csökken a töltés és az oxigénatomok száma szilíciumatomonként.
a Krokidolit, a na2fe5(OH)22 képletű azbeszt ásvány egy példa. Ez az ásványi anyag rostos jellegű, tűz – és hőálló tulajdonságokkal rendelkezik, amelyek az anion hosszú láncú szerkezetéből erednek.
Lappoliszilikátok
ha a láncok oldal-oldal összekapcsolása határozatlan ideig folytatódik, több oxid távozik, és 2-D polimer keletkezik. Ezeket a 2-D polimereket lemezszilikátoknak nevezzük, és N4N – aniont tartalmaznak. Az ezt a szerkezetet tartalmazó ásványi anyagok könnyen vékony lemezekre hasíthatók.
| |
|
| micas | moszkovita és biotit |
| agyagásványok | montmorillonit, kaolinit, Kína agyag és vermikulit |
| talkum | & nbsp |
| zsírkő | & nbsp |
| krizotil azbeszt | & nbsp |
3-D polimer szilikátok
a lapok 3D polimerré kapcsolódnak, amikor az összes oxidion eliminálódik (mind a szerkezet oxigénjei áthidalódnak). Ez a szerkezet töltetlen oxid szilícium-dioxidot tartalmaz n amely már nem bázikus, hanem inkább savas oxid. Sok közös ásványi anyag tartalmazza ezt a szerkezetet: kvarc, flint, jáspis, onyx, ametiszt, citrin, achát és kalcedon.
egymást követő polimerizációs lépések:
- az O/Si atom Arány egymást követő csökkentését eredményezi
- 4:1 ortoszilikátban
- 2:1 szilícium-dioxidban

 helyezze a következő ásványi anyagokat a polimerizáció növekvő fokának sorrendjében. Ehhez számítsa ki az O/Si arányt (minél alacsonyabb az arány, annál polimerizáltabb a szerkezet.
helyezze a következő ásványi anyagokat a polimerizáció növekvő fokának sorrendjében. Ehhez számítsa ki az O/Si arányt (minél alacsonyabb az arány, annál polimerizáltabb a szerkezet.
- pirofillit, Al2Si4O10 (OH) 2
- grunerit, Fe7Si8O22 (OH)2
- spesszartit, Mn3Al2Si3O12
- bustamit, CaMn (SiO3)2
üveg
amikor savas szilícium-dioxidot reagáltatunk bázikus oxidokkal nagyon magas hőmérsékleten (~1700 0C), majd túl gyorsan lehűtjük ahhoz, hogy a poliszilikát ionok lehetővé tegyék az ásványi anyagokban található rendezett poliszilikát ionok képződését. Az eredmény egy amorf szilárd anyag vagy üveg képződése. A szemüveget az jellemzi, hogy nincs határozott fagyáspontja.
az egyszerű üveg a homok nátrium-hidrogén-karbonáttal és mészkővel (Na2O és CaO bázikus oxidok forrásaival) történő olvasztásával (olvasztásával) készül. E folyamat során a szilícium-oxigén hidak megszakadnak.
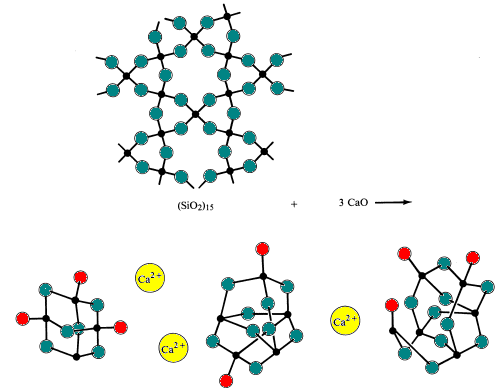
a speciális üvegek az üvegben lévő savas és bázikus oxidok összetételének megváltoztatásával készülnek.
- a Pyrex ™ üveg szokatlanul ellenáll a hősokknak. Ahhoz, hogy 10-25% B2O3, savas oxidot építünk be a szerkezetbe.
- a színes üvegek d-blokk fémoxidokat tartalmaznak az alapvető oxid komponens részeként
- a stroncium-oxid beépítése olyan üveget eredményez, amely elnyeli a színes televíziókészülékek által kibocsátott röntgensugarakat
- a fényképezőgép lencséihez szükséges finom optikai tulajdonságok La2O3 beépítésével érhetők el
Tudjon meg többet a szemüvegről itt és a Corning Múzeum Üvegforrás-oldalán.
Talajkémia
az a tény, hogy az egyre inkább polimerizált poliszilikát ionok szilíciumonkénti töltése csökken, ami alacsonyabb bázicitást eredményez, fontos következményekkel jár a talajkémiában.
minél bázikusabb egy ásvány poliszilikát anionja, annál könnyebben reagál a gyenge savakkal, és az időjárás is befolyásolja.
az esővíz kissé savas az oldott CO2 miatt, még kén és nitrogén-oxidok hiányában is.
idővel az esővíz reakcióba lép a kevésbé polimerizált szilikát anionokkal, hogy az oxidionokat áthidaló oxigénnel helyettesítse, így nagyobb mértékben polimerizált szilikát keletkezik. Az oxidokat vízmolekulák formájában távolítják el.
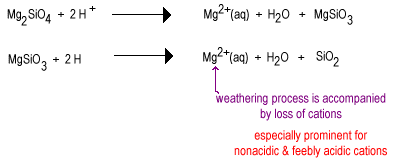
az időjárás közbenső szakaszában nagy mennyiségű rétegszilikát van, például agyag, valamint néhány kvarc. Ezek a talajok általában mérsékelt égövi területeken találhatók fű vagy fák borítása alatt. Az ilyen talajok kevésbé termékenyek, mint az újonnan öntözött sivatagi talajok a nem savas növényi tápanyag k+elvesztése miatt. A közbenső talajokban jelen lévő rétegszilikátok továbbra is tarthatnak kationokat negatív töltésű felületükön, amelyek felszabadulhatnak, mivel a növénynek szüksége van rájuk. Ezek a talajok a még mindig meglehetősen termékeny kukorica és búza övekben találhatók.
izomorf szubsztitúció
a Poliszilikát ionok negatív töltéssel rendelkeznek, amelyet megfelelő kationokkal kell ellensúlyozni. A terminális oxigének negatív töltésű felületekkel rendelkeznek, amelyek megközelítik a negatív töltésű, szorosan csomagolt felületeket. A poliszilikát negatív töltésének semlegesítéséhez szükséges kationok a láncok vagy rétegek közötti rétegekben vagy a 3-D rácsban lévő tetraéderes vagy oktaéderes lyukakban helyezkednek el.
a poliszilikát egy bizonyos formájában található kationok típusai a”
- a
- kationok méretétől
mivel jó néhány ionkészlet létezik, amelyek azonos töltéssel és nagyon hasonló sugarakkal rendelkeznek, kevés oka van annak, hogy ezen illesztett iontípusok egyikét előnyben részesítsék a másikkal szemben, amikor az olvadt magma hűtésén ásványi anyag képződik.
például az olivin, amelynek ideális összetétele Mg2SiO4, tartalmazhat különböző százalékos izomorf szubtitúciót Fe2 +(sugár 92 pm) azonos számú Mg2+ Ion helyett (sugár 86 pm).
az izomorf szubsztitúció első elve
az izomorf szubsztitúció második része
az izomorf szubsztitúció növeli a szilikátokban lehetséges szubsztitúciók számát.
példák
- K+helyettesíthető a ritka Rb+ és Tl+ ionokkal, valamint a közös Ba2+
- Ca2+helyettesíthető Sr2+(132 pm), Na+(116 pm), Y3+(104 pm), La3+ (117 pm), és a hatodik periódusú f-blokk ionok (100-117 pm)
- si4+ helyettesíthető a közös Al-Val3+ Ion (67 PM)
a legtöbb szilikát ásványi anyag kationjai nagymértékben Szubsztituáltak, ami a legtöbb elem számára nem gazdasági érceket eredményez. Az elemek átlós viszonyai vannak (különösen a második periódusban) az egyik csoporttal jobbra, egy ponttal lefelé az asztalon.
 az alábbi ásványok közül melyik keletkezhet izomorf szubsztitúciós folyamatok során a leucitban, K-ban (AlSi2O6)?
az alábbi ásványok közül melyik keletkezhet izomorf szubsztitúciós folyamatok során a leucitban, K-ban (AlSi2O6)?
- K (YSi2O6)
- Rb (AlSi2O6)
- Ba (BeSi2O6)
- Ba (AlSi2O6)
tipp: az ionos vegyületek két alapelvét kell betartani az izomorf szubsztitúció során:
- az összes kation teljes töltésének meg kell egyeznie az összes anion teljes töltésével.
- ahhoz, hogy a helyettesítés izomorf legyen, a bemenő kationok teljes számának megközelítőleg meg kell egyeznie az összes kicserélendő kation teljes töltésével.