Moléculas ou íons que podem doar ou aceitar um próton, dependendo de suas circunstâncias, são chamados de amphiprotic espécies. A espécie anfiprotica mais importante é a própria água. Quando um ácido doa um próton à água, a molécula de água é um aceitador de prótons, e, portanto, uma base. Inversamente, quando uma base reage com água, uma molécula de água doa um próton, e, portanto, age como um ácido.
outro grupo importante de espécies anfipróticas são os aminoácidos. Cada molécula de aminoácido contém um grupo carboxilo ácido e um grupo amino básico. Na verdade, os aminoácidos geralmente existem em zwitterion (alemão para “íon duplo”) forma, onde o próton se transferiu da carboxila para o grupo amino. No caso da glicina, por exemplo, o zwitterion é
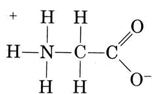
O zwitterion pode doar um dos protões de N, assim como um NH4+ íon pode doar um próton. Por outro lado, seu COO– end pode aceitar um próton, assim como um CH3COO– íon pode. Other common amphiprotic species are HCO3–, H2PO4–, HPO42–, and other anions derived from diprotic or triprotic acids.