Polysilikater
Orthosilicationen, SiO44 –
orthosilicationen er ikke til stede i en lang række mineraler. Det er en meget stærk base, som ikke vil fortsætte i vandig opløsning. I naturen findes den i kombination med sure kationer i uopløselige salte.
| |
||
| phenacit | Be2SiO4 |   |
| vilemite | Nn2sio4 |   |
| sircon | Sirsio4 |   |
| granat | (M2+)3(M3+)2(SiO4)3 | M2+ = Ca, Mg, Fe M3 + = Al, Cr, Fe |
oligomere Polysilikater
polymere silikatstrukturer kræver brodannelse (2-koordinat) iltegener. For at gøre plads til en bro ilt, skal en ilt fjernes fra “modtagende” silicium.
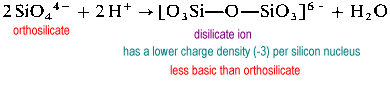
disilicationen er usædvanlig i naturen. Det findes kun i det sjældne mineral thortveitit, Sc2Si2O7. Større strukturer såsom trisilicat og tetrasilicat er ekstremt hastighed.
cykliske oligomere Polysilikater
i stedet for at danne lange åbne kædestrukturer vil enderne af kæderne forbinde eliminering af iltioner.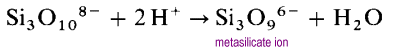
metasilicationen er en oligomer af den ukendte SiO32 – ion. I disse strukturer har hvert silicium to brodannende og to terminale iltatomer. Der er en -2 ladningstæthed pr. De mest almindelige cykliske polysilikater er de cykliske trimerer, (SiO3)36 – og de cykliske sekskamre (SiO3) 612-.

den cykliske trimer findes i mineralet benitoite, BaTi(Si3O9.

Kædepolysilikater
lineære (1-D) polymerer med formel (SiO3)n2n – kan dannes via brodannende iltegener. I disse strukturer er der en ladning på -2 pr. En gruppe af mineraler kaldet pyroksen mineraler har denne type struktur.
| |
|
| enstatit | MgSiO3 |
| diopsite | CaMgSi2O6 |
| spodimene | LiAlSi2O6 |
| pollucit | CsAlSi2O6 |
lineære kæder kan være forbundet side om side, hvis en iltion erstattes med et andet broende iltatom. Hvis denne forbindelse forekommer ved alternative SiO3-grupper i hver kæde, a dobbeltkædestruktur (Si4O11)n6n-resultater. I sådanne strukturer er der en reduktion i ladningen og antallet af iltatomer pr.
Crocidolit, et asbestmineral med formlen Na2Fe5(OH)22, er et eksempel. Dette mineral er fibrøst i naturen og har Brand-og varmebestandige egenskaber, der stammer fra anionens lange kædestruktur.
Arkpolysilikater
når side-til-side-binding af kæder fortsættes på ubestemt tid, elimineres flere iltstoffer, og der opnås en 2-D-polymer. Disse 2-D polymerer kaldes arksilicater og indeholder n4n – anionen. Mineraler indeholdende denne struktur spaltes let i tynde plader.
| |
|
| micas | muscovite og biotit |
| lermineraler | montmorillonit, kaolinit, Kina ler og vermikulit |
| talkum |   |
| fedtsten |   |
| chrysotile asbest |   |
3-D polymere silikater
ark er forbundet til en 3D-polymer, når alle ilteioner elimineres (alle ilt i strukturen bygger bro). Denne struktur indeholder uladet silica n, som ikke længere er basisk, men snarere et surt ilte. Mange almindelige mineraler indeholder denne struktur: kvarts, flint, jaspis, Onyks, ametyst, citrin, agat og Chalcedon.
Successive polymerisationstrin:
- resultat i successiv reduktion af o / Si-atomforhold
- 4:1 i orthosilicat
- 2:1 i silica

 Placer følgende mineraler i rækkefølge af stigende grad af polymerisering. For at gøre dette skal du beregne o/Si-forholdet (jo lavere forholdet er, jo mere polymeriseret strukturen.
Placer følgende mineraler i rækkefølge af stigende grad af polymerisering. For at gøre dette skal du beregne o/Si-forholdet (jo lavere forholdet er, jo mere polymeriseret strukturen.
- pyrophyllit, Al2Si4O10 (OH)2
- grunerit, Fe7Si8O22(OH)2
- spessartite, Mn3Al2Si3O12
- bustamit, CaMn(SiO3)2
glas
når sur silica omsættes med basiske iltstoffer ved meget høje temperaturer (~1700 0C) og derefter afkøles for hurtigt til, at polysilicationerne tillader dannelse af de ordnede polysilikationer, der findes i mineraler. Resultatet er dannelsen af et amorft fast stof eller glas. Briller er kendetegnet ved ikke at have noget bestemt frysepunkt.
enkelt glas fremstilles ved at smelte (smelte) sand med natriumbicarbonat og kalksten (kilder til de basiske iltstoffer Na2O og CaO). Under denne proces brydes silicium-iltbroer.
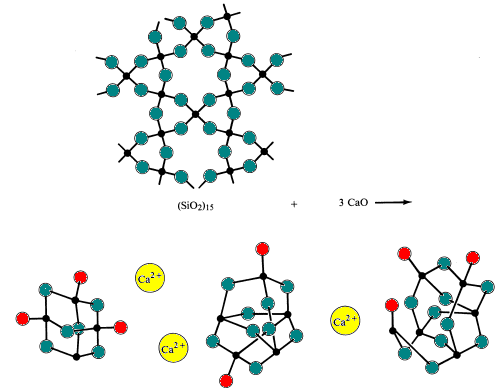
specialbriller fremstilles ved at ændre sammensætningen af sure og basiske iltstoffer i glasset.
- pyreks (TM) glas er usædvanligt modstandsdygtig over for termisk chok. For at gøre det 10-25% b2o3, et surt ilte, inkorporeres i strukturen.
- farvede briller inkorporerer d-blokmetaloksider som en del af den grundlæggende oksidkomponent
- inkorporering af strontiumoksid giver et glas, der absorberer røntgenstrålerne fra farve-TV-apparater
- de fine optiske kvaliteter, der er nødvendige i kameralinser, kan opnås ved inkorporering af La2O3
Lær mere om briller her og på Corning museums Glasressourcested.
Jordkemi
det faktum, at i stigende grad polymeriserede polysilicationer har faldende ladninger pr.
jo mere basisk polysilikatanionen af et mineral, desto lettere vil det reagere med svage syrer og gennemgå forvitring.
regnvand er noget surt på grund af opløst CO2 selv i tha fravær af svovl og kvælstofilter.
over tid vil regnvand reagere med de mindre polymeriserede silikatanioner for at erstatte iltioner med brodannende ilt, hvilket giver et mere stærkt polymeriseret silikat. Ilterne fjernes som vandmolekyler.
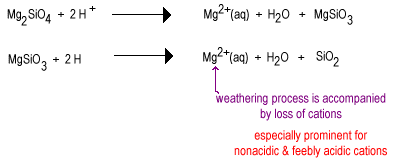
mellemstadiet af forvitring har store mængder lagsilicater såsom ler såvel som noget kvarts. Disse jordarter findes ofte i tempererede områder under et Dække af græs eller træer. Sådanne jordarter er mindre frugtbare end nyvandede ørkenjord på grund af tabet af det ikke-sure plantenæringsstof K+. Lagsilicater, der findes i mellemliggende jordarter, kan stadig holde kationer på deres negativt ladede overflader, som kan frigives, når planten har brug for dem. Disse jordarter findes i de stadig ret frugtbare majs-og hvedebælter.
isomorf Substitution
Polysilicationer har negative ladninger, der skal opvejes af passende kationer. De terminale iltegener har negativt ladede overflader, der tilnærmer tætpakkede overflader med negativ ladning. De kationer, der er nødvendige for at neutralisere polysilikatets negative ladning, er placeret i lagene mellem kæderne eller lagene eller i de tetraedriske eller oktaedriske huller, der findes i 3D-gitteret.
de typer kationer, der findes i en bestemt form for polysilikat, vil afhænge af”
- størrelsen af kationerne
- ladningen af kationerne
da der findes ganske få sæt ioner, der har samme ladning og meget lignende radier, er der ringe grund til, at en af disse matchede typer ioner foretrækkes frem for en anden, når der dannes et mineral ved afkøling af smeltet magma.
for eksempel olivin, som har en ideel sammensætning af Mg2SiO4, kan indeholde varierende procentdele af isomorf undertekstning af Fe2+ (radius 92 pm) i stedet for et lige antal Mg2+ ioner (radius 86 pm).
første princip for isomorf Subsititution
anden Pricipel af isomorf Substitution
isomorf substitution øger antallet af mulige substitutioner i silicater.
eksempler
- K+kan erstattes af de sjældne RB+-og Tl+-ioner såvel som den almindelige Ba2+
- Ca2+kan erstattes af Sr2+(132 pm), Na+(116 pm), Y3+(104 pm), La3+ (117 pm) og den sjette periode f-blokioner (100-117 pm)
- SI4+ kan erstattes af den almindelige AL3+ Ion (67 pm)
kationerne i de fleste silikatmineraler erstattes i vid udstrækning, hvilket gør ikke-økonomiske malm til de fleste grundstoffer. Der er diagonale forhold mellem elementer (især i anden periode) til elementerne en gruppe til højre og en periode nede på bordet.
 hvilke af følgende mineraler kan opstå ved isomorfe substitutionsprocesser i leucit, K(AlSi2O6)?
hvilke af følgende mineraler kan opstå ved isomorfe substitutionsprocesser i leucit, K(AlSi2O6)?
- K(YSi2O6)
- Rb(AlSi2O6)
- Ba(BeSi2O6)
- Ba(AlSi2O6)
tip: der er to grundlæggende principper for ioniske forbindelser, der skal observeres i isomorf substitution:
- den samlede ladning af alle kationer skal svare til den samlede ladning af alle anioner.
- for at substitutionen skal være isomorf, skal det samlede antal kationer, der går ind, være omtrent lig med den samlede ladning for alle kationer, der udskiftes.