El objetivo de la terapia ablativa es destruir el epitelio de Barrett a una profundidad suficiente para eliminar la metaplasia intestinal y permitir el rebrote del epitelio escamoso. Se han probado varias modalidades, generalmente en combinación con terapia médica o quirúrgica, porque la ablación exitosa parece requerir un entorno antiácido.
Se han realizado estudios en seres humanos con ablación por radiofrecuencia (ARF), terapia fotodinámica (TFD), coagulación con plasma de argón (APC), electrocoagulación multipolar (MPEC), sondas calefactoras, varias formas de láseres, resección endoscópica de la mucosa (REM) y crioterapia.
La terapia ablativa está surgiendo como una alternativa viable a la resección quirúrgica o la esofagectomía para pacientes con displasia de grado alto en el esófago de Barrett. De hecho, en la mayoría de los principales centros médicos, la ablación es una terapia de primera línea. En un estudio de Prasad, se encontró que la tasa de supervivencia a 5 años de los pacientes con displasia de grado alto en el esófago de Barrett tratados con TFD y REM fue comparable a la de los pacientes tratados con esofagectomía.
En un estudio retrospectivo de cohortes de 166 pacientes con esófago de Barrett displásico, se observó que la terapia endoluminal que combina la resección endoscópica de la mucosa y la ablación es un tratamiento seguro y eficaz para el esófago de Barrett.
Ablación por radiofrecuencia
La ARF está aprobada por la FDA para erradicar la displasia de alto grado en el esófago de Barrett. También es una opción de tratamiento para la displasia de bajo grado en el esófgo de Barrett, siempre que los riesgos y beneficios se discutan a fondo con el paciente. RFA es un sistema de ablación bipolar por radiofrecuencia basado en balón. Esta técnica requiere el uso de globos de tamaño para determinar el diámetro interno de la porción específica del esófago. Esto es seguido por la colocación de un electrodo a base de balón con un área de tratamiento de 3 cm de largo que incorpora electrodos bipolares estrechamente espaciados que se alternan en polaridad. El electrodo se conecta a un generador de radiofrecuencia y se entrega una cantidad de energía preseleccionada en menos de 1 segundo a 350 W.
Shaheen et al demostraron que la ARF se asoció con una alta tasa de erradicación completa de displasia y metaplasia intestinal y un riesgo reducido de progresión de la enfermedad en pacientes con esófago de Barrett displásico.
En el estudio, la erradicación completa se produjo en el 90,5% de los pacientes con displasia de bajo grado que recibieron ablación por radiofrecuencia, en comparación con 22.el 7% de los pacientes del grupo control se sometieron a un procedimiento simulado. Entre los pacientes con displasia de alto grado, la erradicación completa se produjo en el 81% de los del grupo de ablación, mientras que la erradicación completa se produjo en solo el 19% de los pacientes del grupo de control.
Los pacientes del grupo de ablación tuvieron menos progresión de la enfermedad que los del grupo de control (3,6 frente a 16,3%, respectivamente) y menos cánceres que los pacientes del grupo de control (1,2 frente a 9,3%, respectivamente).
En un estudio aleatorizado de 136 pacientes con esófago de Barrett y displasia de bajo grado, Phoa et al encontraron que, en comparación con la vigilancia endoscópica, la ablación endoscópica por radiofrecuencia (ARF) redujo significativamente la tasa de progresión neoplásica a displasia de alto grado o adenocarcinoma.
Durante 3 años de seguimiento, la ARF redujo el riesgo de progresión a displasia de alto grado o adenocarcinoma de 26,5 a 1,5% (P < .001) y redujo el riesgo de progresión a adenocarcinoma de 8,8 a 1,5% (P = .03). Entre los pacientes del grupo de ablación, la tasa de erradicación completa fue del 92,6% para la displasia y del 88,2% para la metaplasia intestinal, en comparación con el 27,9% para la displasia y el 0% para la metaplasia intestinal entre los pacientes del grupo de vigilancia.
El uso de la resección endoscópica de la mucosa antes de la ARF parece reducir significativamente el riesgo de fracaso del tratamiento para la displasia asociada al esófago de Barrett y el adenocarcinoma intramucoso asociado al esófago de Barrett, mientras que un factor predictivo significativo de fracaso del tratamiento parece ser la presencia de adenocarcinoma intramucoso que compromete 50% o más del área metapástica columnar en el examen índice.
TFD
La TFD implica el uso de un agente fotosensibilizante que se acumula en el tejido e induce necrosis local a través de la producción de radicales libres intracelulares tras la exposición a la luz a una longitud de onda determinada. Por lo general, una hematoporfirina se usa como agente fotosensibilizante porque tiene una mayor afinidad por el tejido neoplásico.
También se ha utilizado otro agente, el ácido 5-aminolevulínico (ALA), que induce la protoporfirina IX endógena y tiene selectividad para la mucosa sobre las capas submucosas más profundas. Los resultados han sido prometedores para la regresión del esófago de Barrett, así como para el tratamiento de la displasia y el carcinoma superficial.
Utilizando DPT para tratar a 100 pacientes, incluidos 73 con displasia de alto grado y 13 con adenocarcinoma superficial, Overholt et al encontraron que la mucosa de Barrett se eliminó por completo en 43 pacientes y la displasia se eliminó en 78 pacientes.
Otros estudios han mostrado tasas de respuesta similares, pero se ha observado epitelio de Barrett debajo de la capa escamosa superficial, lo que indica que se pueden preservar las células pluripotentes colocadas más profundas. Además, la TFD es un esfuerzo costoso y lento, y el uso temprano se complicó por la estenosis esofágica que requirió dilatación en el 58% de los pacientes. La TFD ha sido reemplazada en gran medida por la ARF en la mayoría de los centros médicos que realizan ablaciones.
Ablación de APC
APC es un método de coagulación de corriente de alta frecuencia sin contacto en el que la quema de tejido se detiene tan pronto como se ablata el área. En un estudio en el que se utilizó APC de alta potencia, se notificó que se restauró por completo la mucosa escamosa en 33 de 33 pacientes después de una media de 1,96 sesiones. Las principales complicaciones fueron dolor torácico y odinofagia, que se presentaron en el 57,5% de los pacientes y duraron de 3 a 10 días. Solo 3 pacientes experimentaron estenosis, que se trató fácilmente con dilatación. Solo se observó una recidiva endoscópica e histológica a la media de seguimiento de 10,6 meses, pero en un paciente con una funduplicatura de Nissen ineficaz.
Otros estudios han sido menos alentadores, con persistencia de focos residuales de epitelio de Barrett bajo el revestimiento neosquamoso en 22-29%; se ha informado de ulceración esofágica profunda con sangrado masivo, perforación e incluso muerte.
Ablación de la ECMP
La ECMP es un método en el que la mucosa se ablata por contacto directo con una sonda de electrocauterio. Sampliner et al utilizaron esta técnica para tratar a 10 pacientes con EEBL, utilizando la mitad del esófago del propio paciente como control interno, y encontraron que a los 10 pacientes se eliminó el segmento tratado por criterios visuales y de biopsia a los 6 meses; el segmento no tratado se mantuvo sin cambios en los pacientes, a pesar de la supresión ácida. El tratamiento duró un promedio de 2,5 sesiones, y 5 pacientes tuvieron complicaciones en 75 sesiones en total (2 odinofagia transitoria, 1 disfagia transitoria, 1 dolor torácico y 1 hemorragia gastrointestinal superior).
En un estudio de seguimiento de 10 años de 139 pacientes con esófago de Barrett, la terapia ablativa MPEC se relacionó con complicaciones (todas menores) en menos de 5% de los pacientes. Se presentó esófago de Barrett recidivante en menos de 5% de los pacientes. No se presentó adenocarcinoma ni displasia de alto grado del esófago en ninguno de los pacientes. Estos resultados indicaron la eficacia y seguridad a largo plazo de la ablación de la mucosa en el esófago de Barrett.
Ablación con láser
Los láseres se han utilizado en numerosos estudios pequeños para la erradicación del esófago de Barrett. Los resultados fueron menos consistentes con esta modalidad que con los mencionados anteriormente. Los estudios que demostraron regresión endoscópica total o parcial se confundieron por la persistencia de elementos glandulares debajo del epitelio neosquamoso en hasta un tercio de los casos.
Crioablación
Una de las técnicas ablativas más nuevas es la ablación por crioespray de baja presión con nitrógeno líquido, pionera en la institución del autor. Los componentes del dispositivo de crioablación por pulverización de baja presión son los siguientes:
-
Tanque de nitrógeno líquido
-
Consola electrónica – Para monitorear y controlar la liberación de criogenos
-
Pedal doble para controlar la liberación de criógeno y el calentamiento del catéter
-
Catéter: un catéter multicapa de punta abierta de 7 a 9 F para rociar gas nitrógeno supercolor a través de un endoscopio superior
El mecanismo de lesión es único en relación con otras técnicas ablativas. La crioablación induce la apoptosis, causa crionecrosis a temperaturas supercold (-76°C a -196°C), resulta en isquemia transitoria y puede causar estimulación inmunitaria. El epitelio de Barrett es resistente a la apoptosis y, por lo tanto, puede ser especialmente adecuado para el tratamiento por crioablación.
En un estudio piloto realizado en la institución del autor mediante crioablación en el esófago de Barrett con grados de displasia que van desde la ausencia de displasia hasta la displasia multifocal de alto grado, se logró una reversión endoscópica completa del esófago de Barrett en 78% de los casos, sin SIM subcamosa ni displasia a los 6 meses de seguimiento. Estos resultados necesitarán confirmación en otras instituciones. (Vea las imágenes a continuación.)
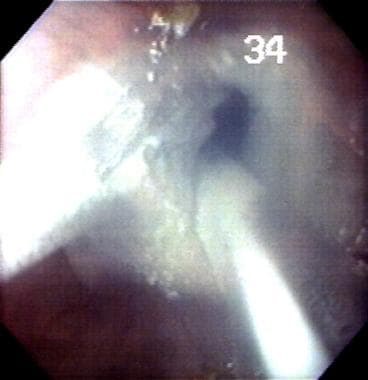 Crioablación del revestimiento esofágico en el esófago de Barrett (BE). Esta es una de las terapias ablativas experimentales más recientes para el esófago que se realiza en el laboratorio del autor.
Crioablación del revestimiento esofágico en el esófago de Barrett (BE). Esta es una de las terapias ablativas experimentales más recientes para el esófago que se realiza en el laboratorio del autor.  Formación de ampollas en la capa de la mucosa esofágica después de la crioablación en el esófago de Barrett (BE).
Formación de ampollas en la capa de la mucosa esofágica después de la crioablación en el esófago de Barrett (BE).