- Come può una piccola molecola come l’etanolo essere alla radice di tanta miseria umana?Qui proponiamo di andare a fondo delle conseguenze chimiche di una notte di festa all’eccesso.
- 2.1 Metabolismo dell’etanolo
- Etanolo ⇒ Acetaldeide
- Acetaldeide ⇒ acido acetico
- 2.2 Ulteriori cambiamenti metabolici
- Prof. Klaus Roth
Come può una piccola molecola come l’etanolo essere alla radice di tanta miseria umana?
Qui proponiamo di andare a fondo delle conseguenze chimiche di una notte di festa all’eccesso.
2.1 Metabolismo dell’etanolo
L’etanolo (CH3CH2OH) viene ossidato nel fegato in acetaldeide (CH3CHO, etanale), che in una seconda fase viene ulteriormente ossidato in acido acetico (CH3COOH, acido etanoico) (Fig. 2). L’acido acetico viene infine scomposto in anidride carbonica e acqua nel ciclo dell’acido citrico .
Nel processo, l’etanolo fornisce una notevole quantità di energia: 450 kcal/100g, un valore tra quelli di glucosio (400 kcal/100g) e grassi (930 kcal/100g). Le bevande alcoliche devono pertanto essere classificate tra i prodotti alimentari.
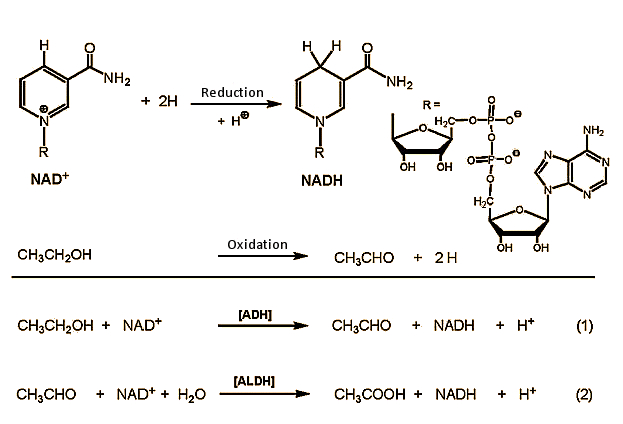
Figura 2. Metabolismo dell’etanolo nel corpo.
Etanolo ⇒ Acetaldeide
Nella prima fase, l’etanolo viene ossidato nelle cellule del fegato in acetaldeide, con NAD+ (nicotinamide adenina dinucleotide) come agente ossidante. Questa reazione è catalizzata da enzimi alcol deidrogenasi (ADH), di cui il corpo umano ha molti disponibili. Sono tutti strutturalmente molto simili e consistono sempre di due subunità, ciascuna contenente 374 aminoacidi. Le subunità α -, β-e γ adatte all’ossidazione dell’etanolo sono codificate in tre geni nel nostro cromosoma 4 e possono essere combinate a piacimento con uno qualsiasi dei sei dimeri ADH (αα, ββ, γγ, αβ, αγ, βγ). Le attività catalitiche delle varie combinazioni differiscono solo leggermente.
Inoltre, esistono anche varie varietà delle subunità β e γ. ADH contenente subunità β1-comune tra gli europei-ossida ca. 110 mg di etanolo all’ora e kg di peso corporeo, mentre la versione β2, più comune tra gli asiatici, è significativamente più cataliticamente attiva, a 130 mg/kg/h.
L’abuso cronico di alcol induce una regolazione ad alto livello nelle cellule epatiche di un meccanismo normalmente subordinato dell’ossidazione dell’etanolo: il sistema ossidante microsomiale dell’etanolo (MEOS). In questo caso, una speciale monoossigenasi del citocromo P450 viene sintetizzata in misura maggiore, che a sua volta metabolizza l’etanolo indipendentemente dall’ADH. Nella sequenza di reazione MEOS, l’etanolo viene ossidato direttamente dall’ossigeno molecolare, cioè non vi è alcun accoppiamento energetico con la catena respiratoria nei mitocondri. L’energia rilasciata attraverso l’ossidazione di MEOS dell’etanolo viene semplicemente scartata sotto forma di calore e, a differenza del “normale” metabolismo dell’ADH, non viene immagazzinata chimicamente.
Ciò è stato dimostrato in modo impressionante con gli esseri umani: in uno studio controllato, il normale apporto calorico giornaliero è stato raddoppiato con una quantità supplementare di etanolo o cioccolato. Il risultato: usando l’etanolo, i pesi corporei dopo due settimane sono rimasti invariati, ma i mangiatori di cioccolato hanno guadagnato 3 kg .
Acetaldeide ⇒ acido acetico
Due aldeide deidrogenasi (ALDHs) sono pronti per un’ulteriore ossidazione dell’etanolo. Anche l’ossidazione rapida è importante, poiché l’acetaldeide è tossica. Gli ALDH svolgono il loro compito in modo esemplare: l’acetaldeide tossica viene ossidata in acido acetico innocuo lungo due percorsi: una piccola frazione viene ossidata nelle cellule del fegato nel citosol dall’aldeide deidrogenasi ALDH1, mentre la frazione principale viene ossidata nei mitocondri da ALDH2.
Nell’ossidazione sia dell’alcool che dell’acetaldeide, NAD+ (nicotinamide adenina dinucleotide) è l’agente ossidante effettivo. La concentrazione ematica di acetaldeide rimane generalmente inferiore a 2 µmol / L, rispetto a una tipica concentrazione di etanolo di 5 mmol / L.
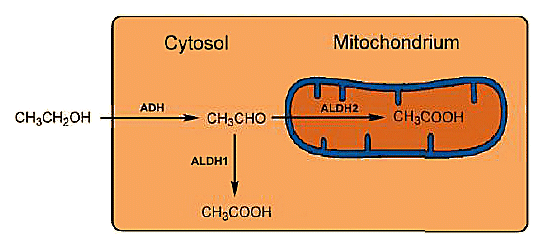
Figura 3. Metabolismo intracellulare di etanolo.
Ogni ALDH è costituito da quattro subunità identiche, ciascuna con 500 aminoacidi, che nel caso di ALDH1 — trovato nel citosol — è localizzato sul cromosoma 9, mentre ALDH2 dai mitocondri è localizzato sul cromosoma 12. La corrispondenza di sequenza tra i due ALDH è solo del 68% e i loro effetti catalitici differiscono di conseguenza: ALDH2 dai mitocondri è molto più attivo di ALDH1 dal citosol (Fig. 3).
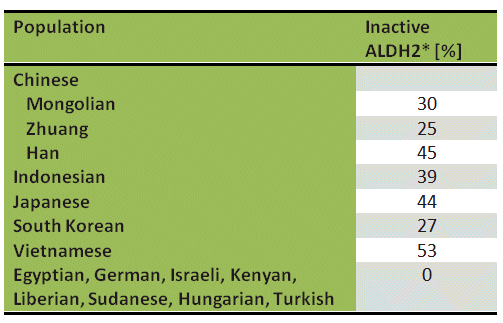
L’insolita sensibilità all’alcol mostrata da parte della popolazione mondiale, in particolare da quella asiatica, è dovuta a un ALDH2 alterato. A differenza di europei e africani, il 44% dei giapponesi (Tab. 1) avere una variante enzimatica ALDH2 nei mitocondri delle loro cellule epatiche. Questa modifica porta la designazione ALDH2*, dove un acido glutammico in posizione 487 è stato sostituito da una lisina . La mutazione è cataliticamente inattiva e le persone con ALDH2 * sono in grado di metabolizzare l’acetaldeide solo lentamente, utilizzando la via ALDH1 meno attiva.
La conseguenza: entro pochi minuti dal consumo di etanolo, la loro concentrazione di sangue-acetaldeide aumenta drammaticamente. Mentre per un europeo (ALDH2) con un tenore di alcol nel sangue di 0,5 ‰ il livello di acetaldeide nel sangue rimane inferiore a 2 µmol/L, per un giapponese con ALDH2*, questo valore può raggiungere 35 µmol/L .
L’acetaldeide ha un potente effetto vasodilatatore, causando il rossore del viso o” rossore ” (sindrome da vampate di calore). Allo stesso tempo, si verificano sintomi violenti simili a sbornia (mal di testa, tremori, sensazione di malessere) .
Tabella 1. Prevalenza di aldeide deidrogenasi inattiva (ALDH2*) in varie popolazioni etniche .
I sintomi identici si osservano per gli europei con ALDH2 attivo se l’enzima viene bloccato. Questo effetto può essere indotto a piacimento con la preparazione farmaceutica Antabuse®, un composto che blocca completamente ALDH2. La conseguente scossa verso l’alto nella concentrazione di acetaldeide, con i suoi gravi sintomi di sbornia che accompagnano, affligge i tossicodipendenti nella fase di astinenza che sono sottoposti a trattamento, dopo ogni indulgenza in alcol.
Allo stesso modo, dopo aver assaporato un piatto che capita di contenere il Coprinus atramentarius di funghi, generalmente noto come “common ink cap” o “tippler’s bane”, si dovrebbe, per i prossimi tre giorni, evitare rigorosamente tutte le bevande alcoliche (Fig. 4). Altrimenti, dopo pochi minuti, si svilupperanno i principali sintomi della sbornia come vampate di calore, palpitazioni cardiache e polso elevato, mal di testa, nausea, vomito, attacchi di sudorazione e tremore degli arti. Casi particolarmente gravi possono persino provocare un collasso . Questo quadro clinico è noto come sindrome di Coprinus. Può persistere per diverse ore, anche se finora non sono stati registrati casi di morte.
.gif)
Figura 4. Sindrome di Coprinus.
La causa della sindrome di Coprinus è una concentrazione di sangue-acetaldeide notevolmente aumentata a causa di un componente del fungo che blocca l’ossidazione dell’acetaldeide in acido acetico. I sintomi osservati sono identici a quelli osservati dopo l’assunzione di alcol durante il trattamento con Antabuse (disulfiram) . Il colpevole può essere coprin, N5-(1-idrossiciclopropil) – L-glutammina (2), che è stato isolato da questo fungo . Più recentemente è stato dimostrato che non è la coprina stessa a bloccare l’aldeide deidrogenasi ALDH2, inducendo così i sintomi, ma piuttosto uno dei suoi metaboliti, probabilmente 1-aminociclopropanolo (3) o l’idrato di ciclopropanone (4) .
2.2 Ulteriori cambiamenti metabolici
L’etanolo e la sua degradazione — quest’ultima che procede a rotta di collo — portano a cambiamenti fisiologici che persistono ben oltre il periodo di intossicazione. Da un punto di vista chimico, l’etanolo è un agente riducente ricco di calorie, la cui lavorazione assorbe quantità considerevoli dell’agente ossidante NAD+ e abbassa il rapporto NAD+/NADH da 4:1 a 2:1. Questo abbassamento del potenziale di ossidazione della cellula provoca un’alterazione massiccia e di vasta portata nel metabolismo, ad esempio una diminuzione della sintesi del glucosio, l’accumulo di acido lattico, una maggiore produzione di lipidi e una diminuzione della degradazione di grassi e proteine.
La ridotta sintesi del glucosio a sua volta abbassa il livello di zucchero nel sangue, con conseguente debolezza fisica generale. Nel caso di un diabetico abituato ai farmaci, questo può produrre la temuta ipoglicemia. Nel frattempo, l’accumulo di acido lattico può diminuire il pH del sangue al di sotto di 7,36 (acidosi).
La sintesi accresciuta degli acidi grassi insieme alla diminuzione del metabolismo lipidico (grasso) e proteico porta alla deposizione di grassi e proteine nel fegato. Questo è un processo reversibile in caso di abuso occasionale di alcol, ma in una situazione cronica porta direttamente al “fegato grasso”, che insieme a ulteriori danni indotti dall’alcol al metabolismo epatico può finire in cirrosi epatica o carcinoma.
Il consumo di etanolo è tuttavia soggetto non solo a svantaggi. La concentrazione plasmatica di colesterolo HDL (“colesterolo buono”) aumenta e la capacità coagulante del sangue diminuisce. Entrambi offrono protezione contro attacchi cardiaci e ictus , il che può aiutare a spiegare la minore prevalenza di malattie circolatorie fatali in alcuni paesi del Mediterraneo (dieta mediterranea). In alcuni casi, tuttavia, il vino rosso viene consumato in quantità tali che, sebbene la malattia coronarica e l’ictus siano meno comuni, le malattie del fegato — dal fegato grasso fino al carcinoma — sono tanto più comuni.
Come sempre — liberamente adattato da Paracelso — la moderazione rappresenta probabilmente la media aurea.
-
Chimica di una sbornia-Alcol e le sue conseguenze Parte 1
► Per saperne di più sulla chimica di una sbornia nella parte 3
K. Roth, Chem. Unserer Zeit 2005, 39, 348. DOI: 10.1002 / ciuz.200590067
Dettagli della struttura e del meccanismo catalitico dell’ossidazione dell’etanolo con ADH: www.chemie.tu-darmstadt.de/akplenio/moproc/zink/alkoholdehydrogenase / ADH_start.htm
C. S. Lieber, Nuova Inghilterra. J. Med. 1973, 288, 356. DOI: 10.1056 / NEJM197302152880710
Hsu et al., Proc. Natl. Acad. Sic. 1985, 82, 3771. 1538 >
H. W. Goedde, D. P. Argawal, Alcolismo, Pergamon Press, New York 1989.
D. Crabb et al., J. Clin. Investire. 1989, 83, 314. DOI: 10.1172 / JCI113875
TL Wall et al., J. Stud. Alcol 2000, 61, 13. Link
D. Michelot, Tossine naturali 1992, 1, 73. DOI: 10.1002 / nt. 2620010203
G. M. Hatfield, J. P. Schaumberg, Lloydia 1975, 38, 489. PMID: 1241098
P. Lindberg et al., Chimica. Comunicazioni. 1975, 946. DOI: 10.1039 / C39750000946
P. Lindberg et al., J. Chem. Soc. Perkin I 1977, 684. DOI: 10.1039 / P19770000684
J. S. W. Wiseman, RH Abeles, Biochemistry 1979, 18, 427. DOI: 10.1021 / bi00570a006
K. Roth, Chem. Unserer Zeit 2004, 38, 426. DOI: 10.1002 / ciuz.200490092
Prof. Klaus Roth
Freie Universität Berlin, Germania.
L’articolo è stato pubblicato in tedesco in:
- Chimica. Unserer Zeit, 2007, 41, 46-55.
DOI: 10.1002 / ciuz.200700409
ed è stato tradotto da W. E. Russey.
Altri articoli di Klaus Roth pubblicati dalla rivista ChemViews:
- In Espresso — Una preparazione in tre fasi
Klaus Roth dimostra che nessun capolavoro culinario può essere raggiunto senza una conoscenza di base della chimica
DOI: 10.1002 / chemv.201000003 - Nel cioccolato — Il polimorfismo più nobile
Klaus Roth dimostra che solo la chimica è in grado di produrre un tale piacere celeste
DOI: 10.1002/chemv.201000021 - Nel vino spumante, Champagne & Co
Klaus Roth mostra che solo la chimica può essere questo formicolio
DOI: 10.1002/chemv.201000047 - In The Chemist’s Fear of the Fugu
Klaus Roth mostra la paura del chimico del fugu o pesce palla si estende fino alla posizione distintiva e intrigante che porta
DOI: 10.1002/chemv.201000104