De Tekniske Detaljene: Kjemi
Atomer, som er den grunnleggende, grunnleggende enheten av all materie, kan avvike sterkt fra hverandre. Selv om atomer er for små til å se uten å bruke kraftige mikroskoper, består de av enda mindre partikler: protoner, nøytroner og elektroner.
Elektroner, som er ekstremt lette, negativt ladede partikler, bane rundt en sentral masse-kjernen til et atom. Atomer kan få eller miste elektroner, som endrer ladningen av atomet (skaper ioner). Atomet forblir imidlertid det samme elementet om det har en positiv, negativ eller nøytral ladning.
den lille, tette kjernen (eller sentrum) av atomet inneholder de andre komponentene–protonene og nøytronene. Protoner er positivt ladede partikler, og antall protoner er alltid løst for et bestemt element. Med andre ord, antall protoner er det som gir hvert element sin unike, individuelle identitet. For eksempel har et karbonatom seks protoner, men et atom med bare fem protoner er bor, mens et atom med syv protoner er elementet nitrogen.
Nøytroner er nøytrale – de har ingen ladning. Isotoper er atomer av samme element som har et annet antall nøytroner. Selv om isotoper av samme element er tvillinger når det gjelder reaktivitet, betyr det forskjellige antall nøytroner at de har en annen masse. Visse isotoper er mer rikelig i noen materialer enn andre siden noen fysiske og kjemiske prosesser «foretrekker» en isotop over en annen. Disse forskjellene i isotopisk overflod brukes som «etiketter» for å identifisere DE forskjellige kildene TIL CO2 som finnes i en atmosfærisk CO2-prøve. Noaa atmosfæriske forskere bruker disse isotopiske etikettene for å bestemme hvilken prosent av karbonet som ble avledet fra fossile brensler, den terrestriske biosfæren eller fra havet.
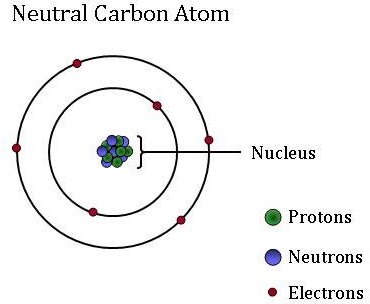
Isotoper Av Karbon
karbonisotoper kommer i tre former. Den desidert vanligste isotopen av karbon er karbon-12 (12c), som inneholder seks nøytroner i tillegg til sine seks protoner. Den neste tyngste karbonisotopen, karbon-13 (13c), har syv nøytroner. BÅDE 12c og 13c kalles stabile isotoper siden de ikke forfall i andre former eller elementer over tid. Den sjeldne karbon-14 (14c) isotopen inneholder åtte nøytroner i kjernen. I motsetning TIL 12c og 13c er denne isotopen ustabil eller radioaktiv. Over tid vil et 14c atom forfalle til et stabilt produkt.

det store flertallet av alt karbon som finnes PÅ Jorden er 12C. Nesten 99% av alt karbon på Jorden er av denne formen. Mens bare ca 1% av alt karbon på Jorden er av 13c isotopform, ER 14C fortsatt mye sjeldnere. Bare en av hver trillion karbonatomer er 14C.
for å få en ide om hvor få 14c-atomer det er sammenlignet MED 12C, la oss sammenligne en til en trillion. En trillion er en million millioner. Hvis du lined opp en trillion en dollarsedler, ville den strekke seg nesten fra Jorden til solen!