- Hoe kan een klein molecuul als ethanol aan de basis liggen van zoveel menselijke ellende?hier stellen we voor om de chemische gevolgen van een avond van feestvreugde tot overmaat tot op de bodem uit te zoeken.
- 2.1 Ethanolmetabolisme
- Ethanol Acet aceetaldehyde
- aceetaldehyde ⇒ azijnzuur
- 2.2 bijkomende metabole veranderingen
- Prof. Klaus Roth
Hoe kan een klein molecuul als ethanol aan de basis liggen van zoveel menselijke ellende?
hier stellen we voor om de chemische gevolgen van een avond van feestvreugde tot overmaat tot op de bodem uit te zoeken.
2.1 Ethanolmetabolisme
Ethanol (CH3CH2OH) wordt in de lever geoxideerd tot aceetaldehyde (ch3cho, ethanal), dat in een tweede stap verder geoxideerd wordt tot azijnzuur (CH3COOH, ethaanzuur) (Fig. 2). Het azijnzuur wordt uiteindelijk afgebroken tot kooldioxide en water in de citroenzuurcyclus .
tijdens het proces levert ethanol een aanzienlijke hoeveelheid energie: 450 kcal/100g, een waarde tussen die van glucose (400 kcal/100g) en vet (930 kcal/100g). Alcoholische dranken moeten daarom onder de levensmiddelen worden ingedeeld.
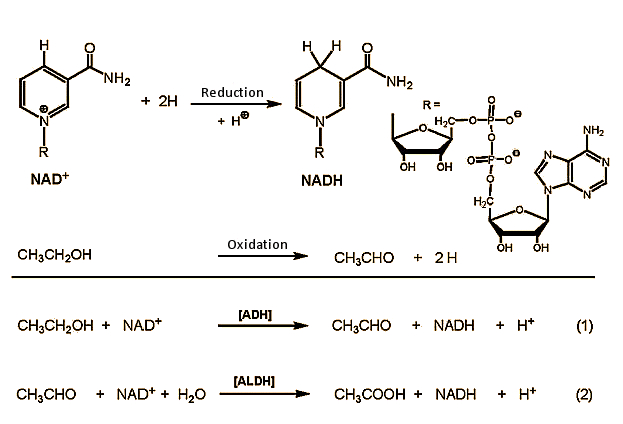
Figuur 2. Ethanolmetabolisme in het lichaam.
Ethanol Acet aceetaldehyde
in de eerste stap wordt ethanol in cellen van de lever geoxideerd tot aceetaldehyde, met NAD+ (nicotinamide adenine dinucleotide) als oxiderende stof. Deze reactie wordt gekatalyseerd door alcoholdehydrogenase (ADH) enzymen , waarvan het menselijk lichaam er vele beschikbaar heeft. Ze zijn allemaal structureel zeer gelijkaardig, en bestaan altijd uit twee subeenheden, die elk 374 aminozuren bevatten. De α-, β – En γ-subeenheden die geschikt zijn voor ethanoloxidatie zijn gecodeerd in drie genen in ons chromosoom 4 en kunnen naar believen worden gecombineerd met een van de zes ADH-dimeren (αα, ββ, γγ, αβ, αγ, βγ). De katalytische activiteiten van de verschillende combinaties verschillen slechts weinig.
daarnaast bestaan er nog diverse variëteiten van de subeenheden β En γ. ADH die β1 subeenheden bevatten-gemeenschappelijk onder Europeanen-oxideert ca. 110 mg ethanol per uur en kg lichaamsgewicht, terwijl de β2-versie, gemeenschappelijker onder Aziaten, aanzienlijk meer katalytisch actief is, bij 130 mg / kg / u.
chronisch misbruik van alcohol induceert een sterke Regulatie in levercellen met een normaal ondergeschikt mechanisme van ethanoloxidatie: het microsomale ethanol oxizing system (meos). In dit geval, wordt een speciale cytochroom P450 monooxygenase samengesteld in een verhoogde mate, die op zijn beurt ethanol onafhankelijk van ADH metaboliseert. In de meos reactie sequentie, ethanol wordt direct geoxideerd door moleculaire zuurstof, dat wil zeggen, Er is geen energetische koppeling aan de respiratoire keten in de mitochondriën. Energie die vrijkomt door meos-oxidatie van ethanol wordt gewoon weggegooid in de vorm van warmte, en — in tegenstelling tot “normale” ADH metabolisme — wordt niet opgeslagen chemisch.
dit is indrukwekkend aangetoond bij mensen: In een gecontroleerde studie werd de normale dagelijkse calorie-inname verdubbeld met een extra hoeveelheid ethanol of chocolade. Het resultaat: met behulp van ethanol bleef het lichaamsgewicht na twee weken onveranderd, maar chocoladeeters verdienden 3 kg .
aceetaldehyde ⇒ azijnzuur
twee aldehydedehydrogenases (ALDS) staan klaar voor verdere oxidatie van ethanol. Snelle oxidatie is ook belangrijk, omdat aceetaldehyde giftig is. De ALDHs vervullen hun taak op voorbeeldige wijze: giftig acetaldehyde wordt geoxideerd aan onschadelijk azijnzuur langs twee wegen: een kleine fractie wordt geoxideerd in levercellen in cytosol door aldehyde dehydrogenase ALDH1, terwijl de belangrijkste fractie in mitochondria door ALDH2 wordt geoxideerd.
bij de oxidatie van zowel alcohol als aceetaldehyde is NAD+ (nicotinamide adenine dinucleotide) het eigenlijke oxiderende middel. De bloedconcentratie van aceetaldehyde blijft over het algemeen onder 2 µmol/L, vergeleken met een typische ethanolconcentratie van 5 mmol / l.
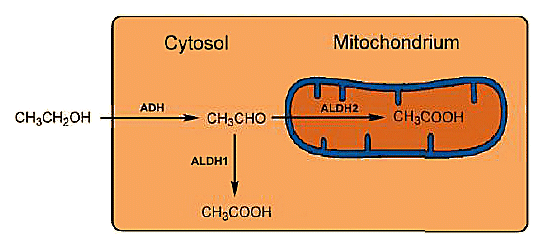
Figuur 3. Intracellulair metabolisme van ethanol.
elke ALDH bestaat uit vier identieke subeenheden, elk met 500 aminozuren, die in het geval van ALDH1 — gevonden in het cytosol — gelokaliseerd is op chromosoom 9, terwijl ALDH2 uit de mitochondriën gelokaliseerd is op chromosoom 12. De sequentie correspondentie tussen de twee ALDS is slechts 68 %, en hun katalytische effecten verschillen dienovereenkomstig: ALDH2 van de mitochondriën is veel actiever dan ALDH1 van de cytosol (Fig. 3).
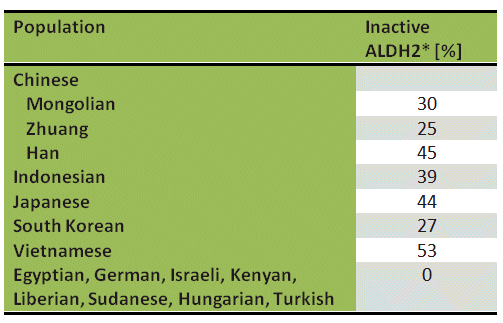
de ongebruikelijke alcoholgevoeligheid van een deel van de wereldbevolking, met name die uit Azië, is het gevolg van een veranderde ALDH2. In tegenstelling tot Europeanen en Afrikanen, 44 % van de Japanners (Tab. 1) hebben een ALDH2 enzym variant in de mitochondriën van hun levercellen. Deze modificatie draagt de benaming ALDH2*, waarbij een glutaminezuur op positie 487 is vervangen door een lysine . De mutatie is katalytisch inactief en mensen met ALDH2* kunnen acetaldehyde slechts langzaam metaboliseren, door de minder actieve ALDH1-route te gebruiken.
het gevolg: binnen enkele minuten na het gebruik van ethanol neemt de concentratie aceetaldehyde in het bloed sterk toe. Terwijl voor een Europeaan (ALDH2) met een alcoholgehalte in het bloed van 0,5 ‰ het aceetaldehydegehalte in het bloed onder 2 µmol/L blijft, kan deze waarde voor een Japanner met ALDH2* 35 µmol/L bereiken .
aceetaldehyde heeft een krachtig vasodilaterend effect, waardoor het gezicht rood wordt, of “flush” (flushing syndrome). Tegelijkertijd treden hevige kater-achtige symptomen op (hoofdpijn, trillen, zich ziek voelen) .
Tabel 1. Prevalentie van inactieve aldehydedehydrogenase (ALDH2*) bij verschillende etnische populaties .
de identieke symptomen worden waargenomen bij Europeanen met actieve ALDH2 als het enzym wordt geblokkeerd. Dit effect kan naar believen worden opgewekt met het farmaceutische preparaat Antabuse®, een verbinding die ALDH2 volledig blokkeert. De resulterende opwaartse schok in de aceetaldehydeconcentratie, met de bijbehorende ernstige kater symptomen, plagen drugsverslaafden in de ontwenningsfase die een behandeling ondergaan, na enige verwennerij aan alcohol.
na het proeven van een gerecht dat toevallig de paddenstoel Coprinus atramentarius bevat, algemeen bekend als de “common ink cap” of “Tippler’ s bane”, moet men, voor de komende drie dagen, strikt alle alcoholische dranken vermijden (Fig. 4). Anders, na slechts een paar minuten, grote kater symptomen ontwikkelen zoals blozen, hartkloppingen en verhoogde pols, hoofdpijn, misselijkheid, braken, zweten aanvallen, en trillen van de ledematen. Vooral ernstige gevallen kunnen zelfs leiden tot instorting . Dit klinische beeld staat bekend als het Coprinus syndroom. Het kan enkele uren aanhouden, maar tot nu toe zijn er geen gevallen van overlijden geregistreerd.
.gif)
Figuur 4. Coprinus syndroom.
de oorzaak van het Coprinus-syndroom is een sterk verhoogde bloed-aceetaldehydeconcentratie als gevolg van een bestanddeel van de paddenstoel dat de oxidatie van aceetaldehyde tot azijnzuur blokkeert. De waargenomen symptomen zijn identiek aan die gezien na alcoholinname tijdens de behandeling met Antabuse (disulfiram) . De boosdoener kan zijn coprin, N5-(1-hydroxycyclopropyl) – L-glutamine (2), dat is geïsoleerd uit deze schimmel . Meer recent is aangetoond dat het niet coprin zelf is dat het aldehyde dehydrogenase ALDH2 blokkeert, waardoor de symptomen worden veroorzaakt, maar eerder een van de metabolieten, waarschijnlijk 1-aminocyclopropanol (3) of het hydraat van cyclopropanon (4) .
2.2 bijkomende metabole veranderingen
Ethanol en de afbraak ervan — de laatste gaat razendsnel door — leiden tot fysiologische veranderingen die lang na de periode van intoxicatie aanhouden. Vanuit chemisch oogpunt is ethanol een calorierijk reductiemiddel, waarvan de verwerking aanzienlijke hoeveelheden van het oxiderende middel NAD+ opslokt en de NAD+/NADH-verhouding verlaagt van 4: 1 tot 2: 1. Dit verminderen van het oxidatiepotentieel van de cel veroorzaakt een massieve en verreikende wijziging in metabolisme, b.v., een vermindering in glucosesynthese, accumulatie van melkzuur, verbeterde productie van lipiden, en verminderde degradatie van vetten en proteã ne.
een verminderde glucosesynthese verlaagt op zijn beurt de bloedsuikerspiegel, met als gevolg een algemene lichamelijke zwakte. In het geval van een diabeticus gewend aan medicatie, kan dit de gevreesde hypoglykemie produceren. Ondertussen kan de ophoping van melkzuur de pH van het bloed verlagen tot onder 7,36 (acidose).
verhoogde vetzuursynthese in combinatie met een verminderd lipidenmetabolisme en eiwitmetabolisme leidt tot vet-en eiwitdepositie in de lever. Dit is een omkeerbaar proces in het geval van occasioneel alcoholmisbruik, maar in een chronische situatie leidt het direct tot “vette lever”, die samen met verdere door alcohol veroorzaakte schade aan het levermetabolisme kan eindigen in cirrose van de lever of carcinoom.
Ethanolverbruik is echter niet alleen onderhevig aan nadelen. De plasmaconcentratie van HDL-cholesterol (“goede cholesterol”) neemt toe en het coagulerende vermogen van het bloed neemt af. Beide bieden bescherming tegen hartaanvallen en beroertes , wat de lagere prevalentie van dodelijke bloedsomloopziekten in bepaalde Mediterrane landen (Mediterraan dieet) kan verklaren. In sommige gevallen wordt er echter rode wijn in zulke grote hoeveelheden geconsumeerd dat, hoewel coronaire aandoeningen en beroertes minder vaak voorkomen, leverziekten — van vette lever tot carcinoom — des te vaker voorkomen.
zoals altijd — vrij aangepast van Paracelsus — vertegenwoordigt matiging waarschijnlijk de gulden middenweg.
-
de chemie van een kater-Alcohol en de gevolgen ervan Onderdeel 1
► Lees meer over de chemie van een kater in deel 3
K. Roth, Chem. Unserer Zeit 2005, 39, 348. DOI: 10.1002 / ciuz.200590067
Details van de structuur en het katalytische mechanisme van ethanoloxidatie met ADH: www.chemie.tu-darmstadt.de/akplenio/moproc/zink/alkoholdehydrogenase / ADH_start.htm
C. S. Lieber, New Engl. J. Med. 1973, 288, 356. DOI: 10.1056 / NEJM197302152880710
Hsu et al., Proc. Natl. Acad. Sci. 1985, 82, 3771. Link
H. W. Goedde, D. P. Argawal, Alcoholism, Pergamon Press, New York 1989.
D. Crabb et al. J. Clin. Investeren. 1989, 83, 314. DOI: 10.1172 / JCI113875
T. L. Wall et al. J. Stud. Alcohol 2000, 61, 13. Link
D. Michelot, Natural Toxins 1992, 1, 73. DOI: 10.1002/nt.2620010203
G. M. Hatfield, J. P. Schaumberg, Lloydia 1975, 38, 489. PMID: 1241098
P. Lindberg et al. Scheikunde. Comm. 1975, 946. DOI: 10.1039 / C39750000946
P. Lindberg et al., J. Chem. Soc. Perkin I 1977, 684. DOI: 10.1039 / P19770000684
J. S. W. Wiseman, R. H. Abeles, Biochemistry 1979, 18, 427. DOI: 10.1021 / bi00570a006
K. Roth, Chem. Unserer Zeit 2004, 38, 426. DOI: 10.1002 / ciuz.200490092
Prof. Klaus Roth
Freie Universität Berlin, Duitsland.
het artikel is in het Duits gepubliceerd.:
- Scheikunde. Unserer Zeit, 2007, 41, 46-55.
DOI: 10.1002/ciuz.200700409
en werd vertaald door W. E. Russey.
andere artikelen van Klaus Roth gepubliceerd door ChemViews magazine:
- in Espresso — a drietraps Preparation
bewijst Klaus Roth dat geen culinair meesterwerk kan worden bereikt zonder een basiskennis van chemie
DOI: 10.1002/chemv.201000003 - in chocolade — het edelste polymorfisme
Klaus Roth bewijst dat alleen chemie in staat is om zo ‘ n hemels genot te produceren
DOI: 10.1002/chemv.201000021 - in mousserende wijn, Champagne & Co
toont Klaus Roth aan dat alleen chemie deze tinteling
kan zijn DOI: 10.1002/chemv.201000047 - in de angst van de chemicus voor de Fugu
toont Klaus Roth aan dat de angst van de chemicus voor de Fugu of kogelvis zich uitstrekt tot de kenmerkende en intrigerende poision die hij draagt
DOI: 10.1002/chemv.201000104