- os Polissilícios
- o íon Ortossilicato, SiO44-
- Procianidinas Polysilicates
- Polissilícios cíclicos Oligoméricos
- Cadeia de Polysilicates
- Polissilícios em folhas
- 3-D Poliméricos Silicatos
- Vidro
- química do solo
- substituição isomórfica
- Primeiro Princípio de subsídio isomórfico
- segundo princípio de substituição isomórfica
os Polissilícios
o íon Ortossilicato, SiO44-
o íon ortossilicato não está presente em uma grande variedade de minerais. É uma base muito forte que não vai persistir em solução aquosa. Na natureza, é encontrada em combinação com catiões ácidas em sais insolúveis.
| |
||
| phenacite | Be2SiO4 |   |
| willemite | Zn2SiO4 |   |
| zircão | ZrSiO4 |   |
| garnet | (M2+)3(M3+)2(SiO4)3 | M2+ = Ca, Mg, Fe M3+ = Al, Cr, Fe |
Procianidinas Polysilicates
Poliméricos silicato de estruturas exigem (2-coordenar a) oxygens. A fim de dar espaço para um oxigênio de ponte, um óxido deve ser removido do Silício” receptor”.
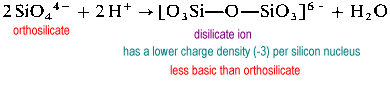
o íon disilicato é incomum na natureza. Apenas pode ser encontrada no mineral raro Thortveitite, Sc2Si2O7. Estruturas maiores como trissilicato e tetrasilicato são extremamente rápidas.
Polissilícios cíclicos Oligoméricos
em vez de formar estruturas de cadeia aberta longa, as extremidades das cadeias irão ligar eliminando íons de óxido.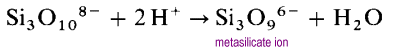
o íon Metasilicato é um oligômero do íon SiO32 desconhecido. Nestas estruturas cada silício possui dois átomos de ligação e dois terminais de oxigênio. Há densidade de carga a -2 por átomo de silício. Os polissilícios cíclicos mais comuns são os trimers cíclicos (SiO3)36-e os hexamers cíclicos (SiO3)612-.

O trímero cíclico é encontrado no mineral benitoite, BaTi(Si3O9.

Cadeia de Polysilicates
Linear (1-D) polímeros da fórmula (SiO3)n2n – pode ser formado através de correspondência oxygens. Nestas estruturas há uma carga de -2 por átomo de silício. Um grupo de minerais chamados de minerais piroxeno têm este tipo de estrutura.
| |
|
| piroxena | MgSiO3 |
| diopsite | CaMgSi2O6 |
| spodimene | LiAlSi2O6 |
| pollucite | CsAlSi2O6 |
cadeias Lineares podem ser ligados lado a lado, se um óxido de íon é substituída por outra ponte átomo de oxigênio. Se esta ligação ocorrer em grupos SiO3 alternativos em cada cadeia, uma estrutura de cadeia dupla (Si4O11)N6N-resulta. Em tais estruturas há uma redução na carga e número de átomos de oxigênio por átomo de silício.
Crocidolite, um mineral de amianto da fórmula Na2Fe5(OH)22, é um exemplo. Este mineral é de natureza fibrosa e tem propriedades resistentes ao fogo e ao calor que derivam da estrutura de cadeia longa do ânion.
Polissilícios em folhas
quando a ligação das cadeias lado-a-lado é continuada indefinidamente, mais óxidos são eliminados e um polímero 2-D. Estes polímeros 2-D são chamados silicatos de folha e contêm o anião n4n. Os minerais que contêm esta estrutura são facilmente clivados em folhas finas.
| |
|
| micas | moscovita e biotita |
| minerais de argila | montmorilonite, caulinita, de caulim e vermiculita |
| talco |   |
| pedra-sabão |   |
| o amianto crisotila |   |
3-D Poliméricos Silicatos
Folhas são vinculados em um 3-D polímero, quando tudo o óxido de íons são eliminados (todos os os oxigénios na estrutura são pontes). Esta estrutura contém sílica de óxido não-carregada n, que já não é básica, mas sim um óxido ácido. Muitos minerais comuns contêm esta estrutura: quartzo, sílex, jasper, onyx, ametista, Citrina, Agato e calcedônia.Passos de polimerização sucessivos:
- resultam numa redução sucessiva da razão átomo de O / Si
- 4:1 em ortossilicato
- 2:1 em sílica

 Coloque o seguinte minerais, em ordem crescente de grau de polimerização. A fim de fazer isso, calcular a razão o/Si (quanto menor a razão, mais polimerizada a estrutura.
Coloque o seguinte minerais, em ordem crescente de grau de polimerização. A fim de fazer isso, calcular a razão o/Si (quanto menor a razão, mais polimerizada a estrutura.
- magnetita, Al2Si4O10(OH)2
- grunerite, Fe7Si8O22(OH)2
- spessartite, Mn3Al2Si3O12
- bustamite, CaMn(SiO3)2
Vidro
Quando ácida de sílica é reagido com óxidos básicos em temperaturas muito elevadas (~1700 0) e em seguida é resfriado muito rapidamente para o polysilicate íons para permitir que o fomation da ordenada polysilicate íons encontrados em minerais para formar. O resultado é a formação de um sólido amorfo ou vidro. Os óculos são caracterizados por não ter um ponto de congelação definido.
o vidro simples é produzido por fusão (fusão) de areia com bicarbonato de sódio e calcário (fontes dos óxidos básicos Na2O e CaO). Durante este processo, pontes silício-oxigênio são quebradas.
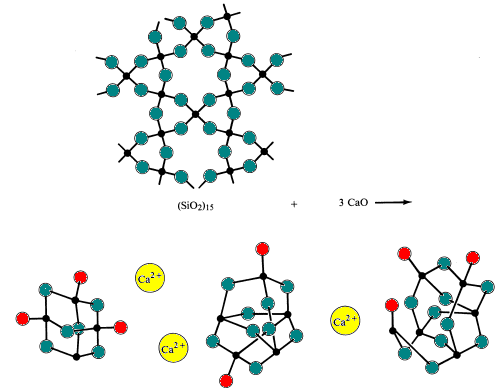
óculos especiais são feitos alterando a composição de óxidos ácidos e básicos no vidro.O vidro Pyrex ™ é invulgarmente resistente ao choque térmico. Para torná-lo 10-25% B2O3, um óxido ácido, é incorporado na estrutura.
Saiba mais sobre óculos aqui e em Corning Museu do Vidro de Recursos do site.
química do solo
o facto de os íons polissilícios cada vez mais polimerizados terem cargas decrescentes por silício, o que resulta numa diminuição da basicidade, tem consequências importantes na química do solo.
quanto mais básico for o ânion polissilicato de um mineral, mais prontamente reagirá com ácidos fracos e passará por intempéries.
a água da chuva é algo ácida devido ao CO2 dissolvido, mesmo na ausência de enxofre e óxidos de azoto. Ao longo do tempo, a água da chuva irá reagir com os ânions de silicato menos polimerizados para substituir iões de óxido por oxigénio em Ponte, produzindo um silicato mais altamente polimerizado. Os óxidos são removidos como moléculas de água.
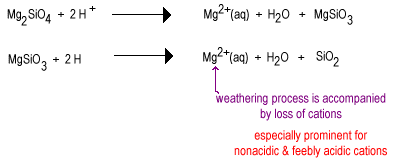
o estágio intermediário de meteorização tem grandes quantidades de silicatos de camada, tais como argila, bem como algum quartzo. Estes solos tendem a ser encontrados em regiões temperadas sob uma cobertura de grama ou árvores. Esses solos são menos férteis do que os solos desérricos recentemente irrigados devido à perda do nutriente vegetal não-ácido K+. Silicatos de camada presentes em solos intermediários ainda podem conter catiões em suas superfícies carregadas negativamente, que podem ser liberados como a planta precisa deles. Estes solos são encontrados nos cinturões ainda bastante férteis de milho e trigo.
substituição isomórfica
os íons Polissilícios têm cargas negativas que devem ser contrabalançadas por catiões apropriados. Os oxigenos terminais possuem superfícies carregadas negativamente que se aproximam de superfícies fechadas de carga negativa. Os catiões que são necessários para neutralizar a carga negativa do polissilício estão localizados nas camadas entre as cadeias ou camadas ou nos buracos tetraédricos ou octaédricos presentes na estrutura 3-D.
Os tipos de catiões encontrado em uma forma particular de polysilicate vai depender de”
- o tamanho dos catiões
- o custo dos catiões
Desde muito poucos conjuntos de íons existem que têm a mesma carga e muito semelhante raios, há pouca razão para que um desses correspondentes tipos de íons para ser o preferido em cima do outro quando um mineral é formado no resfriamento de magma derretido.
Por exemplo, olivina, que tem uma composição ideal de Mg2SiO4, podem conter diferentes porcentagens de isomorphous subtitution de Fe2+ (raio 92 pm) no lugar de um número igual de Mg2+ íons (raio 86 pm).
Primeiro Princípio de subsídio isomórfico
segundo princípio de substituição isomórfica
substituição isomórfica aumenta o número de possíveis substituições em silicatos.
Exemplos
- K+pode ser substituído por um raro Rb+ Tl+ íons bem comum, Ba2+
- Ca2+pode ser substituído por Sr2+(132 horas), Na+(116 horas), Y3+(104 horas), La3+ (117 pm), e o sexto período de f-bloco de íons (100-117 pm)
- Si4+ pode ser substituído pelo comum Al3+ ion (67 pm)
catiões na maioria dos minerais de silicato são amplamente substituído o que torna não-econômica de minérios para a maioria dos elementos. Há relações diagonais de elementos (especialmente no segundo período) para os elementos um grupo à direita e um período Abaixo na tabela.
 quais dos seguintes minerais poderiam surgir por processos de substituição isomorfos em leucite, K (AlSi2O6)?
quais dos seguintes minerais poderiam surgir por processos de substituição isomorfos em leucite, K (AlSi2O6)?
- K(YSi2O6)
- Rb(AlSi2O6)
- Ba(BeSi2O6)
- Ba(AlSi2O6)
DICA: Existem dois princípios fundamentais de compostos iónicos que deve ser observado no isomorphous substituição:
- A carga total de todos os cátions deve ser igual a carga total de todos os ânions.
- para que a substituição seja isomórfica, o número total de catiões que entram deve ser aproximadamente igual à carga total de todas as catiões que estão sendo substituídas.