米国Pharm. 2014;39(4):HS2-HS7.
要約:脳の心室における脳脊髄液(CSF)の蓄積である水頭症の管理には、長期的な影響を防ぐためのシャント移植が含まれることが多い。 シャントは、頭蓋内圧を維持し、CSFのさらなる蓄積を防止するように設計された排水装置であるが、病原体を中枢神経系に導入することができる。 これは、発作、シャント障害、髄膜炎、敗血症、脳炎などの感染症および後遺症につながる可能性があります。 感染症は、無菌技術、化学予防、および/または抗生物質溶出シャントを使用することによって予防することができる。 シャント感染の治療には、感染したハードウェアの除去、排水装置の配置、およびIVまたは脳室内抗生物質の使用が含まれ得る。
水頭症は、脳室またはくも膜下腔に脳脊髄液(CSF)が蓄積し、脳室内圧の上昇および心室拡張をもたらすことを特徴とする疾患である。 水頭症の一般的な病因は、CSFドレナージの障害である。1,2米国およびヨーロッパにおける水頭症の発生は、0.5から0.8あたり1,000出生と推定されており、多くの場合、二分脊椎、頭蓋内出血、または先天性病因に続1,3水頭症の他の潜在的な原因には、骨髄異形成、腫瘍、髄膜炎、後窩嚢胞、Dandy-Walker奇形、または水道管狭窄が含まれる。4
機械的シャントは水頭症の主な治療法です。 水頭症関連のシャント配置は、小児で行われる最も一般的な神経外科的処置であるが、最も高い故障率も有する。5 40,000以上のシャント配置は、2.7%の推定入院死亡率で、米国では毎年行われています。5,6一般的な皮膚細菌叢および他の病原体の導入は、周術期および術後の両方で、シャント感染につながり、シャント障害を引き起こす可能性がある。
シャント感染率は、成人患者では1.6~16.7%、小児患者では最大20%と推定されています。2,7小児集団におけるこの増加した発生は、免疫力の欠如(特に<1歳)、未熟児(<35週の妊娠期間)、潜在的な病原体への曝露、付随する罹患率、および他の生理学3,4小児患者は成人よりも早くシャント感染を発症する傾向があり、ほとんどの感染症は配置後最初の30-60日以内に発生します。1
<5歳の患者と50歳から59歳の成人は、シャント感染の発生率が最も高いようです。1シャント感染の危険因子には、若年、術後CSF漏れ、脳室内出血、複数のシャント、過去90日間のシャント改訂手術、髄膜炎直後のシャント、長期入院(>1ヶ月)、および以前のシャント感染が含まれる。シャント感染に関連する2,4,7,8合併症には、シャント機能不全、短期または長期の認知障害、敗血症、髄膜炎、および長期入院が含まれる。1,4,8
シャントタイプ
シャントの最も一般的なタイプを表1にまとめました。 この記事では、最も利用されている2つのシャントに焦点を当てます:脳室腹膜(VP)と脳室心房(VA)シャント。 VPシャントは、二つのより一般的な、VAシャントは、心臓の心房にCSFをシフトするのに対し、腹膜にCSFを転換することによって動作します。2,9,10

シャント感染の病因
シャント汚染は、シャントの近位端が正常な皮膚細菌叢と接触するときにしばしば引き起こされる。 これは外科注入の間に傷の伝染がpostoperativelyまたはperioperatively原因で起こることができます。コアグラーゼ陰性の表皮ブドウ球菌および黄色ブドウ球菌などの11グラム陽性細菌は、それぞれシャント感染の45%から60%1-3、12および20%から33%2,3(80%4までの報告がある)に関与している。 これらの病原体は早い分路の伝染と密接に関連付けられます(分路の外科の4週以内に起こる)。2
後期シャント感染症はシャント手術の数ヶ月後に発生する可能性があり、シャント関連感染症の約15%を占めています。3多くの場合、これらの後期感染症は、患者が腸穿孔または腹膜炎(主にVPシャントに見られる)を経験している場合、StreptococcusまたはEnterococcus種のようなグラム陽性細菌、ま2シャント感染に関連する最も一般的な病原体は、表2.1-4,11感染にまとめられており、シャント関連の合併症および障害の可能性が高くなります。

シャント感染の予防
シャント感染を予防するために用いられる方法には、滅菌技術、全身抗生物質、および抗生物質含浸カテーテルの使用が含まれる。 無菌外科技術は分路の伝染の危険を減らすのを助けるために示されていました。 クロルヘキシジンシャンプーによる患者の毛髪の術前洗浄、手術チームのすべてのメンバーによるダブルグロービング、抗生物質含浸シャント(AIS)の使用を含む標準化された外科プロトコルは、8.8%から5.7%への感染減少率を示した。13
処置中およびシャント配置後の最初の24時間に、全身性の予防的抗生物質を利用することができる。 メタアナリシスによると、全身性、予防的抗生物質および抗生物質含浸カテーテルの使用は、シャント感染の割合を減少させた。9この同じ研究では、シャント感染の減少のために全身性の予防的抗生物質とプラセボの使用を比較し、抗生物質がシャント感染の率を低下させるこ9シャント配置のための最も適切な予防的抗生物質は、過去には十分に定義されていなかったが、ほとんどの臨床医は、外科的予防のためにIVセファゾ2,14最近のガイドラインは、アレルギー性患者のための代替としてクリンダマイシンとバンコマイシンと、神経外科流体シャント手順のためのセファゾリンを推奨しています。15
AISカテーテルは、2002年に導入されて以来、シャント感染を予防するために一般的に使用されてきました.16ほとんどの装置にはリファンピシンとクリンダマイシンの組み合わせが含浸されています。4,16,17彼らはカテーテルの表面に付着する糖蛋白質のbiofilmを作り出すグラム陽性の細菌の植民地化を目標とするように設計されている。16あるメタアナリシスでは、抗生物質含浸カテーテルと標準カテーテルの使用を検討し、抗生物質含浸カテーテルの使用がシャント感染率の低下(OR、0.21)と関連していることが分かった。 このメタアナリシスでは,全身性抗生物質予防と抗生物質含浸カテーテルの両方の使用がシャント感染の減少に有益であると結論した。9
3年の期間にシャント挿入を受けた小児患者を対象に、遡及的試験も実施した。 最初の18か月の間、患者はnonantibiotic浸透させたカテーテルを受け取りました;次の18か月の間、分路の配置を必要とする新しい患者は抗生物質浸透させたカテー すべての子供は分路の配置の後の6か月間続いた。 非抗生物質含浸カテーテルを有する子供は12%の感染率を有していたが、抗生物質含浸カテーテルを有する子供の1.4%のみで感染が見られた。18 15件の試験のより最近のレビューでは、抗生物質コーティングされたカテーテルは、特に以前の分析とは異なる長期カテーテルを有する患者において、臨床感染率を低下させると結論づけられた。19
予防とAISカテーテルの使用によるシャント感染の予防は、患者ケアのコストを削減することが示されています。20シャント感染を治療するためのコストは、患者あたり$17,300からpatient48,454の範囲であり、米国の推定年間病院コスト2 2億につながると推定されています。16,17各AISカテーテルは平均$400の費用がかかりますが、感染および/または再感染を予防することによって節約される金額は、大幅な長期的な節約を提供16これらの節約は、感染の可能性が2.4倍減少し、感染の結果として病院での時間が短縮されたことによるものです。 これらの節約は、シャントされた患者100人あたり440,000ドル以上に達すると報告されています。17
シャント感染症の診断
一般的なシャント感染症の症状には、頭痛、吐き気、嘔吐、手術部位の炎症、神経学的異常、発熱、発作が含まれます。シャント感染症の2,3患者特異的な臨床症状は、移植されたシャントのタイプに依存する。 VPシャントは腹膜炎、食欲不振、過敏症、および腹痛に関連することがあり、VAシャントは敗血症および心内膜炎に関連することがある8。2,3精神状態の変化、シャントサイト周囲の紅斑、シャントトラックに沿った流体、化膿性排出、乳頭浮腫、膨らんだfontanel、nuchal剛性、または明らかなCSF漏れなどの臨床症状が見られた場合、患者はCSF分析、血液培養、および脳イメージングで評価されるべきである。8
感染を予測するCSF分析には、白血球数の増加、タンパク質濃度の増加、およびグルコースレベルの低下が含まれます。 血液培養は、VPシャント感染とは対照的に、VAシャント感染のより有用な指標である。脳画像は、脳室炎またはCSF閉塞の証拠を同定するために使用することができる。 また腹部イメージ投射がVPの分路の機能不全を識別するのに使用されるかもしれません。
治療選択肢
現在、シャント感染の治療に関する実践ガイドラインはありませんが、感染したハードウェアの除去、外部心室ドレインの配置、培養、IVまたは脳室内抗ビオティクスによる治療はすべて効果的な管理プロセスの一部であることが示されています。2
シャントの存在下での中枢神経系(CNS)感染の経験的治療に関する現在の推奨事項は、CEFEPIME、ceftazidime、cefotaxime、meropenemなどの十分なグラム陰性被覆を有する薬剤と組み合わせてIVバンコマイシンを使用することを推奨している。 細菌のbiofilmに対する抗生物質の活動と同様、csfを突き通す薬物の機能はまた抗生の選択のために考慮して重要です。このような薬剤は、病原体が同定され、決定的な治療が決定されるまで投与されるべきである。22,23VPの分路では、分路の遠位先端は腹膜キャビティの内にあり、グラム陰性の細菌により敏感です;gentamicinは共同作用のために加えられるかもしれません。シャント感染に対する2つの経験的抗菌療法および投薬推奨事項を表に要約する。3.2,18,22,23
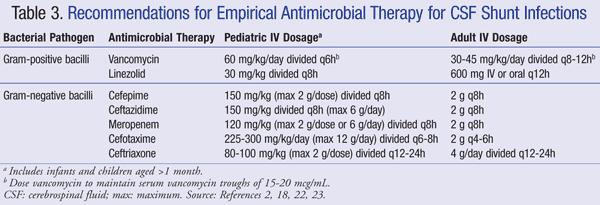
バンコマイシン療法に抵抗しない患者のために、linezolid10mg/kgは小児科の患者の単独療法として有効であるために8時間毎に示されていました。21adjunctive療法としてrifampinの付加はまたCNSへの浸透が原因で考慮されるかもしれません。24抗生物質療法の長さは、使用される外科的アプローチ、シャントのタイプ、および関与する病原体に大きく依存し、ある研究では、4-47日の治療期間の範囲を報告している。25,26より具体的には、7-10日は、グラム陰性感染症のために推奨されるより長いコース(10-14日)で、治療期間のために提案されています23。2
複雑なシャント感染症または治療抵抗性シャント感染症の場合、臨床医はCNS内でより高い殺菌濃度を達成する能力のために、抗生物質の髄腔内ま23バンコマイシンおよびゲンタマイシンはこの状態で一般に使用されます;但し、使用の限定的な推薦がありません。22,23
真菌シャント感染
真菌シャント感染はまれであると考えられており、1件の研究で発生率は0.01%と報告されています。27真菌シャント感染の原因となる最も一般的な病原体はカンジダ種(c albicans、c parapsilosis、およびc tropicalisを含む)であり、真菌症例の75%を引き起こす。 他の生物には、ヒストプラズマ症種、クリプトコッカスネオフォルマンス種、アスペルギルス種が含まれる。 菌類の分路の伝染のための第一次処置は少なくとも12週間liposomal amphotericin B3から5つのmg/kg/dayです。27アンホテリシンBの不寛容な患者のために、5-フルシトシンは代わりであるかもしれません。28これは頻繁にimmunocompetent患者の1年までfluconazole600から800mg/dayまたはitraconazole200mgとの処置およびimmunocompromised患者の可能性としては生涯療法が毎日二から三回続きます。27
結論
シャント感染は水頭症治療に関連する危険因子である。 伝染の防止はかなり伝染の率を減らし、comorbid sequelaeの危険を減らすために適切な無菌技術と結合されるAISのカテーテルの経験的な抗生物質そして使用と示 しかし、バンコマイシンや第三世代セファロスポリンなどのグラム陽性およびグラム陰性の両方のカバレッジを含むIV経験的療法が推奨される。 脳室内抗生物質はまた、最大の殺菌性CNS濃度のために必要とされ得る。
1. Langley JM,Gravel D,Moore D,et al. カナダの院内感染サーベイランスによる、配置後の最初の年における脳脊髄液シャント関連感染の研究。 感染制御病院疫学。 2009;30:285-288.
2. ウェルズDL、アレンJM。 大人の患者の脳室腹膜の分路の伝染。 AACN Adv Critケア. 2013;24:6-12.
3. Lee JK,Seok JY,Lee JH,et al. 小児における脳室腹膜シャント感染の発生率と危険因子:333年の6連続シャントの研究。 J韓国Med Sci. 2012;27:1563-1568.
4. Parker SL,Attenello FJ,Sciubba DM,et al. 抗生物質含浸対標準シャントを受けているハイリスクサブグループにおけるシャント感染発生率の比較。 チャイルズ-ネルフ-シスト 2009;25:77-83.
5. 水頭症の治療。 水頭症協会。 6. Patwardhan RV、Nanda A.米国の植え付けられた心室の分路:水頭症の処置の十億ドル年の費用。 脳神経外科… 2005;56:139-144.
7. Dallacasa P,Dappozzo A,Galassi E,et al. 乳児の脳脊髄液シャント感染症。 チャイルズ-ネルフ-シスト 1995;11:643-648.
8. Rogers EA,Kimia A,Madsen JR,et al. 小児科の救急部に示す子供間の心室の分路の伝染の予測子。 小児科-内科-小児科-外科-整形外科-皮膚科-泌尿器科 2012;28:405-409.
9. Ratilal BO、Costa J、Sampaio C.頭蓋内心室シャントの外科的導入のための抗生物質予防。 Cochrane Database Syst Rev.2006;(3):CD005365.
10. 分路システム。 水頭症協会。 www.hydroassoc.org/hydrocephalus-education-and-support/learning-about-hydrocephalus/shunts.アクセスFebruary12,2014.
11. 前方KR、より少ないHD、Stiver HG。 脳脊髄液シャント感染。 32人の患者における35の感染症のレビュー。 J脳神経外科. 1983;59:389-394.
12. Lan CC,Wong TT,Chen SJ,et al. 水頭症の小児における脳室腹膜シャント感染症および機能不全の早期診断。 J微生物免疫感染症。 2003;36:47-50.
13. Kestle JR,Riva-Cambrin J,Wellons JC,et al. 脳脊髄液シャント感染を低減するための標準化されたプロトコル:水頭症臨床研究ネットワーク品質改善イニシアチブ。 J脳神経外科小児科 2011;8:22-29.
14. Shah SS,Sinkowitz-Cochran RL,Keyserling HL,et al. 小児科の神経外科の患者のバンコマイシンの使用。 アム-ジェイ-コントロール(Am Joy Control 1999;27:482-487.
15. Bratzler DW,Dellinger EP,Olsen KM,et al. 外科の抗菌予防のための臨床練習の指針。 Am J Health-Syst Pharm. 2013;70:195-283.
16. Parker SL,Anderson WN,Lilienfeld S,et al. 抗生物質含浸対標準シャントを受けている患者における脳脊髄シャント感染。 J脳神経外科小児科 2011;8:259-265.
17. Attenello F,Garces-Ambrossi G,Zaidi H,et al. 標準的な分路のカテーテル対抗生浸透させた分路のカテーテルを受け取っている患者の分路の伝染と関連付けられる病院の費用。 脳神経外科… 2010;66:284-289.
18. Sciubba DM,Stuart RM,McGirt MJ,et al. 水頭症の治療におけるシャント感染の発生率を減少させる抗生物質含浸シャントカテーテルの効果。 J脳神経外科. 2005;103(suppl):131-136.
19. Babu MA,Patel R,Marsh WR,et al. 心室カテーテル感染のリスクを減少させるための戦略:エビデンスのレビュー。 ニューロクリットケア… 2012;16:194-202.
20. Bratzler DW,Dellinger EP,Olsen KM,et al. 外科の抗菌予防のための臨床練習の指針。 サギ科(カラマツ科)に分類される。 2013;14:73-156.
21. Yilmaz A,Dalgic N,Musluman M,et al. 子供の分路関連の脳脊髄液の伝染のLinezolidの処置。 J脳神経外科小児科 2010;5:443-448.
22. Tunkel AR,Hartman BJ,Kaplan SL,et al. 細菌性髄膜炎の管理のためのガイドラインを練習します。 クリニークDis. 2004;39:1267-1284.
23. Van de Beek D,Drake JM,Tunkel AR. 院内細菌性髄膜炎。 N Engl J Med. 2010;362:146-154.
24. Hedberg A,Hardemark HG,Olsson-Liljequist B,et al. 表皮ブドウ球菌によって引き起こされる低悪性度の炎症性髄膜炎における脳脊髄液へのフシジン酸およびリファンピシンの浸透。 クリン-ミクロビオール感染症… 2004;10:765-768.
25. 手術のための抗菌予防。 治療ガイドラインMed Lett. 2004;2:27-32.
26. サイモンTD,ホールM,ディーンJM,et al. 最初の脳脊髄液シャント感染後の再感染。 J脳神経外科小児科 2010;6:277-285.
27. Veeravagu A,Ludwig C,Camara-Quintana JQ,et al. 脳室腹膜シャントの真菌感染症:ヒストプラズマ症の診断と治療。 世界の脳神経外科医。 2013;80:222.e5-e13
28. Chiou CC,Wong TT,Lin HH,et al. 小児における脳室腹膜シャントの真菌感染。 クリニークDis. 1994;19:1049-1053.