US Pharm. 2014; 39(4): HS2-HS7.
absztrakt: a hydrocephalus kezelése, a cerebrospinális folyadék (CSF) felhalmozódása az agy kamráiban gyakran magában foglalja a sönt beültetését a hosszú távú hatások megelőzése érdekében. A söntök olyan vízelvezető eszközök, amelyek célja a koponyaűri nyomás fenntartása és a CSF további felhalmozódásának megakadályozása, de kórokozókat juttathatnak a központi idegrendszerbe. Ez fertőzésekhez és következményekhez vezethet, mint pl. görcsrohamok, sönt-elégtelenség, meningitis, sepsis és encephalitis. A fertőzések megelőzhetők aszeptikus technikák, kemoprofilaxis és/vagy antibiotikum-eluáló söntök alkalmazásával. A sönt fertőzés kezelése magában foglalhatja a fertőzött hardver eltávolítását, vízelvezető eszköz elhelyezését, valamint IV vagy intraventrikuláris antibiotikumok alkalmazását.
a Hydrocephalus olyan állapot, amelyet a cerebrospinális folyadék (CSF) felhalmozódása jellemez a kamrákban vagy az agy szubarachnoid térében, ami fokozott intraventrikuláris nyomáshoz és kamrai dilatációhoz vezet. A hydrocephalus gyakori etiológiája a CSF vízelvezetésének károsodása.1,2 a hydrocephalus előfordulását az Egyesült Államokban és Európában 0,5-0,8 / 1000 születésre becsülik, és gyakran másodlagos a spina bifida, az intracranialis vérzés vagy a veleszületett etiológia miatt.1,3 a hydrocephalus egyéb lehetséges okai közé tartozik a myelodysplasia, daganatok, agyhártyagyulladás, hátsó fossa ciszta, Dandy-Walker rendellenesség vagy aqueductalis stenosis.4
a hidrocefalusz elsődleges kezelése a mechanikus tolatás. A hidrocefaluszhoz kapcsolódó sönt elhelyezések a leggyakoribb idegsebészeti eljárások, amelyeket gyermekeknél végeznek, de a legmagasabb a kudarc aránya is.5 Több mint 40 000 sönt elhelyezést végeznek évente az Egyesült Államokban, becsült fekvőbeteg-halálozási arány 2,7%.5,6 a közös bőrflóra és más kórokozók bevezetése, mind perioperatív, mind posztoperatív módon, sönt fertőzésekhez és sönt-kudarchoz vezethet.
a sönt-fertőzések arányát felnőtt betegeknél 1,6-16,7% – ra, gyermekgyógyászati betegeknél pedig 20% – ra becsülik.2,7 a gyermekpopulációban ezt a megnövekedett előfordulást az immunitás hiányának (különösen <1 éves kor), a koraszülöttségnek (<35 hetes gesztációs kor), a potenciális patogéneknek való kitettségnek, az egyidejű morbiditásoknak és más fiziológiai tényezőknek tulajdonítják.3,4 gyermekgyógyászati betegnél hamarabb kialakul a sönt-fertőzés, mint felnőtteknél, a legtöbb fertőzés az elhelyezést követő első 30-60 napon belül jelentkezik.1
a sönt-fertőzések előfordulási gyakorisága a <5 éves betegeknél és az 50-59 éves felnőtteknél fordul elő a leggyakrabban.1 a sönt-fertőzés kockázati tényezői lehetnek fiatalabb életkor, posztoperatív CSF szivárgás, intraventrikuláris vérzés, többszörös sönt, sönt-revíziós műtét az elmúlt 90 napban, közvetlenül agyhártyagyulladás után elhelyezett sönt, hosszan tartó kórházi tartózkodás (>1 hónap) és korábbi sönt-fertőzés.2,4,7,8 a sönt fertőzésekkel kapcsolatos szövődmények közé tartoznak a sönt működési zavarai, rövid vagy hosszú távú kognitív károsodás, szepszis, agyhártyagyulladásés meghosszabbított kórházi tartózkodás.1,4,8
sönt típusok
a söntök leggyakoribb típusait az 1.táblázat foglalja össze. Ez a cikk a két leggyakrabban használt shuntra összpontosít: ventriculoperitonealis (VP) és ventriculoatrialis (VA) shuntokra. A VP shunts, a kettő közül a gyakoribb, úgy működik, hogy a CSF-t a hashártyára tereli, míg a VA shunts a CSF-et a szív pitvarába tolja.2,9,10

a sönt-fertőzések patogenezise
a sönt-szennyeződést gyakran akkor okozzák, amikor a sönt proximális vége érintkezik a normál bőrflórával. Ez műtét után fordulhat elő sebfertőzés vagy perioperatív módon a műtéti beültetés során.11 Gram-pozitív baktériumok, mint például a koaguláz-negatív Staphylococcus epidermidis és a Staphylococcus aureus felelősek a shunt fertőzések 45-60% 1-3,12 és 20-33% 2,3 (egy jelentés akár 80% 4). Ezek a kórokozók szorosan kapcsolódnak a korai sönt fertőzésekhez (amelyek a sönt műtétet követő 4 héten belül jelentkeznek).2
késői sönt fertőzések néhány hónappal a sönt műtét után is előfordulhatnak, és a sönt okozta fertőzések körülbelül 15%-áért felelősek.3 sok esetben ezeket a késői fertőzéseket gram-pozitív baktériumok, például Streptococcus vagy Enterococcus fajok, vagy gram-negatív baktériumok, leggyakrabban Pseudomonas aeruginosa okozhatják, ha a beteg bélperforációt vagy peritonitist tapasztalt (elsősorban a VP shunts).2 a sönt fertőzésekkel kapcsolatos leggyakoribb kórokozókat a 2.1-4,11. táblázat foglalja össze a fertőzések növelik a sönt okozta szövődmények és kudarcok valószínűségét.

a sönt-fertőzések megelőzése
a sönt-fertőzés megelőzésére alkalmazott módszerek közé tartozik a steril technika, a szisztémás antibiotikumok és az antibiotikumokkal impregnált katéterek alkalmazása. Kimutatták, hogy az aszeptikus műtéti technika segít csökkenteni a sönt fertőzések kockázatát. Szabványosított műtéti protokoll, beleértve a beteg hajának preoperatív mosását klórhexidin samponnal, dupla kesztyű a műtéti csoport minden tagja, valamint az antibiotikumokkal impregnált söntök (AIS) használata, amelyet négy Gyermekkórház hajtott végre, 8,8%-ról 5,7% – ra csökkentette a fertőzés mértékét.13
szisztémás profilaktikus antibiotikumok alkalmazhatók az eljárás során és a sönt elhelyezését követő első 24 órában. Egy metaanalízis szerint a szisztémás, profilaktikus antibiotikumok és az antibiotikumokkal impregnált katéterek használata csökkentette a sönt fertőzések arányát.9 ugyanez a vizsgálat összehasonlította a szisztémás, profilaktikus antibiotikumok alkalmazását a placebóval a shunt-fertőzés csökkentése érdekében, és megállapította , hogy az antibiotikumok csökkentették a shunt-fertőzések arányát (esélyhányados, 0,52).9 míg a legmegfelelőbb profilaktikus antibiotikum a sönt elhelyezéséhez a múltban nem volt jól meghatározva, a legtöbb klinikus IV cefazolint vagy vankomicint használ a műtéti profilaxishoz.2,14 a legújabb irányelvek a cefazolint javasolják idegsebészeti folyadék-tolatási eljárásokhoz, a klindamicint és a vankomicint alternatívaként az allergiás betegek számára.15
az AIS katétereket 2002-es bevezetésük óta gyakran használják a sönt-fertőzések megelőzésére. 16 a legtöbb eszközt rifampicin és klindamicin kombinációjával impregnálják.4,16,17 úgy tervezték, hogy megcélozzák a Gram-pozitív baktériumok kolonizációját, amelyek glikoprotein biofilmet termelnek, amely tapad a katéter felületéhez.16 az egyik metaanalízis az antibiotikummal impregnált katéterek használatát vizsgálta a standard katéterekkel szemben, és megállapította, hogy az antibiotikummal impregnált katéterek használata a shunt-fertőzés csökkent arányával jár (OR, 0,21). Ebben a metaanalízisben arra a következtetésre jutottak, hogy mind a szisztémás antibiotikum profilaxis, mind az antibiotikummal impregnált katéterek használata előnyös lehet a shunt fertőzések csökkentésében.9
retrospektív vizsgálatot végeztek olyan gyermekgyógyászati betegeknél is, akik 3 éves időkeret alatt sönt behelyezésen estek át. Az első 18 hónapban a betegek nemantibiotikummal impregnált katétereket kaptak; a következő 18 hónapban minden új beteg, aki sönt elhelyezést igényel, antibiotikummal impregnált katétereket kapott. Minden gyermeket 6 hónapig követtek a sönt elhelyezése után. A nem antibiotikusan impregnált katéterekkel rendelkező gyermekek fertőzési aránya 12% volt, míg az antibiotikummal impregnált katéterekkel rendelkező gyermekek csak 1,4%-ánál észleltek fertőzést.18 a 15 vizsgálat újabb áttekintése azt is megállapította, hogy az antibiotikumokkal bevont katéterek csökkentik a klinikai fertőzés arányát, különösen azoknál a betegeknél, akiknek hosszú távú katéterük van, ami eltér néhány korábbi elemzéstől.19
a shunt fertőzések megelőzése profilaxissal és AIS katéterek használatával bizonyítottan csökkenti a betegellátás költségeit.20 becslések szerint a sönt-fertőzés kezelésének költsége betegenként 17 300 és 48 454 dollár között mozoghat, ami az Egyesült Államokban a becsült éves kórházi költség 2 milliárd dollár.16,17 bár minden AIS katéter átlagosan 400 dollárba kerül, a fertőzés és/vagy újrafertőzés megelőzésével megtakarított pénzmennyiség jelentős hosszú távú megtakarítást eredményezhet.16 ezek a megtakarítások a fertőzés valószínűségének 2,4-szeres csökkenéséből és a fertőzés következtében a kórházban töltött idő csökkenéséből adódnak. Azt jelentették, hogy ezek a megtakarítások összege több mint $440,000 per 100 betegek shunted.17
sönt-fertőzések diagnosztizálása
az Általános sönt-fertőzés tünetei közé tartozik a fejfájás, hányinger, hányás, a műtéti terület gyulladása, neurológiai rendellenesség, láz és roham.2,3 a sönt-fertőzések betegspecifikus klinikai megnyilvánulása a beültetett sönt típusától függ. A VP shunts peritonitis, anorexia, ingerlékenység és hasi fájdalom, 8,míg a VA shunts szepszishez és endocarditishez társulhat.2,3 ha olyan klinikai tüneteket észlelnek, mint a megváltozott elmeállapot, a sönt helyét körülvevő erythema, folyadék a sönt nyomvonal mentén, gennyes váladékozás, papilledema, kidudorodó fontanel, nyakmerevség vagy nyilvánvaló CSF szivárgás, a beteget CSF analízissel, vértenyészetekkel és agyi képalkotó eljárással kell értékelni.8
a fertőzésre prediktív CSF analízis magában foglalja a megnövekedett fehérvérsejtszámot, a megnövekedett fehérjekoncentrációt és a csökkent glükózszintet; a CSF-et szintén tenyészteni és gram-festeni kell. A vérkultúrák a VA sönt fertőzések hasznosabb mutatói, szemben a VP sönt fertőzésekkel.11 az agyi képalkotás felhasználható a ventriculitis vagy a CSF obstrukció bizonyítékainak azonosítására. Hasi képalkotás is használható a VP sönt hibás működésének azonosítására.
kezelési lehetőségek
jelenleg nincsenek gyakorlati irányelvek a sönt-fertőzések kezelésére; azonban a fertőzött hardver eltávolítása, külső kamrai lefolyó elhelyezése, tenyészetek, valamint IV vagy intraventrikuláris anti-biotikumokkal történő kezelés mind a hatékony kezelési folyamat részét képezik.2
a központi idegrendszer (CNS) fertőzés empirikus kezelésére vonatkozó jelenlegi ajánlások sönt jelenlétében IV vankomicin alkalmazását javasolják olyan szerrel kombinálva, amely megfelelő gram-negatív lefedettséggel rendelkezik, például cefepim, ceftazidim, cefotaxim vagy meropenem. A gyógyszer azon képessége, hogy behatoljon a CSF-be, valamint az antibiotikum aktivitása a bakteriális biofilm ellen szintén fontos figyelembe venni az antibiotikum megválasztásakor.21 Az ilyen szereket a kórokozó azonosításáig és a végleges kezelés meghatározásáig kell alkalmazni.22,23 VP sönt esetén a sönt disztális csúcsa a peritoneális üregben helyezkedik el, és érzékenyebb a gram-negatív baktériumokra; szinergia céljából gentamicin adható hozzá.2 az empirikus antimikrobiális terápiát és a sönt-fertőzésekre vonatkozó adagolási ajánlásokat a táblázat foglalja össze 3.2,18,22,23
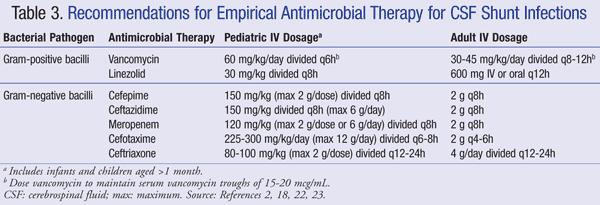
a vankomicin-terápiára refrakter betegek esetében a linezolid 10 mg/kg 8 óránként hatékonynak bizonyult monoterápiaként gyermekgyógyászati betegeknél.21 a rifampin kiegészítő terápiaként történő hozzáadása a központi idegrendszerbe való behatolása miatt is mérlegelhető.24 az antibiotikum-kezelés időtartama nagymértékben függ az alkalmazott műtéti megközelítéstől, a sönt típusától és az érintett kórokozótól, egy vizsgálat szerint a kezelés időtartama 4-47 nap.25,26 pontosabban 7-10 napot javasoltak a kezelés időtartamára, 23 hosszabb (10-14 napos) kúrával Gram-negatív fertőzések esetén.2
komplikált vagy kezelésre rezisztens shunt fertőzések esetén a klinikusoknak fontolóra kell venniük az antibiotikumok intrathecalis vagy intraventrikuláris alkalmazását a fokozott hatékonyság érdekében, mivel képesek magasabb baktericid koncentrációt elérni a központi idegrendszerben.23 a vankomicint és a gentamicint gyakran használják ebben a helyzetben, azonban nincsenek végleges ajánlások a használatukra vonatkozóan.22,23
gombás sönt fertőzések
a gombás sönt fertőzés ritkának tekinthető, egy vizsgálat 0,01% – os előfordulási arányt jelentett.27 a gombás sönt fertőzésért felelős leggyakoribb kórokozók a Candida fajok (beleértve a C albicans, C parapsilosis és C tropicalis), amelyek a gombás esetek 75% – át okozzák. Más organizmusok közé tartoznak a Histoplasmosis Fajok, Cryptococcus neoformansés Aspergillus Fajok. A gombás sönt fertőzések elsődleges kezelése a liposzómás amfotericin B 3-5 mg/kg/nap, legalább 12 hétig.27 az amfotericin B-t intoleráns betegeknél az 5-flucitozin lehet alternatíva.28 ezt gyakran követi napi 600-800 mg flukonazol vagy napi kétszer-háromszor 200 mg itrakonazol-kezelés legfeljebb 1 évig immunkompetens betegeknél, és potenciálisan egész életen át tartó kezelés immunhiányos betegeknél.27
következtetés
a sönt-fertőzések a hydrocephalus kezeléssel kapcsolatos kockázati tényezők. A fertőzés megelőzését empirikus antibiotikumokkal és AIS katéterek alkalmazásával igazolták, megfelelő aszeptikus technikával kombinálva, hogy jelentősen csökkentsék a fertőzés sebességét és csökkentsék a komorbid következmények kockázatát. Jelenleg nincsenek irányelvek a shunt fertőzések kezelésére; azonban IV empirikus terápia, amely magában foglalja mind a gram-pozitív, mind a gram-negatív lefedettséget, mint például a vankomicin és a harmadik generációs cefalosporin, ajánlott lenne. Intraventrikuláris antibiotikumokra is szükség lehet A maximális baktericid központi idegrendszeri koncentrációhoz.
1. Langley JM, Kavics D, Moore D, et al. A cerebrospinális folyadék sönt-asszociált fertőzéseinek vizsgálata az elhelyezést követő első évben, a kanadai nozokomiális fertőzés felügyeletével. Infect Control Kórházi Epidemiol. 2009;30:285-288.
2. Wells DL, Allen JM. Ventriculoperitonealis sönt fertőzések felnőtt betegeknél. AACN Adv Crit ellátás. 2013;24:6-12.
3. Lee JK, Seok JY, Lee JH és mtsai. A ventriculoperitonealis sönt fertőzések incidenciája és kockázati tényezői gyermekeknél: 333 egymást követő sönt vizsgálata 6 év alatt. J Koreai Med Sci. 2012;27:1563-1568.
4. Parker SL, Attenello FJ, Sciubba DM és mtsai. A sönt-fertőzés előfordulásának összehasonlítása az antibiotikummal impregnált magas kockázatú alcsoportokban, szemben a standard söntökkel. Childs Nerv Syst. 2009;25:77-83.
5. A hydrocephalus kezelése. Hydrocephalus Egyesület. www.hydroassoc.org / hydrocephalus-education-and-support/tanulás-about-hydrocephalus/kezelés-of-hydrocephalus/. Hozzáférés Február 11, 2014.
6. Patwardhan RV, Nanda A. beültetett kamrai söntök az Egyesült Államokban: a hydrocephalus kezelés évi milliárd dolláros költsége. Idegsebészet. 2005;56:139-144.
7. Dallacasa P, Dappozzo a, Galassi E, et al. Cerebrospinális folyadék shunt fertőzések csecsemőknél. Childs Nerv Syst. 1995;11:643-648.
8. Rogers EA, Kimia a, Madsen JR, et al. A kamrai sönt fertőzés előrejelzői a gyermekgyógyászati sürgősségi osztályon jelentkező gyermekek körében. Pediatr Emerg Ellátás. 2012;28:405-409.
9. Ratilal BO, Costa J, Sampaio C. antibiotikum profilaxis intracranialis kamrai söntök műtéti bevezetéséhez. Cochrane Database Syst Rev. 2006; (3): CD005365.
10. Shunt rendszerek. Hydrocephalus Egyesület. www.hydroassoc.org/hydrocephalus-education-and-support/learning-about-hydrocephalus/shunts. hozzáférés február 12, 2014.
11. Előre KR, kevesebb HD, Stiver HG. Cerebrospinális folyadék sönt fertőzés. 35 fertőzés áttekintése 32 betegnél. J Idegsebész. 1983;59:389-394.
12. Lan CC, Wong TT, Chen SJ és mtsai. A ventriculoperitonealis shunt fertőzések és a hydrocephalusban szenvedő gyermekek működési zavarainak korai diagnosztizálása. J Mikrobiol Immunol Fertőz. 2003;36:47-50.
13. Kestle JR, Riva-Cambrin J, Wellons JC és mtsai. Szabványosított protokoll a cerebrospinális folyadék shunt fertőzésének csökkentésére: a Hydrocephalus klinikai kutatási hálózat minőségjavítási kezdeményezése. J Neurosurg Pediatr. 2011;8:22-29.
14. Shah SS, Sinkowitz-Cochran RL, Keyserling HL és mtsai. Vancomycin alkalmazása gyermekgyógyászati idegsebészeti betegeknél. Am J Megfertőzni Ellenőrzés. 1999;27:482-487.
15. Bratzler DW, Dellinger EP, Olsen KM és mtsai. Klinikai gyakorlati irányelvek az antimikrobiális profilaxishoz a műtét során. Am J Egészség-Syst Pharm. 2013;70:195-283.
16. Parker SL, Anderson WN, Lilienfeld S és mtsai. Cerebrospinális shunt fertőzés antibiotikummal impregnált betegeknél, szemben a standard shuntokkal. J Neurosurg Pediatr. 2011;8:259-265.
17. Attenello F, Garces-Ambrossi G, Zaidi H, et al. Kórházi költségek a sönt fertőzésekkel kapcsolatban antibiotikummal impregnált sönt katétereket kapó betegeknél, szemben a szokásos sönt katéterekkel. Idegsebészet. 2010;66:284-289.
18. Sciubba DM, Stuart RM, McGirt MJ és mtsai. Az antibiotikumokkal impregnált sönt katéterek hatása a sönt fertőzés előfordulásának csökkentésére a hidrocefalusz kezelésében. J Idegsebész. 2005;103 (kiegészítés): 131-136.
19. Babu MA, Patel R, Marsh WR és mtsai. A kamrai katéterfertőzések kockázatának csökkentésére irányuló stratégiák: a bizonyítékok áttekintése. Neurokrit Ellátás. 2012;16:194-202.
20. Bratzler DW, Dellinger EP, Olsen KM és mtsai. Klinikai gyakorlati irányelvek az antimikrobiális profilaxishoz a műtét során. Surg Fertőzés (Larchmt). 2013;14:73-156.
21. Yilmaz A, Dalg N, Musluman M, et al. Gyermekek sönt okozta cerebrospinális folyadékfertőzéseinek Linezolid kezelése. J Neurosurg Pediatr. 2010;5:443-448.
22. Tunkel AR, Hartman BJ, Kaplan SL, et al. Gyakorlati irányelvek a bakteriális meningitis kezelésére. Clin Megfertőzi Dis-T. 2004;39:1267-1284.
23. Van De Beek D, Drake JM, Tunkel AR. Nozokomiális bakteriális meningitis. N Engl J Med. 2010;362:146-154.
24. Hedberg A, Hardemark HG, Olsson-Liljequist B, et al. A fuzidinsav és a rifampicin penetrációja a cerebrospinális folyadékba a Staphylococcus epidermidis által okozott alacsony fokú gyulladásos meningitisben. Clin Mikrobiol Fertőzés. 2004;10:765-768.
25. Antimikrobiális profilaxis műtéthez. Treat Guidel Med Lett. 2004;2:27-32.
26. Simon TD, Hall M, Dean JM, et al. A kezdeti cerebrospinális folyadék sönt-fertőzést követő újrafertőzés. J Neurosurg Pediatr. 2010;6:277-285.
27. A. V., Ludwig C., Camara-Quintana JQ és mtsai. Ventriculoperitonealis sönt gombás fertőzése: hisztoplazmózis diagnózis és kezelés. Világ Idegsebész. 2013;80:222.e5-e13.
28. Chiou CC, Wong TT, Lin HH és mtsai. A ventriculoperitoneális söntök gombás fertőzése gyermekeknél. Clin Megfertőzi Dis-T. 1994;19:1049-1053.