US Pharm. 2014; 39(4): HS2-HS7.
ABSTRAKT: řízení hydrocefalus nahromadění mozkomíšního moku (CSF) v komorách mozku, často zahrnuje zkrat implantace, aby se zabránilo dlouhodobé účinky. Shunty jsou drenážní zařízení určená k udržení intrakraniálního tlaku a zabránění další akumulaci CSF, ale mohou zavádět patogeny do centrálního nervového systému. To může vést k infekcím a následkům, jako jsou záchvaty, selhání zkratu, meningitida, sepse a encefalitida. Infekcím lze zabránit použitím aseptických technik, chemoprofylaxe a / nebo zkratů eluujících antibiotika. Léčba infekce zkratu může zahrnovat odstranění infikovaného hardwaru, umístění drenážního zařízení a použití IV nebo intraventrikulárních antibiotik.
Hydrocefalus je stav, vyznačující se tím, hromadění mozkomíšního moku (CSF) do komor nebo subarachnoidálním prostoru v mozku, což vede ke zvýšené intraventrikulární tlak a ventrikulární dilatace. Společnou etiologií hydrocefalu je poškození drenáže CSF.1,2 vzniku hydrocefalu ve Spojených Státech a v Evropě se odhaduje na 0,5 až 0,8 na 1000 narozených dětí a je často sekundární spina bifida, intrakraniální krvácení, nebo vrozená etiologie.1,3 Další potenciální příčiny hydrocefalus zahrnují myelodysplasie, nádory, meningitida, cysta zadní jámy lebeční, Dandy-Walker malformace, nebo aqueductal stenóza.4
mechanický posun je primární léčbou hydrocefalu. Umístění zkratu související s hydrocefalem jsou nejčastějším neurochirurgickým postupem prováděným u dětí, ale mají také nejvyšší míru selhání.5 přes 40,000 shunt umístění se provádí ročně v USA, s odhadovanou úmrtností na lůžku 2.7%.5,6 zavedení běžné kožní flóry a dalších patogenů, perioperačně i po operaci, může vést k infekcím zkratu a vést k selhání zkratu.
míra shuntových infekcí se odhaduje na 1,6% až 16,7% u dospělých pacientů, ale až 20% u pediatrických pacientů.2,7 Tento zvýšený výskyt v dětské populaci je myšlenka být kvůli nedostatku imunity (zejména <1 roku věku), u předčasně narozených dětí (<35 týdnů gestačního věku), expozice potenciální patogeny, doprovodnými chorobami, a další fyziologické faktory.3,4 Pediatričtí pacienti mají tendenci vyvinout zkrat infekce dříve než dospělí, přičemž většina infekcí se vyskytla během prvních 30 až 60 dnů po umístění.1
pacienti ve věku <5 let a dospělí ve věku 50 až 59 let mají největší výskyt infekcí shuntem.1 Rizikové faktory pro derivační infekce mohou zahrnovat mladším věku, pooperační únik CSF, intraventrikulární krvácení, více fistule, shunt revizní operace v posledních 90 dní, bočníky umístěné bezprostředně po meningitidy, delší pobyt v nemocnici (>1 měsíc), a předchozí zkrat infekce.2,4,7,8 komplikace související s infekcemi zkratu zahrnují poruchy zkratu, krátkodobé nebo dlouhodobé kognitivní poruchy, sepse, meningitida a prodloužený pobyt v nemocnici.1,4,8
typy Bočníků
nejběžnější typy zkratů jsou shrnuty v tabulce 1. Tento článek se zaměří na dvě nejvíce využívané bočníky: ventriculoperitoneal (VP) a ventriculoatrial (VA) bočníky. VP shunt, častější dvou, práce přesměrování CSF do pobřišnice, vzhledem k tomu, VA bočníky posun SSR do atria srdce.2,9,10

Patogeneze Zkrat Infekce
Zkrat znečištění je často způsobena, když proximální konec zkratu přichází do styku s normální kožní flóry. K tomu může dojít po operaci v důsledku infekce rány nebo perioperačně během chirurgické implantace.11 Gram-pozitivní bakterie, jako jsou koaguláza-negativní Staphylococcus epidermidis a Staphylococcus aureus, jsou zodpovědné za 45% na 60%1-3,12 a 20% na 33%2,3 (s jedním zprávu až 80% 4) zkrat infekce, resp. Tyto patogeny jsou úzce spojeny s časnými infekcemi shuntu (vyskytující se do 4 týdnů po operaci shuntu).2
pozdní infekce shuntu se mohou objevit několik měsíců po operaci shuntu a představují přibližně 15% infekcí souvisejících s shuntem.3 V mnoha případech, tyto pozdní infekce může být způsobena buď gram-pozitivní bakterie, jako je Streptococcus nebo Enterococcus species, nebo gram-negativní bakterie, nejčastěji Pseudomonas aeruginosa, pokud má pacient zažil střevní perforace nebo peritonitidy (především vidět v VP shunt).2 nejčastější patogeny spojené s infekcemi zkratu jsou shrnuty v tabulce 2.1-4,11 infekce zvyšují pravděpodobnost komplikací a selhání souvisejících se zkratem.

Předcházení Zkratu Infekce
Metody, aby se zabránilo zkratu infekce zahrnují použití sterilní techniky, systémová antibiotika a antibiotika-impregnované katétry. Ukázalo se, že aseptická chirurgická technika pomáhá snížit riziko infekcí zkratu. Standardní chirurgický protokol, včetně předoperační mytí pacienta vlasy s chlorhexidin šampon, dvakrát rukavicích všemi členy operačního týmu, a používání antibiotik-impregnované bočníky (AIS), který byl zaveden o čtyři děti v nemocnicích prokázána infekce, snížení nezaměstnanosti z 8,8% na 5,7%.13
systémová profylaktická antibiotika mohou být použita během postupu a v počátečních 24 hodinách po umístění zkratu. Podle metaanalýzy snížilo použití systémových, profylaktických antibiotik a katétrů impregnovaných antibiotiky rychlost infekcí zkratu.9 Tato stejná studie srovnávala použití systémové, preventivní antibiotika versus placebo pro snížení zkrat infekce a zjistil, že antibiotika snížila sazby zkrat infekce (odds ratio , 0.52).9 zatímco nejvhodnější profylaktické antibiotikum pro umístění zkratu nebylo v minulosti dobře definováno, většina lékařů používá k chirurgické profylaxi IV cefazolin nebo vankomycin.2,14 nedávné pokyny doporučují cefazolin pro neurochirurgické postupy posunování tekutin s klindamycinem a vankomycinem jako alternativami pro alergické pacienty.15
katétry AIS se běžně používají k prevenci infekcí zkratu od jejich zavedení v roce 2002.16 většina zařízení je impregnována kombinací rifampicinu a klindamycinu.4,16,17 jsou určeny k cílení na kolonizaci grampozitivních bakterií, které produkují glykoproteinový biofilm, který ulpívá na povrchu katétru.16 Jedna meta-analýza se podíval na používání antibiotik-impregnované katétry versus standardní katetry a zjistil, že používání antibiotik-impregnované katétry byl spojen s snížil sazby zkratu infekce (NEBO, 0.21). V této metaanalýze byl učiněn závěr, že použití jak systémové profylaxe antibiotiky,tak katétrů impregnovaných antibiotiky by mohlo být prospěšné při snižování infekcí shuntu.9
retrospektivní studie byla také provedena u pediatrických pacientů, kteří podstoupili zavedení zkratu během 3letého časového rámce. Během prvních 18 měsíců dostávali pacienti katétry impregnované neantibiotiky; pro příštích 18 měsíců dostal každý nový pacient vyžadující umístění zkratu katétry impregnované antibiotiky. Všechny děti byly sledovány po dobu 6 měsíců po umístění zkratu. Děti s neantibioticky impregnovanými katétry měly míru infekce 12%, zatímco infekce byla pozorována pouze u 1, 4% dětí s katétry impregnovanými antibiotiky.18 novější revize 15 studie také dospěla k závěru, že antibiotika potahované katétry snížení klinických míra infekce, zejména u pacientů, kteří mají dlouhodobé katétry, které se liší od některých předchozích analýz.19
bylo prokázáno, že prevence infekcí shuntem profylaxií a použitím katétrů AIS snižuje náklady na péči o pacienta.20 odhaduje se, že náklady na léčbu derivační infekce se může pohybovat od $17,300 na $48,454 na pacienta, což vede k odhadované roční nemocnice náklady v USA 2 miliardy dolarů.16,17 ačkoli každý katétr AIS stojí v průměru 400 USD, množství peněz ušetřených prevencí infekce a / nebo reinfekce může poskytnout významné dlouhodobé úspory.16 Tyto úspory jsou vzhledem k 2,4 násobnému snížení pravděpodobnosti infekce a snížení času v nemocnici v důsledku infekce. Bylo hlášeno, že tyto úspory by činily více než $ 440,000 na 100 pacientů posunutých.17
diagnostika infekcí shuntu
obecné příznaky infekce shuntu zahrnují bolest hlavy, nevolnost, zvracení, zánět místa chirurgického zákroku, neurologické abnormality, horečku a záchvaty.2,3 klinické projevy infekcí zkratu specifické pro pacienta závisí na typu implantovaného zkratu. VP shunty mohou být spojeny s peritonitidou, anorexií, podrážděností a bolestí břicha,8 zatímco va shunty mohou být spojeny se sepse a endokarditidou.2,3-Li se klinické projevy, jako je změněný duševní stav, erytém v okolí bočníku stránky, tekutiny podél shunt sledovat, hnisavý výtok, papilledema, vypouklé fontanela, nuchální rigidita, nebo zřejmé CSF úniku jsou vidět, pacienta by měla být hodnocena s CSF analýza, krevní kultury a mozkové zobrazovací.8
analýza CSF prediktivní pro infekci zahrnuje zvýšený počet bílých krvinek, zvýšené koncentrace bílkovin a snížené hladiny glukózy; CSF by měl být také kultivován a gram-obarven. Krevní kultury jsou užitečnějšími ukazateli infekcí VA shunt na rozdíl od infekcí VP shunt.11 mozkové zobrazování lze použít k identifikaci ventrikulitidy nebo důkazu obstrukce CSF. Abdominální zobrazování může být také použito k identifikaci poruchy zkratu VP.
Možnosti Léčby
v Současné době, nejsou tam žádné practice guidelines pro léčbu derivační infekce; nicméně, odstranění nakažených hardware, umístění externí ventrikulární kanalizace, kultur a zacházení s IV nebo intraventrikulární antibiotika jsou prokazatelně součástí účinného řízení procesu.2
Aktuální doporučení pro empirickou léčbu centrálního nervového systému (CNS), infekce v přítomnosti zkratu doporučujeme používat IV vankomycin v kombinaci s agentem, který má odpovídající gram-negativní pokrytí, jako cefepim, ceftazidim, cefotaxim, nebo meropenem. Schopnost léku proniknout do CSF, stejně jako aktivita antibiotika proti bakteriálnímu biofilmu, je také důležité vzít v úvahu při výběru antibiotik.21 taková činidla by měla být podávána, dokud není identifikován patogen a stanovena definitivní léčba.22,23 v VP zkratu leží distální špička zkratu v peritoneální dutině a je náchylnější k gramnegativním bakteriím; gentamicin může být přidán pro synergii.2 Empirické antimikrobiální terapie a dávkování doporučení pro zkrat infekce jsou shrnuty v TABULCE 3.2,18,22,23
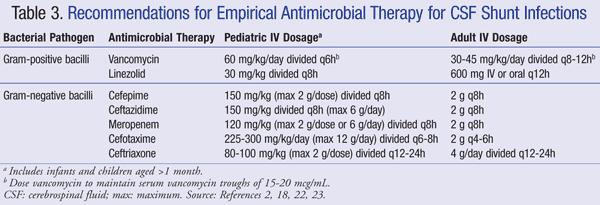
Pro pacienty refrakterní k vankomycinu terapie, linezolid 10 mg/kg každých 8 hodin bylo prokázáno, že být účinná jako monoterapie u dětských pacientů.21 přidání rifampinu jako doplňkové terapie může být také zváženo kvůli jeho proniknutí do CNS.24 délka antibiotické léčby závisí do značné míry na chirurgickém přístupu, který se používá, typ zkratu, a patogenu, jedna studie hlásí trvání léčby rozmezí 4 až 47 dní.25,26 konkrétněji bylo navrženo 7 až 10 dní pro trvání léčby, 23 s delším průběhem (10-14 dní) doporučeným pro gramnegativní infekce.2
V případě komplikovaných nebo ošetření-rezistentní shunt infekcí, lékaři by měli zvážit intrathekální nebo intraventrikulárního podávání antibiotik pro zvýšení účinnosti vzhledem k jejich schopnosti k dosažení vyšší baktericidní koncentrace v CNS.23 vankomycin a gentamicin se v této situaci běžně používají; neexistují však žádná definitivní doporučení ohledně jejich použití.22,23
Houbové Zkrat Infekce
houbové zkrat infekce je považován za vzácný, s jedné studie vykazování incidence 0,01%.27 nejčastějšími patogeny odpovědnými za infekci houbovým zkrat jsou druhy Candida (včetně C albicans, C parapsilosis A C tropicalis), které způsobují 75% případů plísní. Mezi další organismy patří druhy histoplazmózy, Cryptococcus neoformans a druhy Aspergillus. Primární léčbou infekcí houbovým zkratem je lipozomální amfotericin B 3 až 5 mg / kg / den po dobu nejméně 12 týdnů.27 u pacientů netolerujících amfotericin B může být alternativou 5-flucytosin.28 To je často následuje léčba s flukonazolem na 600 až 800 mg/den nebo itrakonazol v dávce 200 mg dvakrát až třikrát denně po dobu až 1 roku, v imunokompetentních pacientů a potenciálně život-dlouhé léčby u pacientů, kteří jsou imunokompromitovaní.27
závěr
shuntové infekce jsou rizikovým faktorem spojeným s léčbou hydrocefalem. Prevence infekce byla prokázána u empirických antibiotik a používání AIS katetry, v kombinaci s správné aseptické techniky, aby výrazně snížit výskyt infekcí a snížit riziko těchto následků. Momentálně zde nejsou žádné pokyny pro léčbu derivační infekce; nicméně, IV empirická terapie zahrnující jak gram-pozitivní a gram-negativní pokrytí, jako je vankomycin a třetí generace cefalosporin, by bylo doporučeno. Intraventrikulární antibiotika mohou být také potřebná pro maximální baktericidní koncentraci CNS.
1. Langley JM, Gravel D, Moore D, et al. Studie infekcí spojených s zkratem mozkomíšního moku v prvním roce po umístění kanadským dohledem nad nozokomiální infekcí. Infect Control Nemocnice Epidemiol. 2009;30:285-288.
2. Wells DL, Allen JM. Infekce ventrikuloperitoneálního zkratu u dospělých pacientů. AACN Adv Crit péče. 2013;24:6-12.
3. Lee JK, Seok JY, Lee JH, et al. Incidence a rizikové faktory ventriculoperitoneal zkratu infekcí u dětí: studie 333 po sobě jdoucích zkratů v 6 letech. J Korean Med Sci. 2012;27:1563-1568.
4. Parker SL, Attenello FJ, Sciubba DM, et al. Srovnání výskytu shuntové infekce ve vysoce rizikových podskupinách, které dostávají antibiotiky impregnované, versus standardní shunty. Childs Nerv Syst. 2009;25:77-83.
5. Léčba hydrocefalu. Hydrocefalus Asociace. WWW.hydroassoc.org / hydrocefalus-vzdělávání a podpora / učení o hydrocefalu / léčba hydrocefalu/. Přístup K 11. Únoru 2014.
6. Patwardhan RV, Nanda A. Implantovány komory bočníky ve Spojených Státech: miliardy-dolaru-za-rok náklady hydrocefalus léčby. Neurochirurgie. 2005;56:139-144.
7. Dallacasa P, Dappozzo A, Galassi E, et al. Infekce zkratu mozkomíšního moku u kojenců. Childs Nerv Syst. 1995;11:643-648.
8. Rogers EA, Kimia A, Madsen JR, et al. Prediktory infekce komorového zkratu u dětí prezentujících se na pediatrickém pohotovostním oddělení. Pediatr Emerg Care. 2012;28:405-409.
9. Ratilal BO, Costa J, Sampaio C. antibiotická profylaxe pro chirurgické zavedení intrakraniálních komorových zkratů. Cochrane Database Syst Rev. 2006; (3): CD005365.
10. Zkrat systémy. Hydrocefalus Asociace. www.hydroassoc.org/hydrocephalus-education-and-support/learning-about-hydrocephalus/shunts. Přístup 12. Února 2014.
11. Vpřed KR, méně HD, Stiver HG. Infekce zkratu mozkomíšního moku. Přehled 35 infekcí u 32 pacientů. J. 1983;59:389-394.
12. Lan CC, Wong TT, Chen SJ, et al. Včasná diagnóza infekcí ventrikuloperitoneálního zkratu a poruch u dětí s hydrocefalem. J Mikrobiol Imunol Infikovat. 2003;36:47-50.
13. Kestle JR, Riva-Cambrin J, Wellons JC, et al. Standardizovaný protokol ke snížení infekce zkratu mozkomíšního moku: iniciativa pro zlepšení kvality sítě hydrocefalus Clinical Research Network. J Neurochirurg Pediatr. 2011;8:22-29.
14. Shah SS, Sinkowitz-Cochran RL, Keyserling HL, et al. Použití vankomycinu u pediatrických neurochirurgických pacientů. Jsem J Kontrola Infekce. 1999;27:482-487.
15. Bratzler DW, Dellinger EP, Olsen KM, et al. Pokyny pro klinickou praxi pro antimikrobiální profylaxi v chirurgii. Am J Health-Syst Pharm. 2013;70:195-283.
16. Parker SL, Anderson WN, Lilienfeld S, et al. Infekce mozkomíšního zkratu u pacientů léčených antibiotiky impregnovanými oproti standardním zkratům. J Neurochirurg Pediatr. 2011;8:259-265.
17. Attenello F, Garces-Ambrossi G, Zaidi H, et al. Náklady na nemocnici spojené s infekcemi zkratu u pacientů užívajících zkrat katétry impregnované antibiotiky oproti standardním katétrům. Neurochirurgie. 2010;66:284-289.
18. Sciubba DM, Stuart RM, McGirt MJ, et al. Účinek zkrat katétrů impregnovaných antibiotiky při snižování výskytu infekce zkratu při léčbě hydrocefalu. J. 2005; 103 (suppl): 131-136.
19. Babu MA, Patel R, Marsh WR, et al. Strategie ke snížení rizika infekcí komorových katétrů: přehled důkazů. Neurokritická Péče. 2012;16:194-202.
20. Bratzler DW, Dellinger EP, Olsen KM, et al. Pokyny pro klinickou praxi pro antimikrobiální profylaxi v chirurgii. Surg Infect (Larchmt). 2013;14:73-156.
21. Yilmaz A, Dalgic N, Musluman M, et al. Linezolid léčba infekcí mozkomíšního moku souvisejících se shuntem u dětí. J Neurochirurg Pediatr. 2010;5:443-448.
22. Tunkel AR, Hartman BJ, Kaplan SL, et al. Praktické pokyny pro léčbu bakteriální meningitidy. Klinická Infekce Dis. 2004;39:1267-1284.
23. Van de Beek D, Drake JM, Tunkel AR. Nozokomiální bakteriální meningitida. N Engl J Med. 2010;362:146-154.
24. Hedberg A, Hardemark, Olsson-Liljequist B, et al. Penetrace kyseliny fusidové a rifampicinu do mozkomíšního moku při zánětlivé meningitidě nízkého stupně způsobené Staphylococcus epidermidis. Klinický Mikrobiol Infikovat. 2004;10:765-768.
25. Antimikrobiální profylaxe pro chirurgii. Treat Guidel Med Lett. 2004;2:27-32.
26. Simon TD, Hall M, Dean JM, et al. Reinfekce po počáteční infekci zkratu mozkomíšního moku. J Neurochirurg Pediatr. 2010;6:277-285.
27. Veeravagu A, Ludwig C, Camara-Quintana JQ, et al. Plísňová infekce ventrikuloperitoneálního zkratu: diagnostika a léčba histoplazmózy. Světová Neurochirurgie. 2013;80:222.e5-e13.
28. Chiou CC, Wong TT, Lin HH, et al. Plísňová infekce ventrikuloperitoneálních shuntů u dětí. Klinická Infekce Dis. 1994;19:1049-1053.