de tekniska detaljerna: Kemi
atomer, som är den grundläggande, grundläggande enheten i all materia, kan skilja sig mycket från varandra. Även om atomer är för små för att se utan att använda högdrivna mikroskop, består de av ännu mindre partiklar: protoner, neutroner och elektroner.
elektroner, som är extremt lätta, negativt laddade partiklar, kretsar runt en central massa-kärnan i en atom. Atomer kan få eller förlora elektroner, vilket förändrar laddningen av atomen (skapar joner). Atomen förblir emellertid samma element oavsett om den har en positiv, negativ eller neutral laddning.
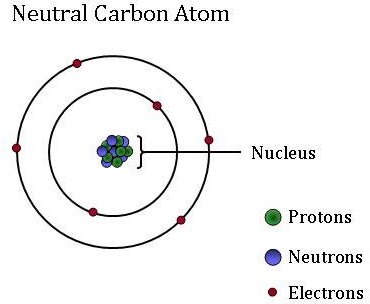
atomens lilla, täta kärna (eller Centrum) innehåller de andra komponenterna–protoner och neutroner. Protoner är positivt laddade partiklar, och antalet protoner är alltid fixerat för ett visst element. Med andra ord är antalet protoner det som ger varje element sin unika, individuella identitet. Till exempel har en kolatom sex protoner, men en atom med endast fem protoner är bor medan en atom med sju protoner är elementet kväve.
neutroner är neutrala – de har ingen laddning. Isotoper är atomer av samma element som har ett annat antal neutroner. Även om isotoper av samma element är tvillingar när det gäller reaktivitet, betyder det olika antalet neutroner att de har en annan massa. Vissa isotoper är rikligare i vissa material än andra eftersom vissa fysikaliska och kemiska processer ”föredrar” en isotop framför en annan. Dessa skillnader i isotopöverflöd används som” etiketter ” för att identifiera de olika källorna till CO2 som finns i ett atmosfäriskt CO2-prov. NOAA atmosfäriska forskare använder dessa isotopiska etiketter för att bestämma vilken procent av det kolet som härrör från fossila bränslen, den markbundna biosfären, eller från havet.
isotoper av kol
kolisotoper finns i tre former. Den överlägset vanligaste isotopen av kol är kol – 12 (12C), som innehåller sex neutroner utöver dess sex protoner. Den näst tyngsta kolisotopen, kol – 13 (13C), har sju neutroner. Både 12C och 13C kallas stabila isotoper eftersom de inte förfaller till andra former eller element över tiden. Den sällsynta kol-14 (14C) isotopen innehåller åtta neutroner i sin kärna. Till skillnad från 12C och 13C är denna isotop instabil eller radioaktiv. Med tiden kommer en 14C-atom att sönderfalla till en stabil produkt.

den stora majoriteten av allt kol som finns på jorden är 12C. nästan 99% av allt kol på jorden är av denna form. Medan endast cirka 1% av allt kol på jorden är av 13C-isotopformen, är 14C fortfarande mycket sällsynt. Endast en av varje biljon kolatomer är 14C.
för att få en uppfattning om hur få 14C-atomer det jämförs med 12c, låt oss jämföra en till en biljon. En biljon är en miljon miljoner. Om du ställde upp en biljon en dollarsedlar skulle den sträcka sig nästan från jorden till solen!