Introducere
clorul este unul dintre cele mai frecvent utilizate dezinfectante pentru dezinfectarea apei. Clorul poate fi aplicat pentru dezactivarea majorității microorganismelor și este relativ ieftin. Clorul este disponibil comercial sub formă de clor gazos (CL2) și sub formă de hipoclorit de sodiu lichid sau pulbere (NaOCL).
atât clorul gazos (CL2), cât și hipocloritul de sodiu (NaOCL) au proprietăți dezinfectante foarte limitate. Este formarea subproduselor de clor, cum ar fi acidul hipocloros (HOCL), ionul Hipoclorit (OCL-), acidul clorhidric (HCL) și oxigenul (o), care inhibă proprietățile dezinfectante.
clorul gazos
clorul gazos (CL2) este disponibil în comerț și este utilizat în principal în dezinfectarea apei din rețea.
când se adaugă clor gazos (CL2) în apă (H2O) are loc următoarea reacție de hidroliză:
Cl2 + H2O = H+ + Cl- + HOCl
Hipoclorit de sodiu
se produce Hipoclorit de sodiu adăugând clor gazos (CL2) la soda caustică (NaOH). Când se face acest lucru, hipocloritul de sodiu (NaOCL), apa (H2O) și sarea (NaCl) sunt produse conform următoarei reacții:
Cl2 + 2NaOH + NaOCl + NaCl + H2O
clorul reacționează cu hidroxidul de sodiu la hipocloritul de sodiu (NaOCl). Hipocloritul de sodiu este cunoscut sub numele de înălbitor. Înălbitorul (NaOCL) nu poate fi combinat cu acizi. Când NaOCL vine în contact cu acizii, hipocloritul devine instabil, provocând scăparea clorului gazos otrăvitor (CL2).
Hypochlorous Acid and Hypochlorite Ion formation
Hypochlorous Acid (HOCL) and Hypochlorite Ion (OCL-) are the by-products of Sodium Hypochlorite (NaOCL) in water (H2O). NaOCL reacts with water (H2O) to Hypochlorous Acid (HOCl) and Hypochlorite Ions (OCl-).
NaOCl + H2O → HOCl + NaOH-
Hypochlorous Acid formation
Hypochlorous Acid (HOCL) is the by-product of gaseous Chlorine (CL2) in Water. Gaseous Chlorine (CL2) reacts with water to Hypochlorous Acid (HOCL).
Cl2 + H2O -> HOCl + H+ + Cl-
formarea oxigenului
în funcție de valoarea pH-ului, acidul hipocloros (HOCL) expiră la ionii de hipoclorit (OCL -).
Cl2 + 2H2O -> HOCl + H3O + Cl – Hocl + H2O -> H3O+ + OCl-
aceasta se descompune la atomii de clor și oxigen:
OCl- -> Cl- + O
eficacitatea dezinfecției este determinată de pH.
dezinfecția va avea loc optim atunci când pH-ul este între 5 și 7, deoarece atunci este prezent un maxim de Hocl.
HOCL reacționează mai repede decât OCl- ; HOCL este cu 80-100% mai eficient decât OCL-. HOCL nu se evaporă și nu provoacă coroziune severă ca CL2. CL2 expus în aer poate fi foarte exploziv și evaporarea trebuie evitată. Din acest motiv, pH-ul ideal este între 6 și 7, deoarece nu este prezent CL2.
nivelul HOCL va scădea atunci când valoarea pH-ului este mai mare de 5. Nivelul HOCL va scădea atunci când valoarea pH-ului este mai mică de 5. Cu o valoare a pH – ului de 6,5, nivelul HOCL este mai mare de 90%, în timp ce concentrația de OCL-este mai mică de 10%.
clorul disponibil gratuit
clorul disponibil gratuit (FAC) este clorul care este prezent sub formă de acid hipocloros, ioni de hipoclorit sau sub formă de clor elementar dizolvat. FAC include toate speciile de clor care nu sunt combinate cu amoniac (sau alți compuși azotați) pentru a forma cloramine. Este ‘ gratuit ‘în sensul că nu a reacționat încă cu nimic și’ Disponibil ‘ în sensul că poate și va reacționa dacă este necesar.
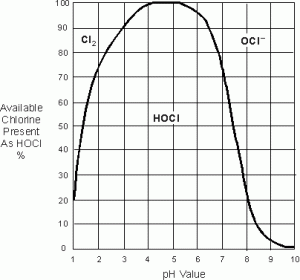
o valoare a pH-ului de la 6 la 7 este cea mai eficientă și cea mai sigură gamă de pH, datorită absenței clorului gazos. Prin urmare, atunci când se menționează clorul disponibil liber, se presupune că clorul disponibil liber constă exclusiv din HOCL și OCL-
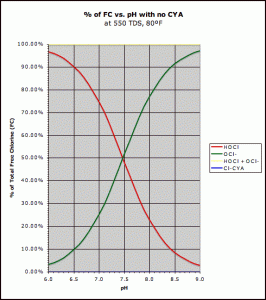
compuși de clor disponibili gratuit în ceea ce privește pH-ul .Acidul hipocloros (roșu) și ionul Hipoclorit (verde)
superioritatea acidului hipocloros în comparație cu ionul Hipoclorit
acidul hipocloros (HOCl, care este neutru din punct de vedere electric) și ionii Hipoclorit (OCl-, negativ din punct de vedere electric) vor forma clor liber Disponibil (FAC) atunci când sunt legați împreună. Acest lucru duce la dezinfecție. Ambele substanțe au un comportament foarte distinctiv.
peretele celular al microorganismelor patogene este încărcat negativ de natură. Ca atare, peretele celular a pătruns numai de acidul hipoclor neutru (HOCL), nu de ionul Hipoclorit încărcat negativ (OCL-).
HOCL poate penetra straturile de nămol, pereții celulari și straturile protectoare ale microorganismelor și, prin urmare, ucide eficient agenții patogeni. Microorganismele vor muri sau vor suferi de eșecuri de reproducere.
acidul hipocloros neutru cu pH (HOCL) poate pătrunde în pereții celulari ai microorganismelor patogene, în timp ce ionul Hipoclorit încărcat negativ (OCL-) nu poate pătrunde în pereții celulari.
pe lângă neutralitatea HOCL, este mult mai reactiv și este un dezinfectant mult mai puternic decât OCL-, deoarece HOCL este împărțit în acid clorhidric (HCl) și atom aer oxigen (O). Oxigenul este un dezinfectant foarte puternic.
apa Electrolizată neutră (HOCL) garantează dezinfectarea optimă
proprietățile dezinfectante ale clorului din apă se bazează pe formarea și puterea de oxidare a oxigenului și HOCL. Aceste condiții apar atunci când pH-ul este între 6 și 7.
apa Electrolizată neutră (nouă) produsă la fața locului dintr-un sistem AQUAOX are un pH de 6,5. La acest pH, mai mult de 90% din clorul liber disponibil este HOCL, mai puțin de 10% OCL – și nu se formează CL2. Puterea clorului liber Disponibil (FAC) în NEW este pre-setată la 300+ppm. Pentru a face o soluție cu 300 + ppm FAC din înălbitor Disponibil în comerț (NaOCL), se diluează în apă (H2O).
problema diluării înălbitorului în apă este dublă:
1) volumul pentru diluarea înălbitorului este foarte mic. Diferențele mici în volumul de înălbitor adăugat în apă determină diferențe semnificative în ceea ce privește pH-ul și clorul disponibil liber (FAC).
2) faptul că apa are niveluri de pH diferite în mod natural, determină ca adăugarea aceluiași volum de înălbitor să ducă la un pH diferit. Deși la fiecare diluție se pot măsura 300 + ppm FAC, pH – ul amestecului și, în consecință, cantitatea de compuși activi HOCL și OCL-pot varia considerabil.
prin urmare, proprietățile dezinfectante folosind înălbitor variază în timp ce proprietățile dezinfectante ale noilor sunt menținute stabile. Ca rezultat nou poate depăși proprietățile dezinfectante de înălbitor de 300 de ori.
siguranță
la producerea HOCL prin acidificarea NaOCL, prețurile relativ ridicate și posibilitatea reacțiilor secundare limitează utilizarea acizilor organici slabi; utilizarea acizilor anorganici mai ieftini provoacă descărcarea de clor gazos și o creștere a nivelului de toxicitate. Din această cauză, metoda de mai sus este utilizată numai pentru tratarea apei, unde valorile concentrației reziduale de clor nu depășesc 0,5-5mg/l.
diluarea clorului gazos în apă pentru a produce HOCL conform ecuației necesită măsuri speciale de siguranță și este utilizată numai pentru dezinfectarea volumelor mari de apă, unde concentrația activă de clor este sub 10-15mg/l. În prezent, toate companiile care produc clor gazos au oprit producția de clor gazos și au început fabricarea NaOCL exclusiv din considerente de siguranță.
apa Electrolizată neutră la fața locului produsă de AQUAOX Systems este o metodă unică de sinteză non-reactivă a HOCL. Dorim să subliniem încă o dată că calitatea unică a sistemului AQUAOX este posibilitatea reglării pH-ului direcționat în 6.0-7.0, în timp ce lucrează cu soluții de orice mineralizare, în timp ce electrolizele soluțiilor de clorură de sodiu au activitate biocidă identică dacă pH-ul și concentrația FAC sunt egale.
pentru mai multe informații, vă rugăm să contactați [email protected]