소개
염소는 물 소독에 가장 일반적으로 사용되는 소독제 중 하나입니다. 염소는 대부분의 미생물의 비활성화를 위해 적용될 수 있으며 상대적으로 저렴합니다. 염소는 가스 염소 및 차아 염소산 나트륨 액체 또는 분말(나오 클)로 상업적으로 이용 가능합니다.이 물질은 주로 얼룩이,더러운,스크래치 또는 젖지 않고 그래픽을 보호의 사용에 초점을 맞추고있다. 그것은 염소 부산물 같은 차아 염소산(호클),차아 염소산염 이온(오클),염산(호클)및 산소(오)소독 특성을 억제합니다.가스 염소(5453
가스 염소(5453
가스 염소)는 상업적으로 이용 가능하며 주로 물 소독에 사용됩니다.차아염소산나트륨은 가성소다에 기체 염소(물)를 첨가하여 생성된다. 염소는 수산화나트륨과 반응하여 차아염소산나트륨(차아염소산나트륨)과 반응하여 차아염소산나트륨(차아염소산나트륨)과 물(차아염소산나트륨)과 반응하여 차아염소산나트륨(차아염소산나트륨)과 반응하여 차아염소산나트륨(차아염소산나트륨)과 반응하여 차아염소산나트륨(차아염소산나트륨)과 반응하여 차아염소산나트륨(차아염소산나트륨)과 반응하여 차아염소산나트륨(차아염소산나트륨)과 반응하여 차아염소산나트륨(차아염소산나트륨)과 반응한다. 차아 염소산 나트륨은 표백제로 알려져 있습니다. 표백제(나오 클)는 산과 함께 사용할 수 없습니다. 나오 클이 산과 접촉 할 때 차아 염소산염이 불안정하여 유독 한 가스 염소가 빠져 나옵니다.
Hypochlorous Acid and Hypochlorite Ion formation
Hypochlorous Acid (HOCL) and Hypochlorite Ion (OCL-) are the by-products of Sodium Hypochlorite (NaOCL) in water (H2O). NaOCL reacts with water (H2O) to Hypochlorous Acid (HOCl) and Hypochlorite Ions (OCl-).
NaOCl + H2O → HOCl + NaOH-
Hypochlorous Acid formation
Hypochlorous Acid (HOCL) is the by-product of gaseous Chlorine (CL2) in Water. Gaseous Chlorine (CL2) reacts with water to Hypochlorous Acid (HOCL).차아염소산(차아염소산)은 차아염소산(차아염소산)이온으로 만료된다.
Cl2+2H2O->차아염소산+H3O+Cl-차아염소산+H2O->H3O++OCl-
이것은 염소 및 산소 원자:
OCl–>Cl-+O
의 효능 소독에 의해 결정됩 pH.
소독을 때 최적으로 pH is between5and7,다음으로 최대의 차아염소산가 존재합니다.
– ; 이 제품은 다른 장소에 쉽게 놓을 수 있습니다. 이 물질들은 증발하지 않으며 2 와 같은 심각한 부식을 일으키지 않습니다. 공기 중에 노출되는 클로 2 는 매우 폭발적 일 수 있으며 증발을 피해야합니다. 이러한 이유로 이상적인 산도는 6 과 7 사이입니다.
산도 값이 5 보다 높을 때 호클의 수준이 감소합니다. 이 값은 5 보다 낮을 때 감소 할 것입니다. 이 물질의 농도는 10%미만입니다.
자유 이용 가능한 염소
자유 이용 가능한 염소는 차아염소산,차아염소산염 이온 또는 용해된 원소 염소의 형태로 존재하는 염소이다. 클로라민을 형성하기 위해 암모니아(또는 다른 질소 화합물)와 결합되지 않은 모든 염소 종을 포함합니다. 그것은 아직 아무것도 반응하지 않은 의미에서’무료’이며,필요한 경우 반응 할 수 있다는 의미에서’사용 가능’입니다.
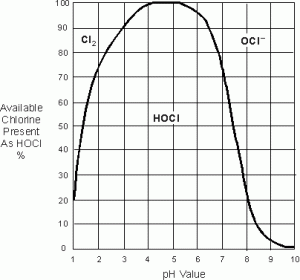
6~7 의 산도 값은 염소 가스의 부재로 인해 가장 효과적이고 안전한 산도 범위입니다. 따라서 무료 사용 가능한 염소가 언급 될 때,그것은 무료 사용 가능한 염소는 전적으로 호클과 오클로 구성되어 있다고 가정한다-
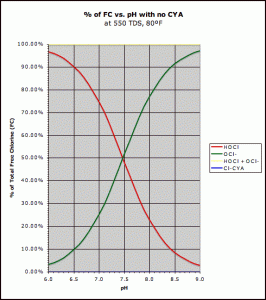
산도에 관한 무료 가능한 염소 화합물.하이포아염소산(적색)과 하이포아염소산염 이온(녹색)
하이포아염소산염 이온
하이포아염소산염 이온
하이포아염소산(전기적으로 중성인 호클)과 하이포아염소산염 이온(옥클-,전기적으로 음성인)에 비해 하이포아염소산의 우월성은 함께 결합될 때 이용 가능한 유리 염소를 형성할 것이다. 이 소독 결과. 두 물질 모두 매우 독특한 행동을합니다.
병원성 미생물의 세포벽은 자연에 의해 음전하를 띤다. 따라서 세포벽은 음으로 하전 된 차아 염소산염 이온이 아닌 중성 차아 염소산(호클)에 의해서만 침투합니다.
호클은 점액층,세포벽 및 미생물의 보호 층에 침투하여 병원균을 효과적으로 죽일 수 있습니다. 미생물은 죽거나 생식 실패로 고통받을 것입니다.
중성 하이포아염소산은 병원성 미생물의 세포벽을 관통할 수 있는 반면 음으로 하전된 하이포아염소산 이온은 세포벽을 관통할 수 없다.
외에도 중립성의 차아염소산,그것은 훨씬 더 민감하고 훨씬 더 강력한 살균제보다 OCL-로 차아염소산으로 분할되는 염산(HCl)및 원자기 산소(O). 산소는 매우 강력한 소독제입니다.
중성전분수(호클)는 최적의 소독을 보장합니다.
물 중 염소의 소독 물성은 산소와 호클의 형성과 산화력에 기초합니다.
이러한 조건은 산도가 6 에서 7 사이 일 때 발생합니다.
아쿠아옥스 시스템에서 현장에서 생산되는 중성 전해 물(신품)의 산도는 6.5 입니다. 이 산도에서 사용 가능한 유리 염소의 90%이상이 호클이며 10%미만이며 2 가 형성되지 않습니다. 새로운 무료 사용 가능한 염소(페이스)의 강도는 300+에 미리 설정되어 있습니다. 시판되는 표백제(나오 클)에서 300+폴리프로필렌 페이스를 사용하여 용액을 만들기 위해 물(물)에 희석합니다.
물 표백제를 희석 문제는 두 가지이다:
1)표백제를 희석 할 수있는 부피가 매우 작다. 물 첨가 표백제의 부피에 작은 차이는 산도 및 무료 사용 가능한 염소의 측면에서 상당한 차이가 발생(얼굴).
2)물 자연스럽 게 다른 산도 수준을가지고 있다는 사실,표 백제의 동일한 볼륨의 추가는 여전히 다른 산도 결과 발생 합니다. 각 희석에서 300+피피 프티 페이스를 측정 할 수 있지만,혼합물의 산도 및 결과적으로 활성 화합물의 양은 상당히 다를 수 있습니다.
따라서 표백제를 사용한 소독 특성은 다양하지만 신규의 소독 특성은 안정적으로 유지됩니다. 그 결과 새로운 표백제의 소독 특성을 300 배 초과 할 수 있습니다.
안전성
나오 클롤을 산성화하여 호클을 생산할 때 상대적으로 높은 가격과 부작용 가능성은 약한 유기산의 사용을 제한합니다; 더 싼 무기산의 사용은 기체 염소 배출과 독성 수준의 상승을 유발합니다. 그것 때문에,위의 방법은 사용되는 물 처리는 곳,염소 잔여 농도 값을 초과하지 않는 0.5-5mg/l.
희석의 기체 염소에서 물을 생산하는 차아염소산에 따라 방정식을 요구한 특별한 안전 대책과 사용에 대한 소독 다량의 물,active 염소 농도가 10-15mg/l. 요즘 가스 염소를 제조하는 모든 회사는 가스 염소 생산을 중단하고 안전 고려 사항 때문에 독점적으로 나오 클 제조를 시작했습니다.
아쿠아옥스시스템에서 생산되는 중성 물분해수는 호클의 비시약 합성의 독특한 방법이다. 우리는 아쿠아 옥스 시스템의 고유 한 품질이 6.0-7 에서 직접 산도 규제의 가능성이라는 것을 다시 한 번 지적하고 싶습니다.0 범위,어떤 광물 화의 솔루션으로 작업하는 동안,산도 및 안면 농도가 동일한 경우 염화나트륨 용액의 전해조는 동일한 살생 활성을 갖는 반면.
자세한 내용은 문의하시기 바랍니다 [email protected]