Johdanto
kloori on yksi yleisimmin käytetyistä desinfiointiaineista veden desinfiointiin. Klooria voidaan käyttää useimpien mikro-organismien deaktivointiin ja se on suhteellisen halpaa. Klooria on kaupallisesti saatavilla kaasumaisena Kloorina (CL2) ja Natriumhypokloriittinesteenä tai-jauheena (NaOCL).
sekä kaasumaisella kloorilla (CL2) että Natriumhypokloriitilla (NaOCL) on hyvin rajoitetut desinfioivat ominaisuudet. Desinfioivia ominaisuuksia estävät kloorin sivutuotteiden, kuten Hypokloorihapon (HOCL), hypokloriitti-Ionin (OCL -), suolahapon (HCL) ja hapen (O) muodostuminen.
kaasumaista klooria
kaasumaista klooria (CL2) on kaupallisesti saatavilla ja sitä käytetään pääasiassa vesijohtoveden desinfiointiin.
kun kaasumaista klooria (CL2) lisätään veteen (H2O), tapahtuu seuraava hydrolyysireaktio:
Cl2 + H2O = H+ + Cl- + HOCl
natriumhypokloriittia
natriumhypokloriittia tuotetaan lisäämällä kaasumaista klooria (CL2) kaustiseen soodaan (NaOH). Näin valmistetaan natriumhypokloriittia (NaOCL), vettä (H2O) ja suolaa (NaCl) seuraavan reaktion mukaisesti:
Cl2 + 2NaOH + → NaOCl + NaCl + H2O
kloori reagoi natriumhydroksidin kanssa Natriumhypokloriitiksi (NaOCl). Natriumhypokloriitti tunnetaan valkaisuaineena. Valkaisuainetta (NaOCL) ei voi yhdistää happoihin. Kun NaOCL joutuu kosketuksiin happojen kanssa, hypokloriitti muuttuu epävakaaksi, jolloin myrkyllistä kaasumaista klooria (CL2)pääsee karkaamaan.
Hypochlorous Acid and Hypochlorite Ion formation
Hypochlorous Acid (HOCL) and Hypochlorite Ion (OCL-) are the by-products of Sodium Hypochlorite (NaOCL) in water (H2O). NaOCL reacts with water (H2O) to Hypochlorous Acid (HOCl) and Hypochlorite Ions (OCl-).
NaOCl + H2O → HOCl + NaOH-
Hypochlorous Acid formation
Hypochlorous Acid (HOCL) is the by-product of gaseous Chlorine (CL2) in Water. Gaseous Chlorine (CL2) reacts with water to Hypochlorous Acid (HOCL).
Cl2 + H2O -> HOCl + H+ + Cl-
Hapenmuodostus
pH-arvosta riippuen Hypokloorihappo (HOCL) vanhenee hypokloriitti-ioneiksi (OCL -).
Cl2 + 2H2O -> HOCl + H3O + Cl – HOCl + H2O -> H3O+ + OCl-
tämä hajoaa kloori – ja Happiatomeiksi:
OCl- – > Cl – + O
desinfioinnin teho määritetään pH: n perusteella
desinfiointi tapahtuu optimaalisesti, kun pH-arvo on 5-7, Sillä silloin HOCL: n enimmäismäärä on olemassa.
HOCL reagoi nopeammin kuin OCl- ; HOCL on 80-100% tehokkaampi kuin OCL -. HOCL ei haihdu eikä aiheuta cl2: n kaltaista vakavaa korroosiota. Ilmassa oleva CL2 voi olla hyvin räjähdysherkkä ja haihtumista tulisi välttää. Tästä syystä ihanteellinen pH on välillä 6 ja 7, koska CL2: ta ei esiinny.
HOCL-taso laskee, kun pH-arvo on suurempi kuin 5. HOCL: n taso laskee, kun pH-arvo on alle 5. PH-arvolla 6,5 hocl-pitoisuus on yli 90%, kun taas OCL-pitoisuus on alle 10%.
vapaa käytettävissä oleva kloori
vapaa käytettävissä oleva kloori (FAC) on kloori, joka esiintyy Hypokloorihappona, hypokloriitti-ioneina tai liuenneena alkuainekloorina. FAC sisältää kaikki kloorilajit, jotka eivät yhdisty ammoniakin (tai muiden typpiyhdisteiden) kanssa kloramiinien muodostamiseksi. Se on ”vapaa” siinä mielessä, että se ei ole vielä reagoinut mihinkään, ja ”käytettävissä” siinä mielessä, että se voi ja reagoi tarvittaessa.
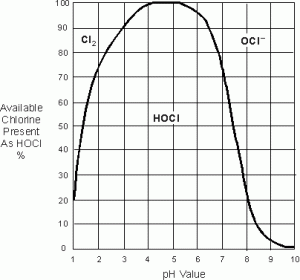
pH-arvo 6-7 on tehokkain ja turvallisin pH-alue kloorikaasun puuttumisen vuoksi. Kun siis mainitaan vapaasti käytettävissä oleva kloori, Oletetaan, että Vapaasti käytettävissä oleva kloori koostuu yksinomaan HOCL: stä ja OCL: stä.-
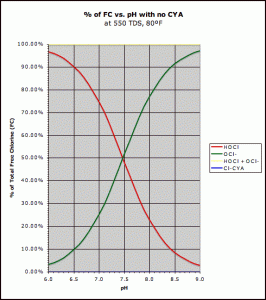
vapaasti saatavilla olevat klooriyhdisteet pH: n osalta .Hypokloorihappo (punainen) ja hypokloriitti-ioni (vihreä)
Hypokloorihapon ylivertaisuus hypokloriitti-ioniin
hypokloriitti-ioniin (hocl, joka on sähköisesti neutraali) ja hypokloriitti-ioneihin (OCl -, sähköisesti negatiivinen) muodostuu sitoutuessaan vapaasti käytettävissä olevaa klooria (FAC). Tämä johtaa desinfiointiin. Molemmilla aineilla on hyvin erottuva käyttäytyminen.
patogeenisten mikro-organismien soluseinä on luonteeltaan negatiivisesti varautunut. Sellaisenaan soluseinän lävistää vain neutraali Hypokloorihappo (HOCL), Ei negatiivisesti varautunut hypokloriitti-ioni (OCL -).
HOCL voi tunkeutua limakerroksiin, soluseiniin ja suojaaviin mikro-organismikerroksiin ja siten tappaa tehokkaasti taudinaiheuttajia. Pieneliöt joko kuolevat tai kärsivät lisääntymiskyvyttömyydestä.
pH: n neutraali Hypokloorihappo (HOCL) voi tunkeutua patogeenisten mikro-organismien soluseiniin, kun taas negatiivisesti varautunut hypokloriitti-ioni (OCL -) ei voi tunkeutua soluseiniin.
hocl: n neutraalisuuden lisäksi se on paljon reaktiivisempi ja paljon voimakkaampi desinfiointiaine kuin OCL -, sillä HOCL jakautuu suolahappoon (HCl) ja atomi-ilman Happeen (O). Happi on erittäin voimakas desinfiointiaine.
Neutraalielektrolysoitu vesi (Hocl) takaa optimaalisen desinfioinnin
kloorin desinfioivat ominaisuudet vedessä perustuvat hapen ja HOCL: n muodostumiseen ja hapettavuuteen. Nämä olosuhteet ilmenevät, kun pH on välillä 6 ja 7.
Neutraalielektrolysoitu vesi (uusi), joka on tuotettu paikan päällä AKVAOKSIJÄRJESTELMÄSTÄ, on pH 6,5. Tässä pH: ssa yli 90% vapaana olevasta kloorista on HOCL: ää, alle 10% OCL: ää – eikä CL2: ta muodostu. Vapaa käytettävissä kloorin (FAC) vahvuus NEW on ennalta asetettu 300+ppm. Jotta liuos, jossa on 300 + ppm FAC kaupallisesti saatavilla olevista valkaisuaineista (NaOCL), laimennetaan vedellä (H2O).
valkaisuaineen laimentamisen ongelma vedessä on kaksijakoinen:
1) valkaisuaineen laimentamisen tilavuus on hyvin pieni. Pienet erot veteen lisätyn valkaisuaineen määrässä aiheuttavat merkittäviä eroja pH: n ja vapaasti käytettävissä olevan kloorin (FAC) suhteen.
2) se, että veden pH-arvot ovat luonnostaan erilaiset, aiheuttaa sen, että saman määrän valkaisuainetta lisääminen johtaa edelleen eri pH-arvoon. Vaikka kussakin laimennuksessa voidaan mitata 300+ppm FAC, seoksen pH ja siten aktiivisten yhdisteiden HOCL ja OCL – määrä voivat vaihdella huomattavasti.
siksi valkaisuaineella desinfioivat ominaisuudet vaihtelevat, kun taas uusien desinfioivat ominaisuudet pysyvät vakaina. Tämän seurauksena Uusi voi ylittää valkaisuaineen desinfioivat ominaisuudet 300 kertaa.
turvallisuus
tuotettaessa HOCL: ää happamoittamalla NaOCL: ää suhteellisen korkeat hinnat ja mahdolliset sivureaktiot rajoittavat heikkojen orgaanisten happojen käyttöä; halvempien epäorgaanisten happojen käyttö aiheuttaa kaasumaisen kloorin purkautumista ja myrkyllisyystason nousua. Sen vuoksi edellä mainittua menetelmää käytetään vain vedenkäsittelyyn, jossa kloorijäämien pitoisuusarvot eivät ylitä 0,5-5mg/l.
kaasumaisen kloorin laimentaminen veteen HOCL: n tuottamiseksi yhtälön mukaisesti vaatii erityisiä turvatoimenpiteitä ja sitä käytetään vain suurten vesimäärien desinfiointiin, kun aktiivisen kloorin pitoisuus on alle 10-15mg/l. Nykyään kaikki kaasumaista klooria valmistavat yritykset lopettivat kaasumaisen kloorin tuotannon ja aloittivat NaOCL-valmistuksen yksinomaan turvallisuussyistä.
Aquaox Systemsin tuottama Neutraalielektrolysoitu vesi paikan päällä on ainutlaatuinen hocl: n reagoimattoman synteesin menetelmä. Haluamme korostaa vielä kerran, että AQUAOX-järjestelmän ainutlaatuinen laatu on mahdollisuus suunnattuun pH: n säätelyyn 6.0-7: ssä.0-alueet, kun käytetään minkä tahansa mineralisaation liuoksia, kun taas natriumkloridiliuosten elektrolyyseillä on sama biosidiaktiivisuus, jos pH-ja FAC-pitoisuus ovat yhtä suuret.
lisätietoja: [email protected]