Einführung
Chlor ist eines der am häufigsten verwendeten Desinfektionsmittel zur Wasserdesinfektion. Chlor kann zur Deaktivierung der meisten Mikroorganismen eingesetzt werden und ist relativ billig. Chlor ist im Handel als gasförmiges Chlor (CL2) und als Natriumhypochlorit flüssig oder Pulver (NaOCl) erhältlich.
Sowohl gasförmiges Chlor (CL2) als auch Natriumhypochlorit (NaOCl) haben sehr begrenzte desinfizierende Eigenschaften. Es ist die Bildung von Chlornebenprodukten wie Hypochloriger Säure (HOCL), Hypochlorition (OCL-), Salzsäure (HCL) und Sauerstoff (O), die die desinfizierenden Eigenschaften hemmen.
Gasförmiges Chlor
Gasförmiges Chlor (CL2) ist im Handel erhältlich und wird hauptsächlich zur Desinfektion von Leitungswasser verwendet.
Bei Zugabe von gasförmigem Chlor (CL2) zu Wasser (H2O) findet die folgende Hydrolysereaktion statt:
Cl2 + H2O = H+ + Cl- + HOCl
Natriumhypochlorit
Natriumhypochlorit wird durch Zugabe von gasförmigem Chlor (CL2) zu Natronlauge (NaOH) hergestellt. Wenn dies geschehen ist, werden Natriumhypochlorit (NaOCl), Wasser (H2O) und Salz (NaCl) gemäß der folgenden Reaktion hergestellt:
Cl2 + 2NaOH + → NaOCl + NaCl + H2O
Chlor reagiert mit Natriumhydroxid zu Natriumhypochlorit (NaOCl). Natriumhypochlorit ist als Bleichmittel bekannt. Bleichmittel (NaOCl) kann nicht mit Säuren kombiniert werden. Wenn NaOCl mit Säuren in Kontakt kommt, wird das Hypochlorit instabil, wodurch giftiges gasförmiges Chlor (CL2) entweicht.
Hypochlorous Acid and Hypochlorite Ion formation
Hypochlorous Acid (HOCL) and Hypochlorite Ion (OCL-) are the by-products of Sodium Hypochlorite (NaOCL) in water (H2O). NaOCL reacts with water (H2O) to Hypochlorous Acid (HOCl) and Hypochlorite Ions (OCl-).
NaOCl + H2O → HOCl + NaOH-
Hypochlorous Acid formation
Hypochlorous Acid (HOCL) is the by-product of gaseous Chlorine (CL2) in Water. Gaseous Chlorine (CL2) reacts with water to Hypochlorous Acid (HOCL).
Cl2 + H2O -> HOCl + H+ + Cl-
Sauerstoffbildung
Abhängig vom pH-Wert reagiert Hypochlorige Säure (HOCL) zu Hypochloritionen (OCL-).
Cl2 + 2H2O -> HOCl + H3O + Cl- HOCl + H2O -> H3O+ + OCl-
Dies zerfällt in Chlor- und Sauerstoffatome:
OCl- -> Cl- + O
Die Wirksamkeit der Desinfektion wird durch den pH-Wert bestimmt.
Die Desinfektion erfolgt optimal, wenn der pH-Wert zwischen 5 und 7 liegt, da dann maximal HOCL vorhanden ist.
HOCL reagiert schneller als OCl- ; HOCL ist 80-100% effektiver als OCL-. HOCL verdunstet nicht und verursacht keine starke Korrosion wie CL2. CL2 an der Luft kann sehr explosiv sein und Verdunstung sollte vermieden werden. Aus diesem Grund liegt der ideale pH-Wert zwischen 6 und 7, da kein CL2 vorhanden ist.
Der HOCL-Gehalt nimmt ab, wenn der pH-Wert höher als 5 ist. Der HOCL-Spiegel nimmt ab, wenn der pH-Wert unter 5 liegt. Bei einem pH-Wert von 6,5 beträgt der HOCL-Gehalt mehr als 90%, während die OCL-Konzentration weniger als 10% beträgt.
Frei verfügbares Chlor
Frei verfügbares Chlor (FAC) ist Chlor, das in Form von hypochloriger Säure, Hypochloritionen oder als gelöstes elementares Chlor vorliegt. FAC umfasst alle Chlorspezies, die nicht mit Ammoniak (oder anderen stickstoffhaltigen Verbindungen) zu Chloraminen kombiniert werden. Es ist ‚frei‘ in dem Sinne, dass es noch mit nichts reagiert hat, und ‚verfügbar‘ in dem Sinne, dass es bei Bedarf reagieren kann und wird.
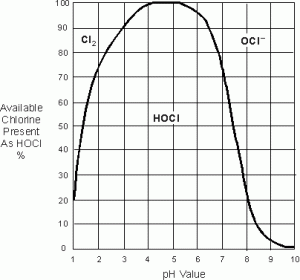
Ein pH-Wert von 6 bis 7 ist aufgrund der Abwesenheit von Chlorgas der effektivste und sicherste pH-Bereich. Deshalb, wenn freies verfügbares Chlor erwähnt wird, Es wird angenommen, dass freies verfügbares Chlor ausschließlich aus HOCL und OCL besteht-
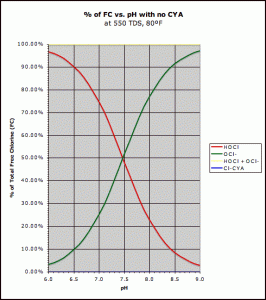
Frei verfügbare Chlorverbindungen in Bezug auf den pH-Wert .Hypochlorsäure (rot) und Hypochlorition (grün)
Überlegenheit von Hypochlorsäure im Vergleich zu Hypochlorition
Hypochlorsäure (HOCl, elektrisch neutral) und Hypochloritionen (OCl-, elektrisch negativ) bilden zusammen freies verfügbares Chlor (FAC). Dies führt zu einer Desinfektion. Beide Substanzen haben ein sehr ausgeprägtes Verhalten.
Die Zellwand pathogener Mikroorganismen ist von Natur aus negativ geladen. Als solches wird die Zellwand nur von der neutralen hypochlorigen Säure (HOCL) durchdrungen, nicht von negativ geladenen Hypochloritionen (OCL-).
HOCL kann Schleimschichten, Zellwände und Schutzschichten von Mikroorganismen durchdringen und dadurch Krankheitserreger wirksam abtöten. Die Mikroorganismen sterben entweder ab oder leiden an Fortpflanzungsstörungen.
Die pH-neutrale Hypochlorige Säure (HOCL) kann die Zellwände pathogener Mikroorganismen durchdringen, während das negativ geladene Hypochlorition (OCL-) die Zellwände nicht durchdringen kann.
Neben der Neutralität von HOCL ist es ein viel reaktiveres und viel stärkeres Desinfektionsmittel als OCL-, da HOCL in Salzsäure (HCl) und Atomluftsauerstoff (O) gespalten wird. Sauerstoff ist ein sehr starkes Desinfektionsmittel.
Neutrales elektrolysiertes Wasser (HOCL) garantiert optimale Desinfektion
Die desinfizierenden Eigenschaften von Chlor in Wasser basieren auf der Bildung und Oxidationskraft von Sauerstoff und HOCL. Diese Bedingungen treten auf, wenn der pH-Wert zwischen 6 und 7 liegt.
Neutrales elektrolysiertes Wasser (NEU), das vor Ort aus einem AQUAOX-System hergestellt wird, hat einen pH-Wert von 6,5. Bei diesem pH-Wert sind mehr als 90% des frei verfügbaren Chlors HOCL, weniger als 10% OCL- und es wird kein CL2 gebildet. Die Stärke von Free Available Chlorine (FAC) in NEW ist auf 300+ppm voreingestellt. Um eine Lösung mit 300+ ppm FAC aus handelsüblichem Bleichmittel (NaOCl) herzustellen, wird es in Wasser (H2O) verdünnt.
Das Problem beim Verdünnen von Bleichmittel in Wasser ist zweifach:
1) Das Volumen zum Verdünnen von Bleichmittel ist sehr klein. Kleine Unterschiede in der Menge an Bleichmittel, die dem Wasser zugesetzt wird, verursachen signifikante Unterschiede in Bezug auf pH-Wert und frei verfügbares Chlor (FAC).
2) Die Tatsache, dass Wasser von Natur aus unterschiedliche pH-Werte aufweist, bewirkt, dass die Zugabe des gleichen Volumens Bleichmittel immer noch zu einem anderen pH-Wert führt. Obwohl bei jeder Verdünnung 300+ ppm FAC gemessen werden können, kann der pH-Wert der Mischung und folglich die Menge der Wirkstoffe HOCL und OCL- erheblich variieren.
Daher variieren die desinfizierenden Eigenschaften mit Bleichmittel, während die desinfizierenden Eigenschaften von NEU stabil gehalten werden. Infolgedessen können SIE die desinfizierenden Eigenschaften von Bleichmittel um das 300-fache überschreiten.
Sicherheit
Bei der Herstellung von HOCL durch Ansäuern von NaOCl schränken relativ hohe Preise und die Möglichkeit von Nebenreaktionen die Verwendung schwacher organischer Säuren ein; die Verwendung von billigeren anorganischen Säuren provoziert die Abgabe von gasförmigem Chlor und eine Erhöhung des Toxizitätsniveaus. Aus diesem Grund wird das obige Verfahren nur zur Wasseraufbereitung verwendet, bei der die Werte der Restchlorkonzentration 0,5-5 mg / l nicht überschreiten.
Die Verdünnung von gasförmigem Chlor in Wasser zur Herstellung von HOCL gemäß Gleichung erfordert besondere Sicherheitsmaßnahmen und wird nur zur Desinfektion großer Wassermengen verwendet, bei denen die Aktivchlorkonzentration unter 10-15 mg / l liegt. Heutzutage haben alle Unternehmen, die gasförmiges Chlor herstellen, die Produktion von gasförmigem Chlor eingestellt und ausschließlich aus Sicherheitsgründen mit der Herstellung von NaOCl begonnen.
Neutrales elektrolysiertes Wasser, hergestellt von AQUAOX Systems, ist eine einzigartige Methode zur Synthese von HOCL ohne Reagenzien. Wir möchten noch einmal darauf hinweisen, dass die einzigartige Qualität des AQUAOX-Systems die Möglichkeit der gerichteten pH-Regulierung im Bereich von 6,0-7 ist.0 reicht, während mit Lösungen jeglicher Mineralisierung gearbeitet wird, während Elektrolysen von Natriumchloridlösungen eine identische biozide Aktivität aufweisen, wenn pH-Wert und FAC-Konzentration gleich sind.
Für weitere Informationen kontaktieren Sie bitte [email protected]