introdução
cloro é um dos desinfectantes mais usados para a desinfecção da água. O cloro pode ser aplicado para a desativação da maioria dos microorganismos e é relativamente barato. O cloro está disponível comercialmente como cloro gasoso (CL2) e como hipoclorito de sódio líquido ou pó (NaOCL).
tanto o cloro gasoso (CL2) como o hipoclorito de sódio (NaOCL) têm propriedades de desinfecção muito limitadas. É a formação de subprodutos de cloro tais como ácido hipocloroso (HOCL), Ião hipoclorito (OCL -), ácido clorídrico (HCL) e oxigênio (O) que inibem as propriedades de desinfecção.
cloro gasoso
cloro gasoso (CL2) está disponível comercialmente e é principalmente utilizado na desinfecção da água da rede.
Quando o Cloro gasoso (CL2) adicionado à água (H2O) a seguinte reação de hidrólise ocorre:
Cl2 + H2O = H+ + Cl- + HOCl
Hipoclorito de Sódio
Hipoclorito de Sódio é produzido a adição de Cloro gasoso (CL2) a soda cáustica (NaOH). Quando isso é feito, o Hipoclorito de Sódio (NaOCL), água (H2O) e de sal (NaCl), são produzidos de acordo com a seguinte reação:
Cl2 + 2NaOH + → NaOCl + NaCl + H2O
o Cloro reage com o hidróxido de sódio para o Hipoclorito de Sódio (NaOCl). O hipoclorito de sódio é conhecido como lixívia. A lixívia (NaOCL) não pode ser combinada com ácidos. Quando o NaOCL entra em contacto com ácidos, o hipoclorito torna-se instável, causando a fuga de cloro gasoso (CL2).
Hypochlorous Acid and Hypochlorite Ion formation
Hypochlorous Acid (HOCL) and Hypochlorite Ion (OCL-) are the by-products of Sodium Hypochlorite (NaOCL) in water (H2O). NaOCL reacts with water (H2O) to Hypochlorous Acid (HOCl) and Hypochlorite Ions (OCl-).
NaOCl + H2O → HOCl + NaOH-
Hypochlorous Acid formation
Hypochlorous Acid (HOCL) is the by-product of gaseous Chlorine (CL2) in Water. Gaseous Chlorine (CL2) reacts with water to Hypochlorous Acid (HOCL).
Cl2 + H2O -> HOCl + H+ + Cl-
formação de Oxigênio
Dependendo do valor do pH, Ácido hipocloroso (HOCL) expira ao Hipoclorito de Íons (OCL-).
Cl2 + 2H2O -> HOCl + H3O + Cl – HOCl + H2O -> H3O+ + OCl-
Este cai ao Cloro e átomos de Oxigênio:
OCl- -> Cl- + O
A eficácia da desinfecção é determinada pelo pH.
Desinfecção irá ter lugar ideal quando o pH está entre 5 e 7, como um máximo de HOCL está presente.
HOCL reage mais depressa do que a OCl- ; A HOCL é 80-100% mais eficaz do que a OCL-. O HOCL não evapora e não provoca corrosão grave como o CL2. CL2 exposto no ar pode ser muito explosivo e a evaporação deve ser evitada. Por esta razão, o pH ideal é entre 6 e 7, Como nenhum CL2 está presente.
o nível de HOCL diminuirá quando o valor do pH for superior a 5. O nível de HOCL diminuirá quando o valor de pH for inferior a 5. Com um valor de pH de 6,5, o nível de HOCL é superior a 90%, enquanto a concentração de OCL – é inferior a 10%.
cloro livre disponível
cloro livre disponível (FAC) é cloro que está presente na forma de ácido hipocloroso, iões hipocloritos ou como cloro elementar dissolvido. A FAC inclui todas as espécies de cloro que não são combinadas com amoníaco (ou outros compostos azotados) para formar cloraminas. É “livre” no sentido em que ainda não reagiu com nada, e “disponível” no sentido em que pode e irá reagir se necessário.
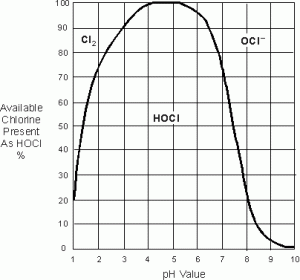
um valor de pH de 6 a 7 é a gama de pH mais eficaz e mais segura, devido à ausência de gás cloro. Por conseguinte, quando se menciona o cloro livre disponível, parte-se do princípio de que o cloro livre disponível consiste unicamente em HOCL e OCL.-
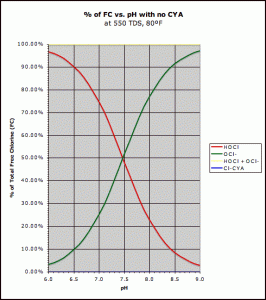
compostos clorados disponíveis livres no que respeita ao pH .O Ácido hipocloroso (vermelho) e Hipoclorito de lítio (verde)
Superioridade do Ácido hipocloroso comparado ao Hipoclorito de Íon
o Ácido hipocloroso (HOCl, que é eletricamente neutro) e Hipoclorito de Íons (OCl-, eletricamente negativo) vai formulário de Cloro Livre (FAC) quando ligados juntos. Isto resulta em desinfecção. Ambas as substâncias têm um comportamento muito distinto.
a parede celular dos microrganismos patogénicos é negativamente carregada por natureza. Como tal, a parede celular apenas penetrou pelo ácido hipocloroso neutro (HOCL), não por íon hipoclorito carregado negativamente (OCL-).
HOCL pode penetrar em camadas de lodo, paredes celulares e camadas protectoras de microrganismos e, consequentemente, matar eficazmente os agentes patogénicos. Os microrganismos morrerão ou sofrerão de falhas reprodutivas.
o ácido hipocloroso neutro do pH (HOCL) pode penetrar nas paredes celulares de microrganismos patogénicos, enquanto o ião hipoclorito carregado negativamente (OCL-) não pode penetrar nas paredes celulares.
além da neutralidade de HOCL, ele é muito mais reativo e é um desinfetante muito mais forte do que a OCL-, como HOCL é dividido em ácido clorídrico (HCl) e oxigênio do ar atômico (O). O oxigénio é um desinfectante muito poderoso.
água Electrolisada neutra (HOCL) garante a desinfecção ideal
as propriedades de desinfecção do cloro na água são baseadas na formação e poder oxidante de oxigénio e HOCL. Estas condições ocorrem quando o pH está entre 6 e 7.
água Electrolisada Neutra (Nova) produzida no local a partir de um sistema AQUAOX tem um pH de 6,5. A este pH mais de 90% do cloro livre disponível é HOCL, menos de 10% OCL – e nenhum CL2 são formados. A resistência do cloro livre disponível (FAC) em Novo é pré-definida para 300 ppm+. Para fazer uma solução com 300+ppm FAC a partir de lixívia comercialmente disponível (NaOCL), é diluída em água (H2O).
o problema com a diluição da lixívia na água é duplo:
1) o volume para diluir a lixívia é muito pequeno. Pequenas diferenças no volume de lixívia adicionada à água causam diferenças significativas em termos de pH e cloro livre disponível (FAC).
2) o facto de a água ter níveis de pH naturalmente diferentes, faz com que a adição do mesmo volume de lixívia ainda resulte num pH diferente. Embora a cada diluição possa ser medida a FAC de 300 ppm+ppm, o pH da mistura e, consequentemente, a quantidade de compostos activos HOCL e OCL – podem variar consideravelmente.
por conseguinte, as propriedades de desinfecção com lixívia variam, ao passo que as propriedades de desinfecção dos novos são mantidas estáveis. Como resultado, novas podem exceder 300 vezes as propriedades de desinfecção da lixívia.Ao produzir HOCL por acidificação da NaOCL, preços relativamente elevados e possibilidade de reacções laterais limitam a utilização de ácidos orgânicos fracos.; o uso de ácidos inorgânicos mais baratos provoca descarga de cloro gasoso e um aumento do nível de toxicidade. Devido a isso, o método acima é usado apenas para o tratamento de água, onde os valores de concentração de cloro residual não excedem 0,5-5mg/l.
diluição de cloro gasoso na água para produzir HOCL de acordo com a equação exige medidas de segurança especiais e é usado apenas para desinfecção de grandes volumes de água, onde a concentração de cloro ativo é inferior a 10-15mg/l. Hoje em dia, todas as empresas que fabricam cloro gasoso cessaram a produção de cloro gasoso e iniciaram a produção de NaOCL exclusivamente por razões de segurança.
água Electrolisada neutra produzida por AQUAOX Systems é um método único de síntese não reagente de HOCL. Gostaríamos de salientar mais uma vez que a qualidade única do sistema AQUAOX é a possibilidade de regulação do pH direcionada no 6.0-7.0 gamas, ao trabalhar com soluções de qualquer mineralização, enquanto eletrólises de soluções de cloreto de sódio têm atividade biocida idêntica se pH e concentração FAC são iguais.Para mais informações, contactar: [email protected]