Inleiding
chloor is een van de meest gebruikte ontsmettingsmiddelen voor waterdesinfectie. Chloor kan worden toegepast voor de deactivering van de meeste micro-organismen en het is relatief goedkoop. Chloor is in de handel verkrijgbaar als gasvormig chloor (CL2) en als Natriumhypochlorietvloeistof of-poeder (NaOCL).
zowel gasvormig chloor (CL2) als natriumhypochloriet (NaOCL) hebben zeer beperkte desinfecterende eigenschappen. Het is de vorming van chloorbijproducten zoals hypochloorzuur (HOCL), Hypochlorietion (OCL -), zoutzuur (HCL) en zuurstof (O) die desinfecterende eigenschappen remmen.
gasvormig chloor
gasvormig chloor (CL2) is in de handel verkrijgbaar en wordt meestal gebruikt voor het desinfecteren van leidingwater.
wanneer gasvormig chloor (CL2) aan water (H2O) wordt toegevoegd, vindt de volgende hydrolysereactie plaats:
Cl2 + H2o = h+ + Cl- + HOCl
natriumhypochloriet
natriumhypochloriet wordt geproduceerd door gasvormig chloor (CL2) toe te voegen aan natronloog (NaOH). Als dit gebeurt, worden natriumhypochloriet (NaOCL), water (H2O) en zout (NaCl) geproduceerd volgens de volgende reactie:
Cl2 + 2NaOH + → NaOCl + NaCl + H2O
chloor reageert met natriumhydroxide tot natriumhypochloriet (NaOCl). Natriumhypochloriet staat bekend als bleekmiddel. Bleekmiddel (NaOCL) kan niet worden gecombineerd met zuren. Wanneer NaOCL in contact komt met zuren wordt het hypochloriet instabiel, waardoor giftig gasvormig chloor (CL2) ontsnapt.
Hypochlorous Acid and Hypochlorite Ion formation
Hypochlorous Acid (HOCL) and Hypochlorite Ion (OCL-) are the by-products of Sodium Hypochlorite (NaOCL) in water (H2O). NaOCL reacts with water (H2O) to Hypochlorous Acid (HOCl) and Hypochlorite Ions (OCl-).
NaOCl + H2O → HOCl + NaOH-
Hypochlorous Acid formation
Hypochlorous Acid (HOCL) is the by-product of gaseous Chlorine (CL2) in Water. Gaseous Chlorine (CL2) reacts with water to Hypochlorous Acid (HOCL).
Cl2 + H2O – > HOCl + H + + Cl –
zuurstofvorming
afhankelijk van de pH-waarde vervalt Hypochlorietzuur (HOCL) tot Hypochlorietionen (OCL -).
Cl2 + 2H2O -> HOCl + H3O + Cl – HOCl + H2O -> H3O+ + OCl-
dit valt uiteen tot chloor – en zuurstofatomen:
OCl- – > Cl – + O
de doeltreffendheid van desinfectie wordt bepaald door de pH.
de desinfectie vindt optimaal plaats wanneer de pH tussen 5 en 7, omdat dan maximaal HOCL aanwezig is.
HOCL reageert sneller dan OCl- ; HOCL is 80-100% effectiever dan OCL-. HOCL verdampt niet en veroorzaakt geen ernstige corrosie zoals CL2. CL2 blootgesteld in lucht kan zeer explosief zijn en verdamping moet worden vermeden. Daarom ligt de ideale pH tussen 6 en 7, omdat er geen CL2 aanwezig is.
het HOCL-gehalte neemt af wanneer de pH-waarde hoger is dan 5. Het niveau van HOCL zal afnemen wanneer de pH-waarde lager is dan 5. Met een pH-waarde van 6,5 is het niveau van HOCL meer dan 90%, terwijl de concentratie van OCL-minder dan 10% is.
vrij beschikbaar chloor
vrij beschikbaar chloor (FAC) is chloor dat aanwezig is in de vorm van hypochloorzuur, hypochlorietionen of als opgelost elementair chloor. FAC omvat alle chloorsoorten die niet worden gecombineerd met ammoniak (of andere stikstofverbindingen) om chloramines te vormen. Het is ‘ vrij ‘in de zin dat het nog niet met iets heeft gereageerd, en’ beschikbaar ‘ in de zin dat het kan en zal reageren indien nodig.
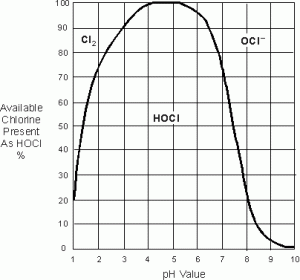
een pH-waarde van 6 tot 7 is het meest effectieve en veiligste pH-bereik, vanwege de afwezigheid van chloorgas. Wanneer vrij beschikbaar chloor wordt genoemd, wordt ervan uitgegaan dat vrij beschikbaar chloor uitsluitend bestaat uit HOCL EN OCL-
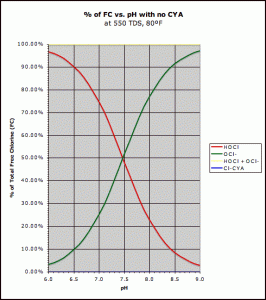
vrij beschikbare chloorverbindingen met betrekking tot pH .Hypochloorzuur (rood) en Hypochlorietion (groen)
superioriteit van Hypochlorietzuur in vergelijking met Hypochlorietion
Hypochlorietzuur (hocl, dat elektrisch neutraal is) en Hypochlorietionen (OCl-, elektrisch negatief) vormen vrij beschikbaar chloor (FAC) wanneer ze samen worden gebonden. Dit resulteert in desinfectie. Beide stoffen hebben zeer onderscheidend gedrag.
de celwand van pathogene micro-organismen is van nature negatief geladen. Als zodanig, de celwand alleen gepenetreerd door het neutrale Hypochlorous zuur (HOCL), niet door negatief geladen Hypochloriet Ion (OCL-).
HOCL kan slijmlagen, celwanden en beschermende lagen van micro-organismen binnendringen en daarmee ziekteverwekkers effectief doden. De micro-organismen zullen sterven of lijden aan voortplantingsstoornissen.
het pH-neutrale hypochloorzuur (HOCL) kan celwanden van pathogene micro-organismen binnendringen, terwijl het negatief geladen Hypochlorietion (OCL -) de celwanden niet kan binnendringen.
naast de neutraliteit van HOCL is het een veel reactiever en veel sterker desinfecterend middel dan OCL-, omdat HOCL wordt gesplitst in zoutzuur (HCl) en atoom luchtzuurstof (O). Zuurstof is een zeer krachtig ontsmettingsmiddel.
neutraal elektrolytisch water (HOCL) garandeert een optimale desinfectie
de desinfecterende eigenschappen van chloor in water zijn gebaseerd op de vorming en oxiderende kracht van zuurstof en HOCL. Deze voorwaarden treden op wanneer de pH tussen 6 en 7 is.
neutraal elektrolytisch water (Nieuw) dat ter plaatse uit een AQUAOX-systeem wordt geproduceerd, heeft een pH van 6,5. Bij deze pH is meer dan 90% van het vrij beschikbare chloor HOCL, minder dan 10% OCL – EN geen CL2 gevormd. De sterkte van vrij beschikbaar chloor (FAC) in nieuw is vooraf ingesteld op 300+ppm. Om een oplossing met 300 + ppm FAC te maken van in de handel verkrijgbaar bleekmiddel (NaOCL), wordt het verdund in water (H2O).
het probleem met het verdunnen van bleekwater in water is tweeledig:
1) het volume voor het verdunnen van bleekwater is zeer klein. Kleine verschillen in het volume van bleekwater toegevoegd aan water veroorzaakt significante verschillen in termen van pH en vrij beschikbaar chloor (FAC).
2) het feit dat water van nature verschillende pH-waarden heeft, zorgt ervoor dat de toevoeging van hetzelfde volume bleekmiddel nog steeds leidt tot een andere pH. Hoewel bij elke verdunning 300 + ppm FAC kan worden gemeten, kan de pH van het mengsel en bijgevolg de hoeveelheid actieve verbindingen HOCL EN OCL – aanzienlijk variëren.
daarom variëren de desinfecterende eigenschappen met bleekmiddel, terwijl de desinfecterende eigenschappen van NEW stabiel blijven. Hierdoor kan nieuw de desinfecterende eigenschappen van bleekmiddel met 300 keer overschrijden.
veiligheid
bij de productie van HOCL door het aanzuren van NaOCL beperken relatief hoge prijzen en de mogelijkheid van bijwerkingen het gebruik van zwakke organische zuren; het gebruik van goedkopere anorganische zuren veroorzaakt gasvormige chloorlossing en een verhoging van het toxiciteitsniveau. Daarom wordt bovenstaande methode alleen gebruikt voor waterbehandeling, waarbij de residuele chloorconcentratie niet hoger is dan 0,5-5mg/l.
verdunning van gasvormig chloor in water om HOCL te produceren volgens de vergelijking vereist speciale veiligheidsmaatregelen en wordt alleen gebruikt voor het desinfecteren van grote hoeveelheden water, waarbij de concentratie actief chloor lager is dan 10-15mg/l. Tegenwoordig zijn alle bedrijven die gasvormig chloor produceren gestopt met de productie van gasvormig chloor en zijn ze uitsluitend uit veiligheidsoverwegingen begonnen met de productie van NaOCL.
neutraal elektrolytisch water dat ter plaatse wordt geproduceerd door AQUAOX-systemen is een unieke methode voor de niet-reagenssynthese van HOCL. We willen er nogmaals op wijzen dat de unieke kwaliteit van het AQUAOX-systeem de mogelijkheid is van gerichte pH-regeling in de 6.0-7.0 bereiken, terwijl het werken met oplossingen van elke mineralisatie, terwijl elektrolysen van natriumchloride-oplossingen identieke biocide activiteit als pH en FAC concentratie gelijk zijn.
voor meer informatie kunt u contact opnemen met [email protected]