US Pharm. 2006;7:58-68.
hjertesvigt er et stort sundhedsproblem i USA. Cirka fem millioner mennesker har hjertesvigt, og 550.000 patienter diagnosticeres med hjertesvigt hvert år.1,2 hjertesvigt er generelt karakteriseret som en sygdom hos ældre; cirka 80% af patienterne indlagt med hjertesvigt er ældre end 65 år. Således forventes forekomsten af hjertesvigt at vokse, når befolkningen bliver ældre.2 hjertesvigt-relaterede indlæggelser steg med cirka 25% til mere end en million mellem 1990 og 1999. I 2001 forårsagede hjertesvigt direkte 53.000 dødsfald. Hjertesvigt-relaterede dødsfald er steget i de senere år, hvilket kan tilskrives en stigning i overlevelse fra tidligere kardiovaskulære hændelser.
hjertesvigt er et klinisk syndrom, hvor funktionelle eller strukturelle ændringer forekommer i hjertet, hvilket resulterer i kliniske symptomer såsom dyspnø, træthed, begrænset træningstolerance, lungestop og perifert ødem.1-3 mange kendte risikofaktorer, såsom koronararteriesygdom (CAD), diabetes, fedme, hypertension og familiehistorie af kardiomyopatier, er forbundet med indtræden og progression til hjertesvigt (tabel 1).4 derudover er valvulær hjertesygdom stadig en almindelig årsag til hjertesvigt. 90% af tiden og øger patientens risiko for hjertesvigt tredobbelt.5 CAD er den mest almindelige årsag til systolisk hjertesvigt. Myokardieinfarkt (MI) tegner sig for systolisk hjertesvigt hos næsten 70% af patienterne. Yderligere etiologier forbundet med systolisk dysfunktion og hjertesvigt inkluderer dilaterede kardiomyopatier og ventrikulær hypertrofi.2,4

Patofysiologi
systolisk hjertesvigt er forbundet med svækkelse af venstre ventrikulær kontraktilitet, der resulterer i ineffektiv hjerteproduktion, især under anstrengelse. Hjertesvigt begynder normalt med en vis skade eller stress på myokardiet, der resulterer i en ændring i hjertets struktur; dette er kendt som hjerteomdannelse. Hjertemodellering går forud for symptomernes begyndelse i måneder eller endda år. Da dilatation ændrer ventriklen til en mere sfærisk form, begynder hæmodynamiske belastninger at øge belastningen på væggene i den svigtende ventrikel, hvilket fører til deprimeret mekanisk funktion og øget regurgitant strømning gennem mitralventilen.1-3
det neurohormonale system har en aktiv rolle i accelerationen af hjerteomdannelse. Patienter med hjertesvigt har forhøjede niveauer af noradrenalin, angiotensin II, aldosteron, endothelin, vasopressin og cytokiner. Aktiveringen af renin-angiotensin-aldosteronsystemet øger perifer vasokonstriktion, hvilket resulterer i øget efterbelastning og hjerteomdannelse. Derudover forårsager aktiveringen af det sympatiske nervesystem takykardi, hvilket fører til øget myokardisk iltbehov. Øget hjerte iltbehov uden ændringer i udbuddet kan forårsage øget myokardisk iskæmi og yderligere hjerteomdannelse. Neurohormonerne kan udøve kardiotoksiske virkninger på cellerne, hvilket yderligere kan ændre hjertets arkitektur og ydeevne.2
klinisk præsentation
systolisk hjertesvigt er et syndrom diagnosticeret baseret på data indsamlet fra en grundig patienthistorie, herunder en evaluering af symptomatologi og fysiske fund. De fleste patienter er til stede på en af tre måder: med nedsat træningstolerance, med væskeretention eller uden symptomer.2,6 dyspnø ved anstrengelse og åndenød er de kardinale symptomer på hjertesvigt. Ved fysisk undersøgelse kan perifert ødem, lungestop eller begge symptomer være til stede.2
klassificering af hjertesvigt er baseret på kombinationen af American College of Cardiology/American Heart Association ‘ s fire stadier af hjertesvigt (tabel 1), der spænder fra risiko for hjertedysfunktion (trin A) til ildfast hjertesvigt (trin D) og på Ny York Heart Association (NYHA) retningslinjer.2,6 NYHA-klassifikationen er den mest anvendte metode til kvantificering af graden af funktionel begrænsning pålagt ved hjertesvigt (tabel 2). Samlet set har den funktionelle klassificering af hjertesvigt en tendens til at falde over tid på grund af udviklingen af hjerteomdannelsen.2
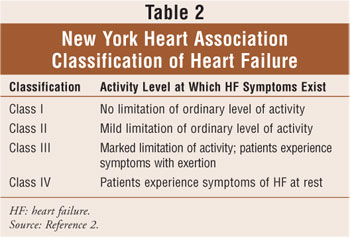
den mest nyttige diagnostiske test er det omfattende todimensionale ekkokardiogram, der bruges sammen med Doppler-strømningsundersøgelser for at afgøre, om der er strukturelle og funktionelle abnormiteter i hjertet. Det transthoraciske ekkokardiogram (TTE) er en ikke-invasiv ultralydundersøgelse, der producerer billeder af hjertet ved hjælp af lydbølger. Det giver information om estimering af venstre ventrikulær udstødningsfraktion (LVEF), ventrikulære dimensioner og volumener, vægvolumener, hjertekammergeometri og regional vægbevægelse. Hos patienter med systolisk hjertesvigt er LVEF normalt mindre end 40%.2 andre undersøgelser anvendt i forbindelse med TTE til vurdering af etiologi, sværhedsgrad og potentielle lægemiddelrelaterede behandlingseffekter ved hjertesvigt inkluderer baseline røntgenbillede af brystet, 12-bly elektrokardiografi og målinger af hjerne natriuretisk peptid, serumelektrolytter og nyrefunktion. Disse undersøgelser er vigtige, fordi sundhedspersonale kan bruge dem som en basislinje til at bestemme, om en patient har oplevet en ændring i klinisk status.2,6
håndtering af systolisk hjertesvigt
ikke-farmakologisk
kontrol af risikofaktorer såsom hypertension, diabetes mellitus, dyslipidemier, aterosklerotiske vaskulære sygdomme og skjoldbruskkirtelforstyrrelser kan bremse udviklingen af hjertesvigt og hjerteomdannelse.2,4,6 patienter med hjertesvigt bør modtage influence-og pneumokokvacciner for at reducere risikoen for comorbiditeter såsom luftvejsinfektioner.2 den mest signifikante modificerbare risikofaktor ville være højrisikoadfærd som rygning, alkohol og ulovlig stofbrug.2,7
Natriumbegrænsning (?2 gram/dag) hjælper med at reducere volumenoverbelastning og kan nedsætte brugen af diuretika. Desuden giver daglig vejning patienter mulighed for at vurdere volumenstatus, hvorpå diuretisk dosisjustering kan baseres. Imidlertid har ingen undersøgelser undersøgt effekten af natriumbegrænsning i kosten på sygelighed eller dødelighed.7,8 fysisk aktivitet har vist sig at mindske dødelighed og indlæggelser for patienter med stabil hjertesvigt. Begrænsning af motion fremmer fysisk dekonditionering, hvilket kan bidrage til en patients træningsintolerance. Endelig har overholdelse af diæt og terapeutisk medicinregime en væsentlig rolle i forebyggelsen af akutte indlæggelser.2,7
farmakologisk
de fleste patienter med hjertesvigt behandles med en standard kombination med tre lægemidler: et loop-diuretikum, en ACE-hæmmer eller en angiotensin II-receptorblokker (ARB) og en beta-adrenerg receptorblokker.1,2 diuretika er grundpillerne for reduktion af symptomer på volumenoverbelastning ved hjertesvigt, mens ACE-hæmmere, ARB ‘ er og betablokkere har vist sig at reducere sygelighed og dødelighed.2 aldosteronantagonister er indiceret som supplerende behandling til patienter med symptomatisk NYHA klasse III eller IV hjertesvigt eller efter tidlig akut MI hos patienter med nedsat venstre ventrikelfunktion og klinisk bevis for hjertesvigt. Hvis patienter fortsat er symptomatiske, kan digoksin føjes til standardmedicinregimen for at reducere symptomer, mindske indlæggelser og øge træningstolerancen. Lægemidler, der anvendes til behandling af hjertesvigt, er beskrevet i tabel 3. Livsstilsændringer og lægemiddelterapier til systolisk hjertesvigt er designet til at reducere sygelighed og dødelighed, forhindre progression af hjerteomdannelse og forbedrepatienters livskvalitet.2
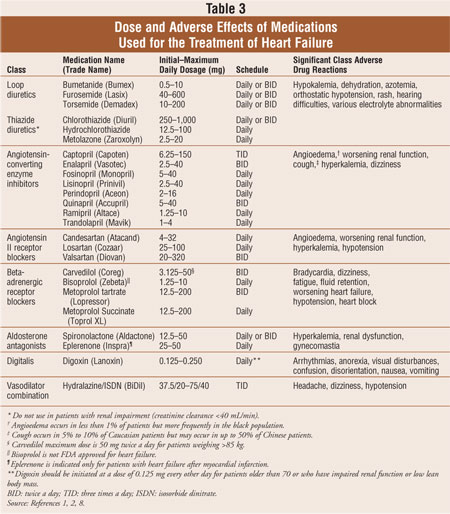
diuretika:Grundpillerne i symptomatisk behandling af volumenoverbelastning ved hjertesvigt, diuretika mindsker væskeretention, der forårsager lungestop, perifert ødem, jugular venøs distention og/eller øget kropsvægt. Loop-diuretika, der virker i Henle-sløjfen, øger serumnatriumudskillelsen med 20% til 25%, forbedrer eliminering af frit vand og opretholder deres virkning hos patienter med nedsat nyrefunktion.1,2 I modsætning hertil reducerer diuretika natriumudskillelsen med 5% til 10%, forbedrer eliminering af frit vand og mister deres virkning hos patienter med kronisk nyresygdom (kreatininclearance <40 mL/min). Loopdiuretika er de foretrukne midler til behandling af hjertesvigt, men thiasider kan anvendes til patienter med mild væskeretention og hypertension. Diuretika, såvel som ACE-hæmmere og beta-blokkere, anbefales til brug hos alle patienter i fase C hjertesvigt.2 undersøgelser har vist, at diuretika forbedrer hjertefunktion, symptomer og træningsintolerance hos patienter med hjertesvigt. Imidlertid er de langsigtede virkninger af diuretika på dødelighed ukendt.1,2,8
ACE-hæmmere: ACE-hæmmere reducerer aktiviteten af renin-angiotensin-aldosteronsystemet ved at blokere omdannelsen af angiotensin I til angiotensin II, hvilket forhindrer angiotensin II–induceret vasokonstriktion. De hæmmer også aldosteronfrigivelse, hvilket fører til et fald i natrium-og væskeretention. Disse kombinerede effekter reducerer både forbelastning og afterload og bremser udviklingen af hjerteomdannelse.1,2 ACE-hæmmere kan også have yderligere aktivitet med forøget kininer og kinin-medieret prostaglandinproduktion.2 Over 30 kliniske kontrollerede forsøg, der evaluerer effekten af ACE-hæmmere, har vist, at ACE-hæmmere reducerer risikoen for død og kombineret risiko for død og indlæggelser. Alle patienter med systolisk hjertesvigt i venstre ventrikel bør gives en ACE-hæmmer, medmindre den er kontraindiceret (angioødem, bilateral nyrearteriestenose, serumkalium >5,5 mekv/L, graviditet, symptomatisk hypotension eller ustabil nyresvigt). ACE-hæmmere bør initieres ved lave doser og titreres langsomt baseret på tolerabilitet af bivirkninger.1,2,8
ARB ‘er: sammenlignet med forsøg med ACE-hæmmere har færre kliniske forsøg undersøgt brugen af ARB’ er hos patienter med hjertesvigt; disse midler er således forbeholdt patienter med påvist intolerance af ACE-hæmmere. ARB ‘ er blokerer selektivt angiotensin II ved binding til angiotensinreceptoren. ARB ‘ er reducerer sværhedsgraden af kinin-bivirkningerne, såsom hoste og angioødem, selvom angioødem er rapporteret med disse midler. Tilføjelsen af en ARB til standardterapi inklusive en ACE-hæmmer kan reducere størrelsen på venstre ventrikel og antallet af indlæggelser, men bevis er utilstrækkelig til reduktion af dødelighed.2,8 en undersøgelse viste, at candesartan tilsat en ACE-hæmmer reducerede kardiovaskulære dødsfald.9 en anden undersøgelse af valsartan hos patienter med MIand-hjertesvigt viste imidlertid ingen fordel af valsartan og en ACE-hæmmer givet sammen sammenlignet med en ACE-hæmmer alene.10 ordination af en kombination af ACE-hæmmere, ARB ‘ er og aldosteronantagonister anbefales ikke på grund af risikoen for hyperkalæmi. ARB ‘ er forbliver et alternativ til ACE-hæmmere til behandling af hjertesvigt.2
Beta-adrenerge receptorblokkere: tre typer betablokkere har vist sig at reducere dødeligheden: metoprolol og bisoprolol med vedvarende frigivelse, som selektivt blokerer beta-1-receptorer, og carvedilol, som blokerer alfa-1 -, beta-1-og beta-2-receptorer.1,2,8 til sammenligning viste en undersøgelse, at kortvirkende metoprolol havde mindre effekt sammenlignet med carvedilol, men den anvendte metoprololdosis var lavere end den anbefalede måldosis.11 ud over standardterapi har betablokkere vist en kombineret reduktion i død og indlæggelse for hjertesvigt. Betablokkere hæmmer bivirkninger fra det sympatiske nervesystem, hvilket opvejer de negative inotrope virkninger.2 Samlet set bør betablokkere initieres i meget lave doser, titreres langsomt med mindst to ugers intervaller og ikke brat trækkes tilbage på grund af risikoen for forværring af hjertesvigt og akut dekompensation.1,2
aldosteronantagonister: aldosteronantagonister blokerer aldosteronreceptoren i nefronens distale tubule, hvilket resulterer i kaliumretention, natriumudskillelse og mild diurese. Aldosteronantagonister anbefales til patienter med moderat svær eller svær hjertesvigt og nylig dekompensation eller hos patienter med venstre ventrikulær dysfunktion kort efter en MI.2 Når lavdosis spironolacton blev tilsat til en ACE-hæmmer hos patienter med NYHA klasse III og IV hjertesvigt, oplevede patienterne en 30% reduktion i dødelighed af alle årsager.12 En anden undersøgelse viste, at eplerenon førte til en reduktion i dødelighed hos patienter med LVEF mindre end 40% inden for 14 dage efter MI, skønt der ikke er data om brugen af eplerenon til behandling af hjertesvigt relateret til andre årsager end MI.13 den mest fremtrædende begrænsende faktor for aldosteronantagonister er potentielt livstruende hyperkalæmi.2,14 hyperkalæmi øges gradvist, når serumkreatinin overstiger 1,6 mg/dL, selvom undersøgelser har undersøgt aldosteronantagonister hos patienter med serumkreatinin på entry level på 2,0 til 2,5 mg/dl. Derudover bør aldosteronantagonister undgås hos patienter med serumkalium større end 5,0 mekv pr.2
Digoksin: digoksin er et hjerteglykosid, der virker for at øge hjertets kontraktilitet ved at hæmme natrium-kaliumadenosintriphosphatase (ATPase) pumpen, hvilket øger intracellulært calcium. DIGOKSIN anbefales til symptomatisk kontrol hos patienter med mild til moderat hjertesvigt NYHA klasse II eller III.2 i en post hoc-analyse reducerede digoksinserumkoncentrationer mellem 0,5 og 0,9 ng/mL indlæggelser; koncentrationer større end 1 ng/mL var imidlertid forbundet med en tendens mod øget dødelighed sammenlignet med placebo.15 mens undersøgelser ikke har vist, at digoksin reducerer dødeligheden, kan dette middel forbedre symptomer og udøve intolerance, reducere indlæggelser og forbedre den generelle livskvalitet.2,8,16
Vasodilatorkombination: Anbefalingen af isosorbiddinitrat (ISDN) i kombination er forbeholdt patienter, der har vist manglende evne til at tolerere en ACE-hæmmer eller ARB. I en nylig undersøgelse, der involverede en kohorte af afroamerikanske patienter med symptomatisk NYHA III eller IV hjertesvigt, førte tilsætningen af ISDN-kombination til standardbehandling (dvs.ACE-hæmmer, diuretikum og beta-blokker) til en 43% forbedring i overlevelse og en 33% reduktion i risikoen for den første indlæggelse versus placebo.17 i teorien kan kombinationen af hydral og ISDN øge biotilgængeligheden af salpetersyre.2 kombinationen ISDN og BiDil er FDA kun godkendt til afroamerikanere som supplerende terapi til standard hjertesvigt terapi.18 er en arteriol vasodilator, som virker til at mindske afterload, mens ISDN er en venøs vasodilator, som virker til at mindske forspændingen. Denne kombination af vasodilatorer foretrækkes ikke frem for ACE-hæmmere eller ARB ‘ er, da det kan have utålelige bivirkninger såsom hovedpine eller svimmelhed og overholdelsesproblemer såsom ubesvarede doser, men det kan bruges som en supplerende terapi til den afroamerikanske befolkning.2
Alternative lægemidler: hagtorn blade med blomster, også kendt som Crataegus ekstrakt, er blevet anbefalet for mild hjertesvigt (NYHA II). Gennem in vitro-undersøgelser har hagtornsblade vist positive inotrope virkninger, vasodilaterende egenskaber og øget koronar blodgennemstrømning. Undersøgelser har vist forbedring af subjektive symptomer hos patienter med mild hjertesvigt. På grund af de digitalislignende virkninger bør patienter, der tager både Crataegus-ekstrakt og digitalis, overvåges nøje. Bivirkninger rapporteret var gastrointestinale symptomer, hjertebanken, brystsmerter og svimmelhed.19,20
en anden alternativ medicin, der er blevet brugt til behandling af hjertesvigt, er coenysme 10.kvartal, et fedtopløseligt vitamin. Nogle undersøgelser viste, at coensym 10.kvartal førte til forbedring af hyppigheden af indlæggelser, dyspnø og ødem.21 imidlertid viste et randomiseret, dobbeltblindet, placebokontrolleret forsøg ingen forskel mellem coenysme 10.kvartal og placebo i LVEF, træningstolerance eller maksimalt iltforbrug hos patienter med hjertesvigt.22 dokumenterede bivirkninger af 10. kvartal var gastrointestinalt ubehag, hypoglykæmi og hypotension.21 kliniske kontrollerede forsøg med crataegusekstrakt og coenysme 10. kvartal er i gang for at evaluere effektiviteten og sikkerheden ved behandling af hjertesvigt.20,21
skadelige medicin i hjertesvigt
flere klasser af medicin kan forværre hjertesvigt og bør undgås. Antiarytmiske midler, undtagen amiodaron eller dofetilid, kan forårsage en kardiodepressiv og proarytmisk virkning på hjertet, hvilket fører til akut dekompensation.1,2 første generations calciumkanalblokkere har været forbundet med øgede kardiovaskulære hændelser og forværring af hjertesvigt. De nyere, langtidsvirkende calciumkanalblokkere amlodipin og felodipin synes at være sikre, men ingen undersøgelser har vist en statistisk signifikant reduktion i mortalitet.2,8,23 thiasolidinedionerne har været forbundet med vægtøgning og væskeretention, hvilket muligvis har ført til hjertesvigt eller udfældet en akut hjerteinsufficiens-eksacerbation. Det er dog mere sandsynligt, at ødem forekommer, når thiasolidinedioner anvendes i kombination med insulinbehandling.24,25 således anbefales ikke til patienter med diabetes mellitus og NYHA klasse III eller IV hjertesvigt.25-27 NSAID ‘ er forårsager natriumretention og perifer vasokonstriktion, hvilket udfælder en akut hjerteinsufficiens forværring. Derudover mindsker de effekten og øger risikoen for toksicitet fra ACE-hæmmere og diuretika. Der er mulighed for lægemiddelinteraktion, når aspirin anvendes i kombination med ACE-hæmmere, men det forbliver kontroversielt og kræver yderligere undersøgelse.2
farmaceutens rolle
en forståelse af fordelene ved lægemiddelterapi ved hjertesvigt kan føre til optimal farmaceutisk pleje. Apotekere kan hjælpe patienter med at identificere og lindre højrisikoadfærd som rygning, alkoholforbrug og ulovlig og skadelig OTC-stofbrug. Derudover skal apotekere overvåge patienter for sygdomstilstandsprogression, herunder tegn og symptomer på hjertesvigt, og opfordre patienter til at kortlægge deres vægt.
at tilskynde patienter til at overholde diætbegrænsninger, træningsretningslinjer og medicinregimer for hjertesvigt bør være apotekets prioritet. Nonadherence til terapeutiske lægemidler har været forbundet med en stigning i dødelighed og kan være relateret til negative bivirkninger af medicin. Apotekere bør overvåge og tilskynde patienter til at overholde deres medicin for at reducere dødeligheden. Ved at overvåge og uddanne patienter og andre sundhedspersonale om narkotikarelaterede bivirkninger kan apotekere bidrage til at øge medicinoverensstemmelsen. Desuden skal apotekere være opmærksomme på alternativer til medicin såsom ACE-hæmmere og diskutere med andre sundhedsudbydere fordelene ved dødelighed forbundet med dem for at yde optimal farmaceutisk pleje og reducere risikoen for dødelighed.
patienter og sundhedsudbydere er muligvis ikke opmærksomme på sammenhængen mellem almindelig medicin og forværringer af hjertesvigt. Da nogle almindelige OTC-medicin, herunder NSAID ‘ er, er kontraindiceret hos patienter med hjertesvigt, er det en anden vigtig rolle for farmaceuter at uddanne patienten om, hvorfor han eller hun ikke bør tage disse lægemidler. Apotekere er nødt til at overvåge patienter for og konsultere sundhedsudbydere og patienter om skadelige lægemiddel-og lægemiddel-sygdomsinteraktioner, der kan resultere i indlæggelse.
1. Klein L, O ‘ Connor CM, Gattis et al. Farmakologisk behandling til patienter med kronisk hjertesvigt og nedsat systolisk funktion: gennemgang af forsøg og praktiske overvejelser. Am J Cardiol. 2003; 91 (suppl): 18F-40F.
2. Hunt SA, Abraham MT, Chin MH, et al. ACC/AHA 2005 retningslinje opdatering til diagnose og håndtering af kronisk hjertesvigt hos voksne: en rapport fra American College of Cardiology / American Heart Association Task Force om retningslinjer for praksis (Skriveudvalg til opdatering af 2001-retningslinjerne for evaluering og styring af hjertesvigt). American College of Cardiology hjemmeside. Tilgængelig på: www.acc.org/clinical/guidelines/failure//index.pdf.
3. Francis GS, Gassler JP, Sonnenblick EH. Patofysiologi og diagnose af hjertesvigt. I: Fuster V, et al, eds. Hurst er hjertet. 10. udgave. 2001: 655-686.
4. Dei Cas L, Metra M, Nodari s, et al. Forebyggelse og håndtering af kronisk hjertesvigt hos patienter i fare. Am J Cardiol. 2003; 91 (suppl): 10F-17F.
5. Chobanian AV, Bakris GL, Black HR, et al. Syvende rapport fra Det Blandede Nationale Udvalg for forebyggelse, påvisning, evaluering og behandling af forhøjet blodtryk. Hypertension. 2003;42:1206-1252.
6. Frigerio M, Oliva F, Danmark, Danmark. Forebyggelse og håndtering af kronisk hjertesvigt ved behandling af asymptomatiske patienter. Am J Cardiol. 2003; 91 (suppl): 4F-9F.
7. Colonna P, Sorino M, D ‘ Agostino C, et al. Ikke-farmakologisk pleje af hjertesvigt: rådgivning, diætbegrænsning, rehabilitering, behandling af søvnapnø og ultrafiltrering. Am J Cardiol. 2003; 91 (suppl): 41F-50F.
8. McConaghy JR, Smith SR. ambulant behandling af systolisk hjertesvigt. Am Fam Læge. 2004;70:2157-2164.
9. Young JB, Dunlap mig, Pfeffer MA, et al. Mortalitet og morbiditetsreduktion med candesartan hos patienter med kronisk hjertesvigt og venstre ventrikulær systolisk dysfunktion: resultater af charm lav-venstre ventrikulær udstødningsfraktion forsøg. Omløb. 2004;110:2618-2626.
10. Cohn JN, Tognoni G. et randomiseret forsøg med angiotensin-receptorblokker valsartan ved kronisk hjertesvigt. N Engl J Med. 2001;345:1667-1675.
11. K, Cleland JG, et al. Sammenligning af carvedilol og metoprolol på kliniske resultater hos patienter med kronisk hjertesvigt i Carvedilol eller metoprolol europæisk forsøg (COMET): randomiseret kontrolleret forsøg. Lancet. 2003;362:7-13.
12. Pitt B, Sannad F, Remme VJ, et al. Virkningen af spironolacton på sygelighed og dødelighed hos patienter med svær hjertesvigt. N Engl J Med. 1999;341:709-717.
13. Pitt B, Remme B, Sannad F, et al. Eplerenon, en selektiv aldosteronblokker, hos patienter med venstre ventrikulær dysfunktion efter myokardieinfarkt. N Engl J Med. 2003;348:1309-1321.
14. Aldactone . Chicago, IL: Pharmacia Corporation; juli 2003.
15. Ahmed A, rig mv, elsker TE, et al. Digoksin og reduktion i dødelighed og hospitalsindlæggelse ved hjertesvigt: en omfattende post hoc-analyse af DIG-forsøget. Eur Hjerte J. 2006; 27: 178-186.
16. Digitalis Investigation Group. Digoksin effekt på dødelighed og sygelighed hos patienter med hjertesvigt. N Engl J Med. 1997;336:525-533.
17. Taylor AL, s, Yancy C, et al. Kombination af isosorbiddinitrat og hydralasin hos sorte med hjertesvigt. N Engl J Med. 2004;351:2049-2057.
18. BiDil . København, MA: Nitromed Inc.; August 2005.
19. De Smet PA. Naturlægemidler. N Engl J Med. 2002;347:2045-2056.
20. Holubarsch CJ, Colucci, Meinert T, et al. Overlevelse og prognose: undersøgelse af Crataegus ekstrakt vs 1442 i kongestiv hjertesvigt(SPICE) – begrundelse, studiedesign og studieprotokol. Eur J Hjertesvigt. 2000;2:431-437.
21. Bonadkar RA, Guarneri E. Coensyme 10.kvartal. Am Fam Læge. 2005;72:1065-1070.
22. Khatta M, Aleksandr BS, Krichten CM, et al. Effekten af coenysme 10. kvartal hos patienter med kongestiv hjertesvigt. Ann Praktikant Med. 2000;132:636-640.
23. De Vries RJM, van Veldhuisen DJ, Dunselman PHJM. Effektivitet og sikkerhed af calciumkanalblokkere ved hjertesvigt: fokus på nylige forsøg med anden generation af dihydropyridiner. Am Hjerte J. 2000;139:185-194.
24. Delea TE, Edelsberg JS, Hagivara M, et al. Risiko for hjertesvigt hos mennesker med type 2-diabetes. Diabetes Pleje. 2003;26:2983-2989.
25. Hollenberg NK. Overvejelser til styring af væskedynamiske problemer forbundet med thiasolidinedioner. Am J Med. 2003; 115: 111S-115S.
26. Avandia . Forskning Triangle Park, NC: Glasosmithkline; August 2005.
27. Actos . Lincolnshire, IL: Takeda Pharmaceutical American Inc.; August 2004.
for at kommentere denne artikel, kontakt [email protected].