prostaglandiineilla on monenlaisia biologisia vaikutuksia, ja niiden vaikutus on mitä erilaisimpia luonnossa esiintyvistä yhdisteistä. Tästä havainnosta huolimatta tällä lipidien ryhmällä on huomattava rakenne-aktiivisuusspesifisyys, joka määräytyy pääasiassa syklopentanonirengassubstituutioiden ja prostaanihapon sivuketjujen epätyydyttävyysasteen perusteella. Prostaglandiinien soluvaste välittyy niiden yhteisvaikutuksesta plasman kalvoreseptoreihin.
PG-reseptorit luokiteltiin aluksi luonnollisten ja synteettisten agonistien toiminnallisten aktiviteettien perusteella, ja antagonistit luokiteltiin seuraaviin luokkiin: DP, EP, FP, IP ja TP. Ensimmäinen kirjain merkitsee prostaglandiinityyppiä, ja kirjain P tarkoittaa ”prostanoidia.”30 myöhemmin tutkimukset sitomisanalyysin ja molekyylikloonauksen avulla vahvistivat erillisten reseptorityyppien sekä kolmen tai neljän EP: n alatyypin (EP1–4) olemassaolon. Plasmakalvon prostaglandiinireseptorit kuuluvat G-proteiinikytkentäisten reseptorien superperheeseen, jolle on ominaista seitsemän transmembraanipitoista aluetta.31 prostaglandiinireseptorien solunsisäisiin toisiin sanansaattajiin kuuluvat cAMP, proteiinikinaasi C ja kalsium.30,31 eri reseptorit osoittavat huomattavaa spesifisyyttä eikosanoidille, ja ligandia suositaan vähintään 100-kertaisesti. Suurina pitoisuuksina PGE2 ja pgf2a vuorovaikuttavat DP-reseptorin kanssa; vastaavasti PGF2A aktivoi EP-reseptorin, kun taas PGD2 ja PGE2 vuorovaikuttavat FP-reseptorin kanssa suurina pitoisuuksina. Useimmat kudokset sisältävät reseptorien sekoitusta, joka näyttää olevan perustana tietyn prostaglandiinin usein vastakkaisille vaikutuksille eri annoksilla.
prostaglandiinien rooli gonadotropiinin erityksessä
on julkaistu tuoreita tietoja, jotka viittaavat prostaglandiinien fysiologiseen rooliin gonadotropiinia vapauttavan hormonin (GnRH) erityksen säätelyssä.32,33 useat raportit viittaavat nyt siihen, että prostaglandiinit,erityisesti PGE2, aiheuttavat stimuloivia vaikutuksia gonadotropiinin vapautumiseen, vaikutus, joka näyttää välittyvän hypotalamuksen tasolla. PGE2: n on osoitettu stimuloivan GnRH: n vapautumista hypotalamuksesta, ja eläinten esikäsittely antiseerumilla endogeenisen GnRH: n neutraloimiseksi estää PGE2: n aiheuttaman LH: n vapautumisen.Lisäksi PGE1 ja PGE2 näyttävät olevan voimakkaimpia kasvuhormonin vapautumisen stimulaattoreita viljellyistä adenohypofyseaalisoluista.35 PGB, PGA1, PGA2, PGB2, PGF1 ja pgf2 ovat myös aktiivisia stimulaattoreita, mutta niiden vaikutuksia ei havaita fysiologisilla annoksilla. Yleensä prostaglandiinit eivät näytä stimuloivan gonadotropiinin eritystä suoralla vaikutuksella aivolisäkkeeseen.
lisää näyttöä siitä, että prostaglandiinit saattavat vaikuttaa gonadotropiinin eritykseen (vaikuttamalla suoraan hypotalamukseen), saadaan tutkimuksista, joissa käytetään prostaglandiinisyntetaasin estäjiä, kuten indometasiinia, joka ilmeisesti vähentää gonadotropiinin eritystä.36 prostaglandiinien vaikutus hypotalamusta vapauttavien tekijöiden kautta ilmenee kahden havainnon perusteella:
- naaras-ja urosrottien esikäsittely antiseerumilla LH: ta vapauttavalle hormonille (LHRH) heikensi PGE2: n (100 mg / rotta) kykyä lisätä LH: n eritystä.36
- PGE2: n suora anto rotan aivojen kammioon jäljitteli prostaglandiinien suonensisäistä vaikutusta gonadotropiinin erityksen stimulointiin.36
Lisähavainnot tukevat vakuuttavasti käsitystä, jonka mukaan PGE2: n vaikutus on LHRH: n vapautumisen mediaanitasolla. Tätä väitettä tukee myös havainto, jonka mukaan mediaani-eminenssikudos sisältää suurempia määriä endogeenisiä prostaglandiineja kuin hypotalamuksen tyvialueet. Urosrottien in vitro-inkubaatioista saadut tiedot osoittavat, että noradrenaliini ja dopamiini stimuloivat LHRH: n ja PGF2a: n samanaikaista vapautumista. Indometasiini estää tämän vaikutuksen, mikä viittaa siihen, että intraneuronaalisesti tuotetut prostaglandiinit ovat katekoliamiinin stimuloiman LHRH: n vapautumisen välittäjiä. Näitä mielenkiintoisia havaintoja käsitellään yksityiskohtaisemmin Ojedan ja työtovereiden tekemässä katsauksessa.
ovulaatio ja prostaglandiinit
sen jälkeen kun havaittiin,että indometasiini ja asetyylisalisyylihappo (prostaglandiinisynteesin estäjät) voivat estää ovulaation,33, 37 prostaglandiinit osallistuivat munasarjojen follikulaarisen repeämisprosessiin. Tätä väitettä vahvisti entisestään havainto, että myös pgf2a-antiseerumin intraovaarinen ruiskutus esti ovulaatiota.38 nyt on olemassa huomattava määrä näyttöä siitä, että follikulaarinen prostaglandiinin muodostuminen on lisääntynyt ovulaation aikana ja että tämä nousu on riippuvainen gonadotropiineista.
gonadotropiinien keskijakso stimuloi follikulaarista eikosanoidibiosynteesiä cAMP-välitteisellä prosessilla, joka on riippuvainen geenien aktivaatiosta, mutta riippumaton steroidogeneesistä. LH näyttää olevan hallitseva fysiologinen aivolisäkkeen gonadotropiini vastuussa ovulaation induktiosta, ja näyttää todennäköiseltä, että LH: n vaikutukset follikkelin repeämään voivat välittyä leukosyyteiltä, jotka erittävät proteolyyttisiä entsyymejä, happiradikaaleja ja prostaglandiineja. Indometasiini, esimerkiksi, estää ovulaation normaalisti indusoi suuret annokset koriongonadotropiinia in vivo. Prostaglandiinit saattavat välittää LH: n stimuloivia vaikutuksia ”ovulatorisiin entsyymeihin”, kuten proteaasi-tai kollagenaasiin.Prostaglandiinit saattavat myös aiheuttaa supistuvan vasteen follikkelin seinämässä,41 jonka tiedetään nyt sisältävän supistuvia elementtejä, kuten myosiinia ja aktiinia. Plasminogeeniaktivaattori tai jokin muu proteaasi vaikuttaa osallistuvan olennaisesti follikkelin repeämiseen,42 ja on ilmeistä, että tämän proteiinin eritys liittyy LH: n aiheuttamaan follikulaarisen prostaglandiinin biosynteesin lisääntymiseen, vaikka on osoitettu, että nämä kaksi tapahtumaa eivät välttämättä ole toisistaan riippuvaisia. Prostaglandiinin mahdollinen vaikutusmekanismi follikkelin repeämässä on esitetty kuvassa 6.
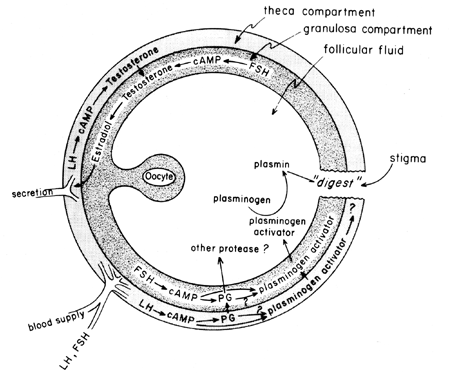 Kuva. 6. Prostaglandiinin mahdollinen vaikutusmekanismi follikkelin repeämässä.(Behrman HR: prostaglandiinit hypotalamo-aivolisäkkeen ja munasarjojen toiminnassa. Ann Rev Physiol 41:685, 1979)
Kuva. 6. Prostaglandiinin mahdollinen vaikutusmekanismi follikkelin repeämässä.(Behrman HR: prostaglandiinit hypotalamo-aivolisäkkeen ja munasarjojen toiminnassa. Ann Rev Physiol 41:685, 1979)
prostaglandiinien rooli Luteaalitoiminnassa: Luteolyysi ja kuukautiset
mekanismi, jolla ihmisen keltarauhanen taantuu 10-12 päivän kuluttua sen muodostumisesta, on mysteeri. Sen jälkeen,kun rotalla ja monilla muilla alalajeilla havaittiin varhain, että pgf2a oli luteolyyttistä, 43 on pgf2a: lla tehty suuri tutkimus kuukautisten säätelymahdollisuuden selvittämiseksi.PGF2a indusoi keltarauhasen funktionaalista regressiota reseptorivälitteisellä prosessilla, joka on riippumaton aluksi munasarjojen tai luteaalisen verenkierron muutoksista.32 minuutin kuluessa pgf2a kuluttaa askorbiinihappoa, 44 irrottaa miehitetyn LH-reseptorin adenylaattisyklaasista ja vähentää gonadotropiinin kuljetusta hiussuonista luteaalisoluun.
asiaa koskevan kirjallisuuden tarkastelu paljastaa monia ristiriitaisia raportteja PGF2a: n vaikutuksista ihmisiin. Joissakin tutkimuksissa on havaittu ohimenevää vähenemistä verenkierrossa pgf2a: n progesteronipitoisuuksissa, 45, vaikka muissa tutkimuksissa tällaista vaikutusta ei ole pystytty osoittamaan normaalisti ovuloivilla naisilla.Koska ihmisen keltarauhasessa on pgf2a-reseptoreita, 48 katsottiin, että luteolyysin epäonnistuminen laskimonsisäisillä pgf2a-infuusioilla saattoi johtua nopeasta keuhkoaineenvaihdunnasta. Myöhemmät tutkimukset, joissa pgf2a: ta ruiskutettiin suoraan ihmisen keltarauhaseen, indusoivat progesteronin vieroitusoireita, joiden pohjalukema sattui samaan aikaan varhaisten kuukautisten alkamisen kanssa.Nämä löydökset viittaavat siihen, että endogeenisiä munasarjojen prostaglandiineja (tai jotain muuta luteolyyttistä ainetta) saatetaan tarvita luteaalisen regression aikaansaamiseksi. Tämä vaikuttaa mahdolliselta, kun otetaan huomioon havainto, että ihmisen luteaalitoiminta näyttää olevan riippumaton kohdun kontrollista, sillä hysterektomia 50 tai kohdun, emättimen tai munanjohtimien synnynnäinen puuttuminen ei vaikuta munasarjojen syklisyyteen.51 ihmisen luteaalikudos pystyy varmasti tuottamaan prostaglandiineja, kuten in vitro-kokeet52 osoittavat; kuitenkin yritykset korreloida lisääntynyt pgf2a-taso munasarjoissa luteaalisen regression kanssa myöhäisessä luteaalivaiheessa eivät ole onnistuneet.53 näyttää siltä, että ainoa kerta munasarjojen pgf2a tuotanto tehostuu ihmisen kuukautiskierto on pian ovulaation jälkeen.54 on kuitenkin myös ilmeistä, että pgf2a: n pitoisuudet ovat aina korkeammat munasarjojen stroomakudoksessa varhaisvaiheen, keskivaiheen ja myöhäisen luteaalivaiheen aikana.
toisin kuin PGF2a: n in vivo-vaikutukset, in vitro-tutkimukset ovat osoittaneet sekä ohimeneviä että pitkäkestoisia luteolyyttisiä vaikutuksia ihmisen luteaalikudoksessa.55, 56, 57 yleisen käsityksen mukaan varhainen tapahtuma pgf2a: n aiheuttamassa luteolyysissä on rotan keltarauhasessa tehdyistä tutkimuksista saatu gonadotropiiniherkän cAMP-tuotannon kumoaminen.58, 59 tämä kumoutuminen tapahtuu todennäköisesti adenyylisyklaasin suoran eston kautta, jolloin solunsisäinen Ca2+ – pitoisuus kasvaa.60 neurotieteen alalta saadut viimeaikaiset todisteet osoittavat, että prostaglandiinit stimuloivat solunsisäisen Ca2+: n vapautumista lisäämällä fosfoinositolin hydrolyysiä diasyyliglyseroliksi ja inositolitrifosfaatiksi.Koe-eläimillä tehtyjen havaintojen mukaisesti osoitettiin, että myös ihmisen keltarauhasen taantuminen liittyy LH-reseptorien häviämiseen.62
tiedetään hyvin, että monien lajien vastamuodostunut keltarauhanen ei reagoi PGF2a63: n lyyttiseen vaikutukseen; tämä havainto näyttää ulottuvan myös ihmisen keltarauhaseen.64 Henderson ja McNatty65 ehdottivat, että juuri muodostuneen keltarauhasen pgf2a-reseptorit saattavat jotenkin peittyä käytössä olevien LH-reseptorien alle ja että LH: n asteittainen irtautuminen reseptoristaan voi lisätä keltarauhasen alttiutta pgf2a: lle. Vaihtoehtoisen hypoteesin tarjosivat toiset tutkijat, 65, joiden mukaan ihmisen keltarauhasen alttius PGF2a: lle voi riippua munasarjojen noradrenaliinitasoista, jotka nousevat luteaalivaiheen aikana. Katekoliamiinien lisääntyminen näyttää mahdollistavan pgf2a: n antigonadotrooppisen vaikutuksen ihmisen keltarauhaseen.
prostaglandiinit kohdussa
toisin kuin myometrium, joka tuottaa pääasiassa SMM2: ta, raskauden ulkopuolinen endometrium tuottaa pääasiassa pgf2a: ta ja PGE2: ta. Prostaglandiinien synteesi on suurempi rauhasepiteelissä kuin kohdun limakalvon stroomassa ja eritysvaiheessa kuin syklin proliferatiivisessa vaiheessa.67, 68 sekä pgf2a: n että PGE2: n tiedetään stimuloivan myometriaalista supistumiskykyä, mikä johtaa solunsisäisen Ca2+: n lisääntymiseen. Tällainen prostaglandiinin aiheuttama kohdun hyperkontractilitymekanismi on yhdistetty primaarisen dysmenorrean patogeneesiin. Dysmenorreaa sairastavien naisten endometriumissa ja kuukautisnesteessä on havaittu kohonneita pgf2a-ja PGE2-pitoisuuksia, ja antiprostaglandiinilääkkeiden on osoitettu vähentävän huomattavasti kipua näillä potilailla.
kohdun kohdunkaulassa tuotetaan myös erilaisia prostaglandiineja, ja kohdunkaulassa on sekä PGE: n että PGF: n reseptoripaikkoja.Prostaglandiinien tai niiden paikallisen annostelun lisääntyminen liittyy raskaana olevien naisten kohdunkaulan kypsymiseen.69
prostaglandiinit ja synnytys
useat havainnot viittaavat epäsuorasti prostaglandiinien osallisuuteen synnytykseen. Tiedetään esimerkiksi, että indometasiinin tai muiden steroideihin kuulumattomien tulehduskipulääkkeiden, kuten aspiriinin, antaminen pidentää raskausaikaa.Lisäksi prostaglandiinien, erityisesti PGF2a: n, tiedetään stimuloivan voimakkaasti kohdun supistumiskykyä ja aiheuttavan gravid-kohdun syklisiä supistuksia. Kohonneet prostaglandiinipitoisuudet ovat yhteydessä spontaanin synnytyksen käynnistymiseen ihmisillä. Supistusten alkamista edeltävälle ajanjaksolle on lisäksi ominaista plasman pgf2a-pitoisuudet, jotka vastaavat raskaana olevien naisten pitoisuuksia. Rokotus PGF2a: ta vastaan viivästyttää myös synnytyksen alkamista.70 prostaglandiinit käytetään nyt indusoimaan varhaisen työvoiman ja abortin; todellakin, prostaglandiini on lääke valinta toteutettaessa midtrimester abortteja.69,71
lampailla tehtyjen laajojen tutkimusten perusteella näyttää siltä, että paikallisesti kohdussa syntetisoidut prostaglandiinit käynnistävät synnytyksen vaikuttamalla suoraan myometriumiin kohdun supistusten edistämiseksi. Paikallisen, istukan progesteronin väheneminen yhdistettynä estrogeenin lisääntymiseen johtaa Ca2+: n vapautumiseen lysosomeista, jotka ovat haurastuneet. Tämä Ca2+ – vapautus stimuloi prostaglandiinisynteesiä lisäämällä fosfolipaasiaktiivisuutta. Oksitosiini näyttää pikemminkin helpottavan kuin käynnistävän estrogeeni-ja progesteronivaikutuksia.72 sikiökalvot, decidua vera ja myometrium voivat kaikki osallistua prostaglandiinien muodostumiseen.73,74
tuore ehdotus on, että kohdunsisäisen kudoksen aiheuttama prostaglandiinituotanto estyy tonaalisesti ihmisen raskauden aikana ja että tällainen esto poistuu asteittain termillä lähestyttäessä. Vaikka prostaglandiinisynteesin tonic-inhibitiota aiheuttavia mekanismeja ei ole vahvistettu, ihmisen istukasta, amnionista,75: stä ja korionista on löydetty useita fosfolipaasipeptidejä.76 toinen mahdollisuus on, että prostaglandiinisynteesiä stimuloidaan samanaikaisesti synteesin eston poistamisen kanssa. Prostaglandiinien lisääntyneen synteesin mahdollisia signaaleja ovat useat kasvutekijät ja verihiutaleita aktivoiva tekijä. Sikiön keuhko-ja munuaiskudokset erittävät verihiutaleita aktivoivaa tekijää, joka kykenee stimuloimaan prostaglandiinituotantoa ihmisen amnionin avulla.77
prostaglandiinit ja valtimotiehyt
valtimotiehyen avoimuuden ylläpitäminen (vasodilataation relaksaatio) on keskeistä sikiön kudosten hapetuksen säätelyssä. Syntymän jälkeen valtimotiehyt normaalisti supistuu tai menettää avuttomuutensa. Mekanismi, jolla tämä sulkeutuminen tapahtuu, on epäselvä, vaikka veren happijännityksen uskotaan olevan tärkeä tekijä (Fig. 7). Sikiön valtimotiehyen ensisijainen tehtävä on pitää yllä jonkinasteista vasemmalta oikealle kulkevaa valtimoverenkiertoa, jolloin keuhkoihin palaavien laskimoiden määrä saadaan hallintaan. Valtimotiehyen sulkeutuminen on tärkeä fysiologinen prosessi, joka epätäydellisenä johtaa hengitysvaikeuksiin ja syanoosiin/hypoksiaan—oireyhtymiin, jotka ovat syynä suureen sairastuvuuteen ja kuolleisuuteen monilla avoimesta valtimotiehytestä kärsivillä keskosilla. Tästä syystä ductus arteriosuksen toiminnan säätelymekanismi (- mekanismit) herättää paljon kiinnostusta. Kiinnostus kohdistuu erityisesti prostaglandiinitutkimukseen, jossa on nyt huomattava määrä näyttöä prostaglandiinien osallistumisesta valtimotiehyiden avoimuuden säätelyyn pitkällä aikavälillä.
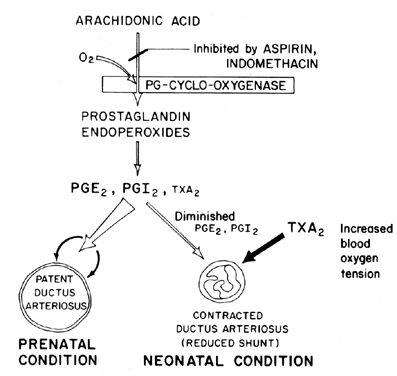 Kuva. 7. Scheme for prostaglandin modulation of patency of ductus arteriosus in fetus and neonate as a function of oxygen tension.
Kuva. 7. Scheme for prostaglandin modulation of patency of ductus arteriosus in fetus and neonate as a function of oxygen tension.
tämä näyttö perustuu seuraaviin havaintosarjoihin:
sikiön valtimotiehyt voidaan sulkea antamalla prostaglandiinisyntetaasin estäjiä.78
indometasiini voi aiheuttaa hypoksisen verisuonen supistumista, minkä osoittavat sen vaikutukset eläimiin lähiaikoina.
PGE2: n (ja PGE1: n) antaminen aiheuttaa eristettyjen karitsan valtimotiehyiden (pyöreiden suikaleiden) relaksaation (avoimuuden menetyksen) vähähappisessa ympäristössä (PO2 alle 14 mmHg).80
näyttää todennäköiseltä, että E-sarjan prostaglandiinit yhdessä prostaglandiiniantagonistien ja prostaglandiinisyntetaasinestäjien (aspiriini) kanssa voivat osoittautua toivottaviksi nonurgisiksi hoidoiksi keskosille, joilla on mahdollisesti tappava valtimotiehyt. Viimeaikaiset todisteet viittaavat tasapainoon valtimotiehyen ja supistumisen välillä, jota ylläpitää laajentuvien prostaglandiinien (SMM2 ja PGE2) ja supistuvien prostaglandiinien (txa2) synteesi. Karitsan sikiössä sekä valtimotiehyt että keuhko syntetisoivat smmi2: ta ja PGE2: ta; sitten, kun termi lähestyy, keuhko siirtyy kohti TXA2 synteesi.81 lisätietoa prostaglandiinin osallistumisesta valtimotiehyeen kontrollointiin on saatavilla.82