プロスタグランジンは幅広い生物学的効果を示し、その作用は天然に存在する化合物の中で最も多様 この観察にもかかわらず、脂質のこのグループは、シクロペンタノン環置換とプロスタン酸側鎖の不飽和の程度によって主に決定される顕著な構造活 プロスタグランジンに対する細胞応答は、原形質膜受容体との相互作用によって媒介される。
PG受容体は、当初、天然および合成アゴニストの機能活性に基づいて分類され、拮抗薬は、DP、EP、FP、IP、およびTPのカテゴリに分類された。 最初の文字はプロスタグランジン型を示し、文字Pは”プロスタノイド”を表します。”30後、結合分析および分子クローニングによる研究は、異なる受容体タイプならびにEP(EP1–4)の三つまたは四つのサブタイプの存在を確認した。 原形質膜プロスタグランジン受容体は、七つの膜貫通領域によって特徴付けられるGタンパク質共役受容体のスーパーファミリーに属しています。プロスタグランジン受容体の31細胞内第二メッセンジャーには、cAMP、プロテインキナーゼC、カルシウムが含まれる。30,31様々な受容体は、リガンドのための少なくとも100倍の好みで、エイコサノイドのための顕著な特異性を示しています。 高濃度では、PGE2およびPgf2AはDP受容体と相互作用する;同様に、PGF2AはEP受容体を活性化するが、PGD2およびPGE2は高濃度でFP受容体と相互作用する。 ほとんどのティッシュは異なった線量に特定のプロスタグランジンの頻繁に反対の効果のための基礎であるようである受容器の混合物を含んで
ゴナドトロピン分泌におけるプロスタグランジンの役割
ゴナドトロピン放出ホルモン(GnRH)分泌の調節におけるプロスタグランジンの生理的32,33いくつかのレポートは今プロスタグランジン、特にPGE2が性腺刺激ホルモン解放、視床下部のレベルで行為によって仲介されるようである効果のstimulatory PGE2は視床下部からのGnRHの放出を刺激することが示されており、内因性GnRHを中和するために抗血清を用いた動物の前処理は、PGE2誘導性LHの放出を防34さらに、PGE1およびPGE2は培養されたadenohypophyseal細胞からの成長ホルモン解放の最も有効な刺激物であるようです。Pgb、Pga1、Pga2、Pgb2、PGF1、およびPGF2もまた活性刺激物質であるが、それらの効果は生理学的用量では見られない。 一般に、プロスタグランジンは下垂体の直接作用によって性腺刺激ホルモンの分泌を刺激しないようです。
プロスタグランジンが性腺刺激ホルモン分泌に(視床下部に直接作用することによって)影響する可能性があることを示唆するさらなる証拠は、インドメタシンなどのプロスタグランジン合成酵素阻害剤を用いた研究から供給されており、これは明らかに性腺刺激ホルモン分泌を減少させる。36プロスタグランジンが視床下部放出因子を介して作用することは、二つの観察に基づいて明らかである:
- lh放出ホルモン(LHRH)に対する抗血清を有する雌および雄ラットの前処理は、LH分泌を増加させるPGE2(ラットあたり100mg)の能力を障害した。36
- ラットの脳の心室へのPGE2の直接投与は、性腺刺激ホルモン分泌の刺激に対するプロスタグランジンの静脈内効果を模倣した。36
追加の知見は、PGE2がLHRHの放出を誘発するために中央値の隆起のレベルで作用するという概念の説得力のある支持を提供する。 この競合はさらに中央隆起組織が基底視床下部領域よりも内因性プロスタグランジンのより多くの量が含まれていることを発見することによ 雄ラットから得られた中央隆起断片のin vitroインキュベーションから得られたデータは、ノルエピネフリンとドーパミンがLHRHとPgf2Aの同時放出を刺激するこ この効果はインドメタシンによってブロックされ,神経内で産生されるプロスタグランジンがカテコールアミン刺激LHRH放出のメディエーターであることを示唆した。 これらの興味深い発見は、Ojedaと同僚によるレビューでより詳細に議論されています。36
排卵とプロスタグランジン
インドメタシンとアスピリン(プロスタグランジン合成阻害剤)が排卵をブロックできることが発見された後、33、37プロスタグランジンが卵巣濾胞破裂過程に関与していることが示唆された。 この競合は、Pgf2A抗血清の卵巣内注射も排卵を阻害するという発見によってさらに強化された。38今濾胞のプロスタグランジンの形成が排卵の間に高められ、この高度が性腺刺激ホルモンに依存していることを示す相当な量の証拠があります。39
ゴナドトロピンの中間サイクルサージは、遺伝子活性化に依存するが、ステロイド形成とは独立したcAMPを介したプロセスによって濾胞性エイコサノイド生合成を刺激する。 LHは排卵の誘導に責任がある支配的な生理学的な下垂体の性腺刺激ホルモンであるようで小嚢の破裂に対するLHの効果が蛋白分解酵素、酸素基およ インドメタシンは、例えば、普通人間の絨毛性ゴナドトロピンの大きい線量によって生体内で引き起こされる排卵を妨げます。 プロスタグランジンは、プロテアーゼやコラゲナーゼなどの”排卵酵素”に対するLHの刺激効果を仲介する可能性がある。40プロスタグランジンが卵胞壁に収縮応答を誘発する可能性もあり、41は現在、ミオシンやアクチンなどの収縮要素を含むことが知られている。 プラスミノーゲン活性化剤またはいくつかの他のプロテアーゼは、本質的に卵胞の破裂に関与しているように見えます,42そして、このタンパク質の分泌 濾胞破裂におけるプロスタグランジン作用の可能なメカニズムを図6に示す。
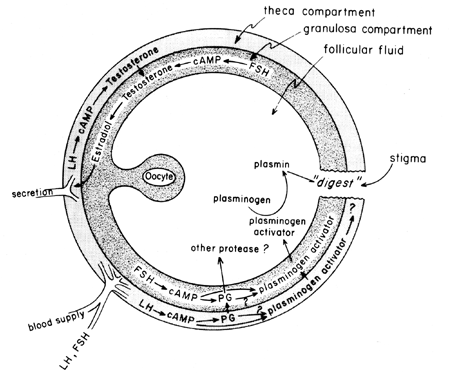 図1.1.1. 6. 濾胞破裂におけるプロスタグランジン作用の可能性のある機序。(Behrman HR:hypothalamo-pituitaryおよび卵巣機能のプロスタグランジン。 アン-レヴィジョール41:685, 1979)
図1.1.1. 6. 濾胞破裂におけるプロスタグランジン作用の可能性のある機序。(Behrman HR:hypothalamo-pituitaryおよび卵巣機能のプロスタグランジン。 アン-レヴィジョール41:685, 1979)
黄体機能におけるプロスタグランジンの役割:黄体溶解および月経
ヒト黄体が形成されてから10-12日後に退行するメカニズムは謎である。 Pgf2Aがラットおよび他の多くのsubprimate種でluteolyticだったこと早い発見以来、43主要な研究の努力はPgf2Aとのmenstrual規則の可能性を調査するためになされました。Pgf2aは、最初に卵巣または黄体血流の変化とは無関係に、受容体を介したプロセスによって黄体の機能的退行を誘導する。32分以内に、pgf2Aはアスコルビン酸を枯渇させ、44はアデニル酸シクラーゼから占有されたLH受容体を開裂し、毛細血管から黄体細胞への性腺刺激ホルモンの輸送を減少させる。
関連文献のレビューでは、ヒトにおけるPgf2Aの影響に関する多くの相反する報告が明らかになっている。 他の調査が普通排卵の女性のそのような効果を示さなかったがある調査はPgf2A、45によってプロゲステロンの循環のレベルの一時的な低下を記録46,47ヒト黄体における推定Pgf2A受容体の存在を考慮して、48Pgf2Aの静脈内注入による黄体溶解を達成することができないことは、おそらく急速な肺代謝によるものであると推論された。 ヒト黄体へのPgf2Aの直接注入を含むその後の研究は、プロゲステロンの撤退を誘発し、その天底は早期月経の発症と一致した。49これらの知見は、内因性卵巣プロスタグランジン(またはいくつかの他の黄体溶解剤)が黄体退行に必要とされ得ることを示唆している。 これは、ヒトの黄体機能が子宮制御とは独立しているように見えるという観察を考慮すると、子宮摘出術も子宮、膣、卵管の先天性不在も卵巣周期性に影響を与えないため、実現可能であると思われる。51ヒト黄体組織は、in vitro実験によって示されるように、確かにプロスタグランジンを産生することができる52;しかし、卵巣のpgf2Aレベルの増加を黄体期後期の黄体退行と相関させる試みは成功していない。53人間の月経周期で卵巣Pgf2A産生が増強される唯一の時間は、排卵直後であると思われる。しかし、Pgf2Αの濃度は、黄体期の初期、中期、および後期を通じて卵巣間質組織において常に高いこともまた明らかである。
Pgf2Aのin vivo効果とは対照的に、in vitroでの研究では、ヒト黄体組織における一過性および持続性の黄体溶解効果の両方が示されている。55,56,57pgf2A誘発性黄体溶解の初期のイベントは、ラット黄体の研究から派生した性腺刺激ホルモン感受性cAMP産生の廃止であることが一般的なコンセンサスです。58,59この廃止は、細胞内Ca2+の増加によるアデニルシクラーゼの直接阻害によるものである可能性が高い。60神経科学の分野からの最近の証拠は、プロスタグランジンがホスホイノシトールのジアシルグリセロールおよびイノシトール三リン酸への加水分解を増加させることによって細胞内Ca2+の放出を刺激することを示している。61実験動物における所見と一致して、ヒト黄体の退行はまた、LH受容体の喪失と関連していることが示された。62
多くの種の新たに形成された黄体はPgf2A63の溶解作用に難治性であることはよく知られており、この観察はヒト黄体にも及ぶようである。64HendersonとMcnatty65は、新たに形成された黄体のPgf2A受容体が何らかの形で占有されたLH受容体によってマスクされ、その受容体からのLHの徐々の解離がpgf2Aへの黄体の感受性を増加させる可能性があることを示唆した。 Pgf2Aに対するヒト黄体の感受性は、黄体期の間に増加する卵巣ノルアドレナリンレベルに依存している可能性があることを示唆する他の研究者65によって対立仮説が提供された。 カテコールアミンのこの増加は人間の体のluteumに対するPgf2Aのantigonadotropic効果を可能にするようです。66
子宮内のプロスタグランジン
主にPGI2を産生する子宮筋層とは異なり、非妊娠子宮内膜は主にPgf2AおよびPGE2を産生する。 プロスタグランジンの合成は、子宮内膜の間質よりも腺上皮において、およびサイクルの増殖期よりも分泌期においてより大きい。67,68Pgf2AおよびPGE2の両方は、特定の受容体との相互作用を介して、細胞内Ca2+の増加につながる子宮筋収縮を刺激することが知られている。 このようなプロスタグランジン誘発性子宮収縮亢進のメカニズムは、原発性月経困難症の病因に関与している。 Pgf2AおよびPGE2の上昇値はdysmenorrheaの女性のendometriumそしてmenstrual液体で識別され、antiprostaglandinの代理店はこれらの患者の苦痛のマーク付きの減少で起因するために示されて
子宮頸部でも様々なプロスタグランジンが産生され、子宮頸部にはPGEとPGFの両方の受容体部位が存在する。69プロスタグランジンの産生の増加、またはそれらの局所投与は、妊婦の子宮頸部熟成と関連している。69
プロスタグランジンと分娩
多くの観察が、分娩におけるプロスタグランジンの関与を間接的に関係させている。 例えば、インドメタシンまたはアスピリンのような他の非ステロイド性抗炎症薬の投与は、妊娠を延長することが知られている。69さらに、プロスタグランジン、特にPgf2Aは、子宮収縮の強力な刺激剤であり、重力子宮の周期的収縮を誘導することが知られている。 高いプロスタグランジンの集中は人間の自発の労働の手始めと関連付けられます。 さらに、収縮の開始に先行する期間は、非妊娠女性のものと同等の血漿Pgf2Aレベルによって特徴付けられる。 Pgf2Aに対する免疫はまた分娩の手始めを遅らせます。70のプロスタグランジンが今早い労働および中絶を引き起こすのに使用されています;全く、プロスタグランジンはmidtrimesterの中絶を達成するための選択の69,71
ヒツジの広範な研究によると、子宮内で局所的に合成されたプロスタグランジンは、子宮筋層に直接作用して子宮収縮を促進することによっ エストロゲンの増加と組み合わせた局所的な胎盤プロゲステロンの減少は、脆弱になったリソソームからのCa2+の放出をもたらす。 このCa2+リリースは、ホスホリパーゼ活性を増加させることによってプロスタグランジン合成を刺激 オキシトシンはエストロゲンおよびプロゲステロンの効果を始めるよりもむしろ促進するようです。72胎児の膜、decidua veraおよびmyometriumはすべてプロスタグランジンの形成に加わるかもしれません。73,74
最近の提案では、子宮内組織によるプロスタグランジン産生はヒト妊娠中に緊張的に阻害され、そのような阻害は用語が近づくにつれて徐々に除去されるというものである。 プロスタグランジン合成の強壮阻害に影響を与えるメカニズムは確立されていないが、いくつかの抗リン脂質ペプチドは、ヒト胎盤、羊膜、75および絨毛膜に見出されている。76もう一つの可能性はプロスタグランジンの統合が統合の阻止の取り外しと並行して刺激されることです。 プロスタグランジンの合成増加のための潜在的なシグナルは、いくつかの成長因子および血小板活性化因子である。 胎児の肺および腎臓組織は、ヒト羊膜によるプロスタグランジン産生を刺激することができる血小板活性化因子を分泌する。77
プロスタグランジンと動脈管
動脈管の開存性の維持(血管拡張の緩和)は、胎児の組織の酸素化を制御する上で極めて重要である。 出生後、動脈管は通常収縮するか、またはその開存性を失う。 この閉鎖が起こるメカニズムは不明であるが、血中酸素の張力が重要な要因であると考えられている(図2)。 7). 胎児の動脈管の主な機能は、ある程度の左から右の動脈血シャントを維持し、それによって肺への静脈還流の量を制御することである。 期間中の導管の閉鎖は、不完全であれば、動脈管開存に罹患している多くの未熟児における高い罹患率および死亡率の原因となる呼吸窮迫およびチアノーゼ/低酸素症症候群につながる重要な生理学的プロセスである。 このため、動脈管機能を制御するメカニズムにはかなりの関心があります。 この関心は、プロスタグランジン研究の分野で特に深刻であり、現在では動脈管開存性の制御にプロスタグランジンの関与を示唆するかなりの量の証拠がある。
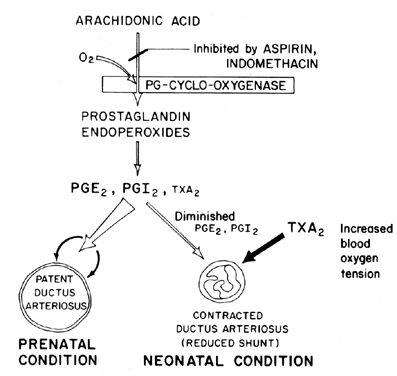 図1.1.1. 7. 酸素張力の関数としての胎児および新生児における動脈管の開存性のプロスタグランジン変調のためのスキーム。
図1.1.1. 7. 酸素張力の関数としての胎児および新生児における動脈管の開存性のプロスタグランジン変調のためのスキーム。
この証拠は、次の一連の観察に基づいています:
心肺機能低下および硝子体膜疾患を有する胎児の動脈管は、プロスタグランジン合成酵素阻害剤の投与により閉鎖することができる。78
インドメタシンは低酸素血管の収縮を誘発する可能性があり、これは近い将来の動物におけるその効果によって示される。79
PGE2(およびPGE1)の投与は、低酸素環境(PO2 14mmHg未満)で単離された胎児の子羊動脈管調製物(円形ストリップ)の弛緩(開存性の喪失)を誘導する。80
Eシリーズのプロスタグランジンは,プロスタグランジンきっ抗薬およびプロスタグランジン合成酵素遮断薬(アスピリン)とともに,潜在的に致命的な動脈管開存を有する早産児に対して望ましい非外科的治療であると考えられた。 最近の証拠は、拡張プロスタグランジン(PGI2とPGE2)と収縮プロスタグランジン(TXA2)の合成によって維持される管開存性と狭窄のバランスを示唆している。 子羊の胎児では、動脈管と肺の両方がPGI2とPGE2を合成します; その後、用語が近づくにつれて、肺はTXA2合成に向かってシフトする。81動脈管機能の制御におけるプロスタグランジンの関与に関するさらなる情報が利用可能である。82