prostaglandyny wykazują szeroki zakres efektów biologicznych,a ich działanie należy do najróżniejszych spośród naturalnie występujących związków. Pomimo tej obserwacji, ta grupa lipidów wykazuje wyraźną specyficzność strukturalno-aktywną, która jest określana głównie przez podstawienia pierścieni cyklopentanonowych i stopień nienasycenia łańcuchów bocznych kwasu prostanowego. W odpowiedzi komórkowej na prostaglandyny pośredniczy ich interakcja z receptorami błon osoczowych.
receptory PG były początkowo klasyfikowane na podstawie aktywności funkcjonalnej naturalnych i syntetycznych agonistów, a antagonistów klasyfikowano do następujących kategorii: DP, EP, FP, IP i TP. Pierwsza litera oznacza typ prostaglandyn, a litera P oznacza ” prostanoid.”30 później badania poprzez analizę wiązań i klonowanie molekularne potwierdziły obecność odrębnych typów receptorów, a także trzech lub czterech podtypów EP (EP1–4). Błonowe receptory prostaglandynowe należą do nadrodziny receptorów sprzężonych z białkiem G, charakteryzujących się siedmioma regionami przezbłonowymi.Wewnątrzkomórkowe wtórne przekaźniki receptorów prostaglandynowych obejmują cAMP, kinazę białkową C i wapń.30,31 różne receptory wykazują niezwykłą swoistość dla eikozanoidu, z co najmniej 100-krotną preferencją dla ligandu. W wysokich stężeniach PGE2 i PGF2a oddziałują z receptorem DP; podobnie PGF2a aktywuje receptor EP, podczas gdy PGD2 i PGE2 oddziałują z receptorem FP w wysokich stężeniach. Większość tkanek zawiera mieszaninę receptorów, co wydaje się być podstawą często przeciwnego działania konkretnej prostaglandyny w różnych dawkach.
rola prostaglandyn w wydzielaniu Gonadotropin
opublikowano Najnowsze dane sugerujące fizjologiczną rolę prostaglandyn w regulacji wydzielania hormonu uwalniającego gonadotropinę (GnRH).32,33 wiele doniesień sugeruje teraz, że prostaglandyny, szczególnie PGE2, wywierają stymulujący wpływ na uwalnianie gonadotropin, efekt, który wydaje się być pośredniczony przez działanie na poziomie podwzgórza. Wykazano, że PGE2 stymuluje uwalnianie GnRH z podwzgórza, a wstępne leczenie zwierząt antysurowicą w celu zneutralizowania endogennego GnRH zapobiega indukowanemu przez PGE2 uwalnianiu LH.Ponadto PGE1 i PGE2 wydają się być najsilniejszymi stymulatorami uwalniania hormonu wzrostu z hodowanych komórek adenohypophyseal.35 PGB, PGA1, PGA2, PGB2, PGF1 i PGF2 są również aktywnymi stymulatorami, ale ich działanie nie jest widoczne w dawkach fizjologicznych. Ogólnie wydaje się, że prostaglandyny nie stymulują wydzielania gonadotropin poprzez bezpośrednie działanie na przysadkę mózgową.
dalsze dowody sugerujące, że prostaglandyny mogą wpływać na wydzielanie gonadotropin (poprzez działanie bezpośrednio na podwzgórze) pochodzą z badań z zastosowaniem inhibitorów syntetazy prostaglandyn, takich jak indometacyna, które najwyraźniej zmniejszają wydzielanie gonadotropin.36 to, że prostaglandyny działają poprzez czynniki uwalniające podwzgórze, jest oczywiste na podstawie dwóch obserwacji:
- wstępne leczenie samic i samców szczurów surowicą do hormonu uwalniającego LH (LHRH) osłabiło zdolność PGE2 (100 mg na szczura) do zwiększenia wydzielania LH.36
- bezpośrednie podanie PGE2 do komory mózgu szczura naśladowało dożylne działanie prostaglandyn na stymulację wydzielania gonadotropin.36
dodatkowe ustalenia dostarczają przekonującego poparcia dla koncepcji, że PGE2 działa na poziomie mediany, aby wywołać uwolnienie LHRH. Twierdzenie to zostało dodatkowo potwierdzone przez stwierdzenie, że tkanka pośrednia Eminencji zawiera większe ilości endogennych prostaglandyn niż podstawowe obszary podwzgórzowe. Dane uzyskane z inkubacji in vitro mediany fragmentów Eminencji uzyskanych od samców szczurów wykazały, że norepinefryna i dopamina stymulują jednoczesne uwalnianie LHRH i PGF2a. Efekt ten jest blokowany przez indometacynę, co sugeruje, że wytwarzane donauronalnie prostaglandyny są mediatorami uwalniania LHRH stymulowanego katecholaminą. Te interesujące ustalenia zostały szczegółowo omówione w przeglądzie przeprowadzonym przez Ojedę i współpracowników.
owulacja i prostaglandyny
po odkryciu,że indometacyna i aspiryna (inhibitory syntezy prostaglandyn) mogą blokować owulację,33, 37 zasugerowano, że prostaglandyny biorą udział w procesie pękania pęcherzyków jajnikowych. Twierdzenie to zostało dodatkowo wzmocnione przez stwierdzenie, że wewnątrzowarstwowe wstrzyknięcie PGF2a antyserum również hamowało owulację.Obecnie istnieje znaczna ilość dowodów wskazujących na to, że tworzenie prostaglandyn pęcherzykowych jest nasilone podczas owulacji i że podwyższenie to zależy od gonadotropin.
wzrost gonadotropin w cyklu środkowym stymuluje biosyntezę eikozanoidów pęcherzykowych w procesie za pośrednictwem cAMP, który jest zależny od aktywacji genów, ale niezależny od steroidogenezy. Wydaje się, że LH jest dominującą fizjologiczną gonadotropiną przysadkową odpowiedzialną za indukcję owulacji i wydaje się prawdopodobne, że wpływ LH na pęknięcie pęcherzyków może być pośredniczony przez leukocyty, które wydzielają enzymy proteolityczne, rodniki tlenowe i prostaglandyny. Na przykład indometacyna blokuje owulację normalnie indukowaną dużymi dawkami ludzkiej gonadotropiny kosmówkowej in vivo. Prostaglandyny mogą pośredniczyć w stymulującym działaniu LH na „enzymy owulacyjne”, takie jak proteaza lub kolagenaza.Istnieje również możliwość, że prostaglandyny mogą wywoływać reakcję kurczliwą w ścianie pęcherzyka, 41 która obecnie zawiera elementy kurczliwe, takie jak miozyna i aktyna. Wydaje się,że aktywator plazminogenu lub inna proteaza są nierozerwalnie zaangażowane w pękanie pęcherzyków, 42 i jest oczywiste, że wydzielanie tego białka jest związane z indukowanym LH wzrostem biosyntezy prostaglandyn pęcherzykowych, chociaż wskazano, że te dwa zdarzenia mogą nie być współzależne. Możliwy mechanizm działania prostaglandyn w pęknięciu pęcherzyka jajnikowego przedstawiono na fig.
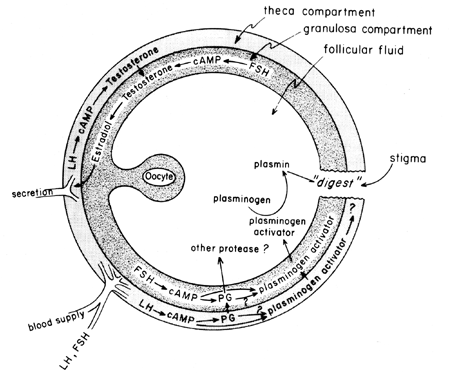 Fig. 6. Możliwy mechanizm działania prostaglandyn w pęknięciu pęcherzyka.(Behrman HR: prostaglandyny w funkcji podwzgórzowo-przysadkowej i jajników. Ann Rev Physiol 41:685, 1979)
Fig. 6. Możliwy mechanizm działania prostaglandyn w pęknięciu pęcherzyka.(Behrman HR: prostaglandyny w funkcji podwzgórzowo-przysadkowej i jajników. Ann Rev Physiol 41:685, 1979)
rola prostaglandyn w funkcji lutealnej: Luteoliza i miesiączka
mechanizm, w którym ludzkie ciałko żółte regresuje 10 do 12 dni po jego utworzeniu, jest tajemnicą. Od wczesnego odkrycia, że PGF2a jest luteolityczna u szczurów i wielu innych gatunków podrzędnych, 43 podjęto duże wysiłki badawcze w celu zbadania możliwości regulacji miesiączki za pomocą PGF2a.PGF2a indukuje regresję czynnościową ciałka żółtego w procesie zależnym od receptora, niezależnym początkowo od zmian w przepływie krwi jajnikowej lub lutealnej.32 W ciągu kilku minut PGF2a wyczerpuje kwas askorbinowy, 44 odkleja zajęty receptor LH z cyklazy adenylanowej i zmniejsza transport gonadotropiny z naczyń włosowatych do komórki lutealnej.
przegląd odnośnej literatury ujawnia wiele sprzecznych doniesień na temat wpływu PGF2a na ludzi. W niektórych badaniach odnotowano przejściowe zmniejszenie stężenia progesteronu we krwi przez PGF2a, 45, chociaż w innych badaniach nie wykazano takiego działania u kobiet z prawidłową owulacją.46,47 biorąc pod uwagę istnienie domniemanych receptorów PGF2a w ciałku żółtym człowieka,48 uzasadniono, że brak osiągnięcia luteolizy po dożylnych wlewach PGF2a był prawdopodobnie spowodowany szybkim metabolizmem płucnym. Późniejsze badania z bezpośrednim wstrzyknięciem PGF2a do ciałka żółtego człowieka wywołały odstawienie progesteronu, którego nadir zbiegł się z początkiem wczesnych miesiączek.Wyniki te sugerują, że do regresji lutealnej może być konieczne stosowanie endogennych prostaglandyn jajnikowych (lub innych leków luteolitycznych). Wydaje się to możliwe w świetle obserwacji, że ludzka funkcja lutealna wydaje się być niezależna od kontroli macicy, ponieważ ani histerektomia50, ani wrodzony brak macicy, pochwy lub jajowodów nie wpływa na cykliczność jajników.Ludzka tkanka lutealna jest z pewnością zdolna do wytwarzania prostaglandyn, jak pokazano w doświadczeniach in vitro 52; jednakże próby skorelowania zwiększonego poziomu PGF2a w jajniku z regresją lutealną w późnej fazie lutealnej nie powiodły się.Wydaje się, że produkcja PGF2a przez jajniki w cyklu menstruacyjnym człowieka jest zwiększona dopiero po owulacji.Jest jednak również oczywiste, że stężenia PGF2a są zawsze wyższe w tkance zrębowej jajnika w fazie wczesnego, środkowego i późnego lutealnego.
w przeciwieństwie do działania PGF2a in vivo, badania in vitro wykazały zarówno przemijające, jak i utrzymujące się działanie luteolityczne w ludzkiej tkance lutealnej.55,56,57 panuje ogólna zgoda co do tego, że wczesnym zdarzeniem wywołanym przez PGF2a luteolizą jest zniesienie wrażliwej na gonadotropinę produkcji cAMP pochodzącej z badań ciałka żółtego szczura.58,59 zniesienie to jest prawdopodobnie spowodowane bezpośrednim hamowaniem cyklazy adenylowej przez zwiększenie wewnątrzkomórkowego Ca2+.Najnowsze dane z dziedziny neurobiologii wskazują, że prostaglandyny stymulują uwalnianie wewnątrzkomórkowego Ca2+ poprzez zwiększenie hydrolizy fosfoinozytolu do diacyloglicerolu i trifosforanu inozytolu.Zgodnie z wynikami badań u zwierząt laboratoryjnych wykazano, że regresja ludzkiego ciałka żółtego wiąże się również z utratą receptorów LH.62
wiadomo, że nowo powstałe ciałko żółte wielu gatunków jest oporne na działanie lityczne PGF2a63; ta obserwacja wydaje się również rozciągać się na ludzkie ciałko żółte.Henderson i McNatty65 zasugerowali, że receptory PGF2a w nowo utworzonym ciałku żółtym mogą być w jakiś sposób maskowane przez zajęte receptory LH i że stopniowe oddzielanie LH od jego receptora może zwiększać wrażliwość ciałka żółtego na PGF2a. Alternatywna hipoteza została zaproponowana przez innych badaczy, 65, którzy sugerują, że podatność ludzkiego ciałka żółtego na PGF2a może zależeć od poziomu noradrenaliny jajników, które zwiększają się w fazie lutealnej. Ten wzrost katecholamin wydaje się umożliwiać antygonadotropowe działanie PGF2a na ludzkie ciałko żółte.
prostaglandyny w macicy
w przeciwieństwie do mięśniówki macicy, która produkuje głównie PGI2, endometrium niedojrzałe wytwarza głównie PGF2a i PGE2. Synteza prostaglandyn jest większa w nabłonku gruczołowym niż w zrębie endometrium, a w fazie wydzielniczej niż w fazie proliferacyjnej cyklu.Zarówno PGF2a, jak i PGE2, dzięki oddziaływaniu ze specyficznymi receptorami, stymulują kurczliwość miometriów, co prowadzi do zwiększenia wewnątrzkomórkowego Ca2+. Taki mechanizm wywołanej prostaglandyną hiperkontraktywności macicy jest zaangażowany w patogenezę pierwotnego bolesnego miesiączkowania. Stwierdzono podwyższone stężenia PGF2a i PGE2 w endometrium i płynie menstruacyjnym u kobiet z bolesnym miesiączkowaniem, a wykazano, że leki przeciwprostaglandynowe powodują znaczne zmniejszenie bólu u tych pacjentów.
różne prostaglandyny są również wytwarzane w szyjce macicy, a miejsca receptorowe zarówno dla PGE, jak i PGF są obecne w szyjce macicy.Zwiększona produkcja prostaglandyn lub ich miejscowe podawanie wiąże się z dojrzewaniem szyjki macicy u kobiet w ciąży.
prostaglandyny i przebieg porodu
szereg obserwacji pośrednio implikuje udział prostaglandyn w przebiegu porodu. Wiadomo na przykład, że podawanie indometacyny lub innych niesteroidowych leków przeciwzapalnych, takich jak aspiryna, przedłuża ciążę.Ponadto wiadomo, że prostaglandyny, w szczególności PGF2a, są silnymi stymulatorami kurczliwości macicy i wywołują cykliczne skurcze macicy ciążowej. Podwyższone stężenie prostaglandyn wiąże się z początkiem spontanicznego porodu u ludzi. Ponadto, okres poprzedzający wystąpienie skurczów charakteryzuje się stężeniem PGF2a w osoczu, które jest równoważne z występowaniem u kobiet w ciąży. Szczepienie przeciwko PGF2a opóźnia również początek porodu.70 prostaglandyn jest obecnie używanych do wywoływania wczesnego porodu i aborcji; rzeczywiście, prostaglandyna jest lekiem z wyboru do przeprowadzenia aborcji midtrimestru.69,71
opierając się na obszernych badaniach u owiec, wydaje się, że prostaglandyny syntetyzowane lokalnie w macicy inicjują poród poprzez bezpośrednie działanie na miometrium w celu pobudzenia skurczów macicy. Zmniejszenie miejscowego, łożyskowego progesteronu w połączeniu ze wzrostem estrogenu powoduje uwalnianie Ca2+ z lizosomów, które stały się kruche. To uwalnianie Ca2 + stymuluje syntezę prostaglandyn poprzez zwiększenie aktywności fosfolipazy. Oksytocyna wydaje się ułatwiać, a nie inicjować, działanie estrogenu i progesteronu.Błona płodowa, decidua vera i myometrium mogą uczestniczyć w tworzeniu prostaglandyn.73,74
najnowsza propozycja jest taka, że wytwarzanie prostaglandyn w tkance wewnątrzmacicznej jest tonicznie hamowane podczas ciąży u ludzi i że takie hamowanie jest stopniowo usuwane w miarę zbliżania się terminu. Chociaż mechanizmy wpływające na toniczne hamowanie syntezy prostaglandyn nie zostały ustalone, kilka peptydów antyfosfolipazowych znaleziono w ludzkim łożysku,amnonie, 75 i Kosmówce.Inną możliwością jest stymulowanie syntezy prostaglandyn równolegle z usuwaniem zahamowania syntezy. Potencjalnymi sygnałami zwiększonej syntezy prostaglandyn jest kilka czynników wzrostu i czynnik aktywujący płytki krwi. Płodu płuca i tkanki nerek wydzielają czynnik aktywujący płytki krwi, który jest zdolny do stymulowania produkcji prostaglandyn przez ludzką amnię.
prostaglandyny i przewód tętniczy
utrzymanie drożności (rozluźnienie rozszerzenia naczyń) przewodu tętniczego ma kluczowe znaczenie dla kontrolowania natlenienia tkanek płodu. Po urodzeniu przewód tętniczy Zwykle ulega zwężeniu lub traci drożność. Mechanizm, w którym następuje to zamknięcie, jest niejasny, chociaż uważa się, że ważnym czynnikiem jest napięcie tlenu we krwi (rys. 7). Podstawową funkcją przewodu tętniczego u płodu jest utrzymanie pewnego stopnia przetaczania krwi tętniczej od lewej do prawej, kontrolując w ten sposób ilość żylnego powrotu do płuc. Zamknięcie przewodu w terminie jest ważnym procesem fizjologicznym, który, jeśli jest niekompletny, prowadzi do niewydolności oddechowej i sinicy/niedotlenienia—zespołów odpowiedzialnych za wysoką zachorowalność i śmiertelność u wielu wcześniaków cierpiących na patentowy przewód tętniczy. Z tego powodu istnieje duże zainteresowanie mechanizmem(mechanizmami) kontrolowania funkcji przewodu tętniczego. Zainteresowanie to jest szczególnie dotkliwe w dziedzinie badań nad prostaglandynami, w których obecnie istnieje znaczna ilość dowodów sugerujących udział prostaglandyn w kontrolowaniu drożności przewodu tętniczego w okresie.
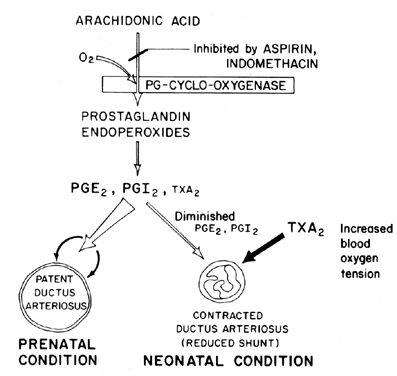 Fig. 7. Schemat prostaglandynowej modulacji drożności przewodu tętniczego u płodu i noworodka w funkcji napięcia tlenowego.
Fig. 7. Schemat prostaglandynowej modulacji drożności przewodu tętniczego u płodu i noworodka w funkcji napięcia tlenowego.
dowody te opierają się na następujących seriach obserwacji:
przewód tętniczy u płodu z pogorszeniem czynności układu krążenia i chorobą błony szklistej można zamknąć przez podanie inhibitorów syntetazy prostaglandynowej.
Indometacyna może wywoływać skurcz naczynia niedotlenienia, o czym świadczą jej działania u zwierząt w okresie niedotlenienia.
podanie PGE2 (i PGE1) powoduje relaksację (utratę drożności) izolowanych preparatów z przewodu tętniczego jagnięcego płodu (okrągłe paski) w środowisku o niskiej zawartości tlenu (PO2 poniżej 14 mmHg).80
wydaje się prawdopodobne, że prostaglandyny serii E, w połączeniu z antagonistami prostaglandyn i blokerami syntetazy prostaglandynowej (aspiryna), mogą okazać się pożądanym leczeniem niechirurgicznym u wcześniaków z potencjalnie śmiertelnym przewodem tętniczym. Najnowsze dowody sugerują równowagę między drożnością przewodu i zwężeniem, która jest utrzymywana przez syntezę rozszerzających się prostaglandyn (PGI2 i PGE2) i zwężających prostaglandyn (TXA2). U płodu jagnięcego zarówno przewód tętniczy, jak i płuca syntetyzują PGI2 i PGE2; następnie, w miarę zbliżania się terminu, płuca przesuwa się w kierunku syntezy TXA2.Dostępne są dalsze informacje na temat udziału prostaglandyn w kontroli czynności przewodu tętniczego.82