US Pharm. 2006;7:58-68.
srdeční selhání je hlavním zdravotním problémem ve Spojených státech. Přibližně pět milionů lidí má srdeční selhání a 550 000 pacientů je diagnostikováno se srdečním selháním každý rok.1,2 srdeční selhání je obecně charakterizováno jako onemocnění starších osob; přibližně 80% pacientů hospitalizovaných se srdečním selháním je starších 65 let. Očekává se tedy, že výskyt srdečního selhání poroste s věkem populace.2 hospitalizace související se srdečním selháním se v letech 1990 až 1999 zvýšily přibližně o 25% na více než milion. V roce 2001 srdeční selhání přímo způsobilo 53 000 úmrtí. Úmrtí související se srdečním selháním v posledních letech vzrostla, což lze připsat zvýšení přežití z předchozích kardiovaskulárních příhod.
Srdeční selhání je klinický syndrom, ve kterém funkční nebo strukturální změny se vyskytují v srdci, což vede v klinické příznaky, jako je dušnost, únava, omezená tolerance cvičení, plicní kongesce, a periferní edém.1-3 mnoho známých rizikových faktorů, jako je ischemická choroba srdeční (CAD), diabetes, obezita, hypertenze a rodinná anamnéza kardiomyopatií, je spojeno s nástupem a progresí srdečního selhání (Tabulka 1).4 kromě toho je chlopňové srdeční onemocnění stále běžnou příčinou srdečního selhání. Hypertenze předchází srdeční selhání přibližně 90% času a zvyšuje riziko srdečního selhání u pacienta třikrát.5 CAD je nejčastější příčinou systolického srdečního selhání. Infarkt myokardu (MI) představuje systolické srdeční selhání u téměř 70% pacientů. Mezi další etiologie spojené se systolickou dysfunkcí a srdečním selháním patří dilatační kardiomyopatie a ventrikulární hypertrofie.2,4

Patofyziologie
Systolický srdeční selhání je spojena s dysfunkcí levé komory kontraktility, která vyústí v neefektivní srdečního výdeje, zejména při námaze. Srdeční selhání obvykle začíná nějakým zraněním nebo stresem na myokardu, což má za následek změnu struktury srdce; Toto je známé jako remodelace srdce. Srdeční remodelace předchází nástupu příznaků měsíce nebo dokonce roky. Jako dilatace změny komory, aby se více kulovitý tvar, hemodynamické zdůrazňuje, začít přidávat napětí na stěnách selhávající srdeční komory, což vede k depresi mechanické funkce a zvýšené regurgitant průtoku přes mitrální chlopeň.1-3
neurohormonální systém má aktivní roli při akceleraci srdeční remodelace. Pacienti se srdečním selháním mají zvýšené hladiny norepinefrinu, angiotensinu II, aldosteronu, endotelinu, vazopresinu a cytokinů. Aktivace systému renin-angiotensin-aldosteron zvyšuje periferní vazokonstrikci, což vede ke zvýšené afterload a srdeční remodelaci. Kromě toho, aktivace sympatického nervového systému, způsobuje tachykardii, což vede ke zvýšení poptávky myokardu kyslíku. Zvýšená potřeba srdečního kyslíku bez změn nabídky může způsobit zvýšenou ischemii myokardu a další remodelaci srdce. Neurohormony mohou mít kardiotoxické účinky na buňky, což může dále změnit architekturu a výkon srdce.2
Klinické Prezentace
Systolický srdeční selhání je syndrom diagnostikován na základě údajů získaných od důkladné anamnézy, včetně vyhodnocení symptomatologie a fyzikální nález. Většina pacientů je přítomna jedním ze tří způsobů: se sníženou tolerancí cvičení, s retencí tekutin nebo bez příznaků.2,6 dušnost při námaze a dušnost jsou kardinálními příznaky srdečního selhání. Při fyzickém vyšetření může být přítomen periferní edém, plicní kongesce nebo oba příznaky.2
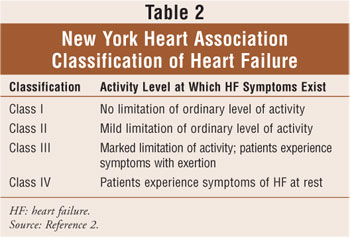
Klasifikace srdečního selhání je založena na kombinaci American College of Cardiology/American Heart Association je čtyři fáze srdečního selhání (Tabulka 1), které se pohybují od v ohrožení pro srdeční dysfunkcí (stupeň A) pro refrakterní srdeční selhání (stupeň D), a na New York Heart Association (NYHA) pokyny.2,6 klasifikace NYHA je nejčastěji používanou metodou pro kvantifikaci stupně funkčního omezení uloženého srdečním selháním (Tabulka 2). Celkově má funkční klasifikace srdečního selhání tendenci v průběhu času klesat v důsledku progrese srdeční remodelace.2
jeden z nejdůležitějších užitečný diagnostický test je komplexní dva-rozměrné echokardiografie, který se používá spolu s Doppler flow studie k určení, zda existují strukturální a funkční abnormality v srdci. Transthorakální echokardiogram (TTE) je neinvazivní ultrazvuková studie, která vytváří obrazy srdce pomocí zvukových vln. Poskytuje informace o odhadu ejekční frakce levé komory (LVEF), komorových rozměrech a objemech, objemech stěn, geometrii srdeční komory a regionálním pohybu stěny. U pacientů se systolickým srdečním selháním je LVEF obvykle nižší než 40%.2 Další studie používá ve spojení s TTE posoudit, etiologie, závažnosti a možných lékových účinků léčby souvisejících se u srdečního selhání zahrnují základní rentgenový snímek hrudníku, 12-svodového ekg a měření mozkový natriuretický peptid, sérových elektrolytů a renální funkce. Tyto studie jsou důležité, protože zdravotní péče může použít jako základ pro určení, zda pacient má zkušený změnu klinického stavu.2,6
ŘÍZENÍ SYSTOLICKÉHO SRDEČNÍHO SELHÁNÍ
Nefarmakologické
Ovládání rizikové faktory jako je hypertenze, diabetes mellitus, dyslipidemias, aterosklerotické cévní onemocnění a poruchy štítné žlázy může zpomalit progresi srdečního selhání a srdeční remodelace.2,4,6 pacienti se srdečním selháním by měli dostávat vakcíny proti chřipce a pneumokokům, aby se snížilo riziko komorbidit, jako jsou respirační infekce.2 nejvýznamnějším modifikovatelným rizikovým faktorem by bylo vysoce rizikové chování, jako je kouření, alkohol a nedovolené užívání drog.2,7
omezení sodíku (?2 gramy / den) pomáhá při snižování přetížení objemu a může snížit užívání diuretik. Denní vážení navíc umožňuje pacientům posoudit objemový stav, na kterém může být založena úprava dávky diuretika. Žádné studie však nezkoumaly účinek dietárního omezení sodíku na morbiditu nebo mortalitu.Bylo prokázáno, že fyzická aktivita 7,8 snižuje úmrtnost a hospitalizace u stabilních pacientů se srdečním selháním. Omezení cvičení podporuje fyzickou dekondici, což může přispět k intoleranci cvičení pacienta. A konečně, dodržování dietního a terapeutického léčebného režimu má významnou roli v prevenci akutních hospitalizací.2,7
Farmakologické
Většina pacientů se srdečním selháním jsou léčeni standardní kombinací tří léků režim: smyčka diuretika, inhibitory angiotenzin-konvertujícího enzymu (ACE) inhibitory nebo antagonisté angiotensinu II, blokátory receptorů (ARB), beta-adrenergních receptorů blokátory.1,2 diuretika jsou základem pro snížení příznaků přetížení objemu při srdečním selhání, zatímco ACE inhibitory, ARB a beta-blokátory ukázaly, že snižují morbiditu a mortalitu.2 antagonisty Aldosteronu je indikován jako přídatná terapie u pacientů se symptomatickou NYHA třída III nebo IV srdečního selhání nebo brzy po akutním infarktu myokardu u pacientů se sníženou funkci levé komory a klinické známky srdečního selhání. Pokud jsou pacienti i nadále symptomatičtí, může být digoxin přidán do standardního léčebného režimu, aby se snížily příznaky, snížily hospitalizace a zvýšila se tolerance cvičení. Léky používané k léčbě srdečního selhání jsou popsány v tabulce 3. Změny životního stylu a farmakoterapii systolického srdečního selhání jsou navrženy tak, aby snížení nemocnosti a úmrtnosti, brání progresi srdeční remodelace a improvepatients kvality života.2
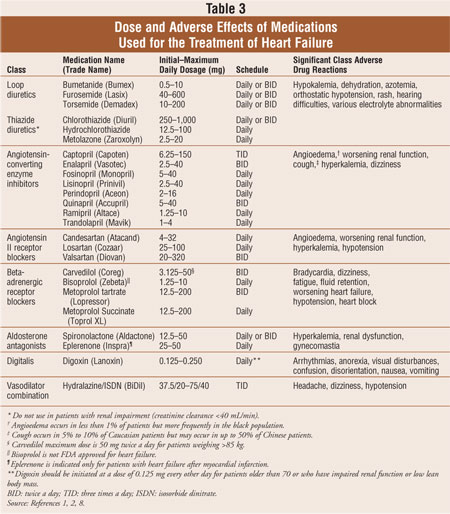
Diuretika:Základem symptomatické léčby přetížení objemu při srdečním selhání, diuretika snižují retenci tekutin, která způsobuje plicní kongesci, periferní edém, jugulární žilní distenzi a/nebo zvýšenou tělesnou hmotnost. Smyčková diuretika působící ve smyčce Henle zvyšují vylučování sodíku v séru o 20% až 25%, zvyšují vylučování volné vody a udržují jejich účinnost u pacientů s poruchou funkce ledvin.1,2 V kontrastu, thiazidová diuretika snižují vylučování sodíku o 5% na 10%, zvýšit toaletní voda eliminace, a ztratí svou účinnost u pacientů s chronickým onemocněním ledvin (clearance kreatininu <40 mL/min). Kličková diuretika jsou preferovanými látkami pro léčbu srdečního selhání, ale thiazidy mohou být použity u pacientů s mírnou retencí tekutin a hypertenzí. Diuretika, stejně jako ACE inhibitory a beta-blokátory, se doporučují pro použití u všech pacientů se srdečním selháním ve stadiu C.2 studie ukázaly, že diuretika zlepšují srdeční funkce, příznaky a nesnášenlivost cvičení u pacientů se srdečním selháním. Dlouhodobé účinky diuretik na mortalitu však nejsou známy.1,2,8
Inhibitorů ACE: inhibitory ACE snižují aktivitu renin-angiotenzin-aldosteronový systém tím, že blokuje přeměnu angiotenzinu I na angiotenzin II, brání angiotenzin II indukovanou vazokonstrikci. Také inhibují uvolňování aldosteronu, což vede ke snížení retence sodíku a tekutin. Tyto kombinované účinky snižují předpětí i následné zatížení a zpomalují progresi srdeční remodelace.1,2 ACE inhibitory mohou mít také další aktivitu se zvýšenou produkcí kininů a kininem zprostředkovanou produkcí prostaglandinů.2 Více než 30 klinických kontrolovaných studií hodnotících účinnost ACE inhibitory prokázaly, že inhibitory ACE snižují riziko smrti a kombinované riziko úmrtí a hospitalizací. U všech pacientů s levou ventrikulární systolický srdeční selhání by měl být podáván inhibitor ACE, pokud je kontraindikováno (angioedém, bilaterální stenóza renální tepny, sérové hladiny draslíku >5.5 mmol/L, těhotenství, symptomatická hypotenze nebo nestabilní renální selhání). ACE inhibitory by měly být zahájeny v nízkých dávkách a pomalu titrovány na základě snášenlivosti nežádoucích účinků.1,2,8
ARB: ve srovnání se studiemi ACE inhibitorů bylo méně klinických studií studováno použití ARB u pacientů se srdečním selháním; tato činidla jsou tedy vyhrazena pro pacienty s prokázanou intolerancí ACE inhibitorů. ARB selektivně blokují angiotensin II vazbou na receptor angiotensinu. ARB snižují závažnost nežádoucích účinků kininu, jako je kašel a angioedém, ačkoli u těchto látek byl hlášen angioedém. Přidání ARB k standardní terapii včetně ACE inhibitorů může snížit velikost levé srdeční komory a počet hospitalizací, ale důkazy jsou nedostatečné ve snížení úmrtnosti.2,8 jedna studie ukázala, že kandesartan přidaný k ACE inhibitoru snižuje kardiovaskulární úmrtí.9 Nicméně, další studie valsartanu u pacientů s MIand srdečního selhání prokázán žádný prospěch z valsartan a inhibitor ACE podáván společně ve srovnání s ACE inhibitory sám.10 předepisování kombinace ACE inhibitorů, ARB a antagonistů aldosteronu se nedoporučuje kvůli riziku hyperkalemie. ARB zůstávají alternativou k ACE inhibitorům při léčbě srdečního selhání.2
blokátory Beta-adrenergních receptorů: bylo prokázáno, že tři typy beta-blokátorů snižují mortalitu: s prodlouženým uvolňováním metoprolol a bisoprolol, které selektivně blokují beta-1 receptory, a karvedilol, který blokuje alfa-1, beta-1 a beta-2 receptory.1,2,8 Ve srovnání, studie ukázala, že krátkodobě působící metoprolol měl menší efekt ve srovnání s karvedilol, ale dávka metoprololu byla použita nižší, než doporučenou dávku.11 kromě standardní terapie prokázaly beta-blokátory kombinované snížení úmrtí a hospitalizace pro srdeční selhání. Beta-blokátory inhibují nepříznivé účinky sympatického nervového systému a převažují nad negativními inotropními účinky.2 Celkově, beta-blokátory by měla být zahájena velmi nízkými dávkami, titruje se pomalu v nejméně dvoutýdenních intervalech, a ne náhle stažena, vzhledem k riziku zhoršení srdečního selhání a akutní dekompenzace.1,2
Antagonisty Aldosteronu: antagonisty Aldosteronu blok receptoru aldosteronu v distálním tubulu nefronu, což vede k retenci draslíku, sodíku ledvinami, a mírné diurézy. Antagonisty aldosteronu se doporučuje u pacientů se středně závažným nebo závažným srdečním selháním a posledních dekompenzace nebo u pacientů s dysfunkcí levé komory brzy po infarktu myokardu.2 při přidání nízké dávky spironolaktonu k ACE inhibitoru u pacientů se srdečním selháním třídy III a IV NYHA došlo u pacientů k 30% snížení mortality ze všech příčin.12 Další studie ukázala, že eplerenone vedlo ke snížení mortality u pacientů s LVEF méně než 40% do 14 dnů MI, i když nejsou k dispozici žádné údaje o použití eplerenone v léčbě srdečního selhání týkající se jiných příčin, než MI.13 nejvýznamnějším limitujícím faktorem antagonistů aldosteronu je potenciálně život ohrožující hyperkalemie.2,14 hyperkalemie se postupně zvyšuje, když sérový kreatinin překročí 1,6 mg / dL, přestože studie zkoumaly antagonisty aldosteronu u pacientů se vstupní hladinou sérového kreatininu 2,0 až 2,5 mg / dl. Kromě toho, antagonisty aldosteronu je třeba se vyhnout u pacientů s hladinou sérového draslíku větší než 5,0 mEq na litr.2
Digoxin: Digoxin je srdeční glykosid, který pracuje na zvýšení kontraktility srdce tím, že brání sodno-draselný adenosin triphosphatase (Atpáza) čerpadla, čímž se zvyšuje intracelulární vápník. Digoxin je doporučeno pro symptomatické kontroly u pacientů s mírným až středně závažným srdečním selháním NYHA třídy II nebo III.2 V post hoc analýzy sérové koncentrace digoxinu v rozmezí 0,5-0,9 ng/mL snížil hospitalizací; nicméně, koncentrace vyšší než 1 ng/mL byly spojeny s trend ke zvýšení mortality ve srovnání s placebem.15 Zatímco studie neprokázaly, že digoxin snižuje úmrtnost, tento agent může zlepšit příznaky a cvičení nesnášenlivosti, snížení hospitalizací, a zlepšit celkovou kvalitu života.2,8,16
Vazodilatační Kombinace: Doporučení hydralazin a isosorbid dinitrát (ISDN) v kombinaci je vyhrazena pro pacienty, kteří prokázali neschopnost tolerovat inhibitoru ACE nebo ARB. V nedávné studii zahrnující kohortu afroamerických pacientů se symptomatickým srdečním selháním NYHA III nebo IV však přidání kombinace hydralazinu a ISDN ke standardní terapii (tj.17 teoreticky může kombinace hydralazinu a ISDN zvýšit biologickou dostupnost oxidu dusnatého.2 kombinace ISDN a hydralazin (BiDil) je schválena FDA pouze pro Afroameričany jako doplňková terapie ke standardní terapii srdečního selhání.18 Hydralazin je arteriole vazodilatační, který působí na snížení dotížení, zatímco ISDN je žilní vazodilatační, který působí na snížení předpětí. Tato kombinace vazodilatancií není upřednostňována ACE inhibitory nebo o arb, protože to může mít netolerovatelné nežádoucí účinky, jako jsou bolesti hlavy nebo závratě a otázky dodržování předpisů, jako jsou zmeškané dávky, ale může být použita jako doplňková terapie pro Afro-Americkou populaci.2
alternativní léky: hlohové listy s květy, také známé jako extrakt Crataegus, byly obhajovány pro mírné srdeční selhání (NYHA II). Prostřednictvím studií in vitro prokázaly listy hlohu pozitivní inotropní účinky, vazodilatační vlastnosti a zvýšený koronární průtok krve. Studie prokázaly zlepšení subjektivních symptomů u pacientů s mírným srdečním selháním. Vzhledem k účinkům podobným digitalisu by pacienti užívající jak extrakt Crataegus, tak digitalis měli být pečlivě sledováni. Hlášenými nežádoucími nežádoucími účinky byly gastrointestinální příznaky, palpitace, bolest na hrudi a závratě.19,20
dalším alternativním lékem, který byl použit při léčbě srdečního selhání, je coenyzme Q10, vitamín rozpustný v tucích. Některé studie prokázaly, že koenzym Q10 vedl ke zlepšení frekvence hospitalizací, dušnosti a edému.21 Nicméně, randomizované, dvojitě zaslepené, placebem kontrolované studie neprokázaly rozdíl mezi coenyzme Q10 a placebem v LVEF, tolerance cvičení, nebo maximální spotřeby kyslíku u pacientů se srdečním selháním.22 dokumentované nežádoucí účinky koenzymu Q10 byly gastrointestinální diskomfort, hypoglykémie a hypotenze.Probíhá 21 klinických kontrolovaných studií s extraktem Crataegus a coenyzme Q10 za účelem vyhodnocení účinnosti a bezpečnosti při léčbě srdečního selhání.20,21
ŠKODLIVÉ LÉKY PŘI SRDEČNÍM SELHÁNÍ
Několik tříd léků může zhoršit srdeční selhání a je třeba se vyhnout. Antiarytmika, kromě amiodaronu nebo dofetilidu, mohou způsobit kardiodepresivum a proarytmický účinek na srdce, což vede k akutní dekompenzaci.1,2 blokátory kalciových kanálů první generace byly spojeny se zvýšenými kardiovaskulárními příhodami a zhoršením srdečního selhání. Novější, dlouhodobě působící blokátory kalciových kanálů amlodipin a felodipin se zdají být bezpečné, ale žádné studie, které prokázaly statisticky významné snížení mortality.2,8,23 thiazolidindiony byly spojeny s přibýváním na váze a retencí tekutin, což mohlo vést k srdečnímu selhání nebo k exacerbaci akutního srdečního selhání. Při použití thiazolidindionů v kombinaci s inzulínovou terapií je však pravděpodobnější edém.24,25 thiazolidindiony se proto nedoporučují u pacientů s diabetes mellitus a srdečním selháním třídy III nebo IV NYHA.25-27 NSAID způsobují retenci sodíku a periferní vazokonstrikci, což vyvolává akutní exacerbaci srdečního selhání. Kromě toho snižují účinnost a zvyšují riziko toxicity ACE inhibitorů a diuretik. Existuje možnost lékové interakce, pokud se aspirin používá v kombinaci s ACE inhibitory, ale zůstává kontroverzní a vyžaduje další studium.2
role lékárníka
pochopení výhod farmakoterapie při srdečním selhání může vést k optimální farmaceutické péči. Lékárníci mohou pacientům pomoci identifikovat a zmírnit vysoce rizikové chování, jako je kouření, konzumace alkoholu a nedovolené a škodlivé užívání OTC drog. Kromě toho musí lékárníci sledovat progresi chorobného stavu pacientů, včetně známek a příznaků srdečního selhání, a povzbuzovat pacienty, aby zmapovali jejich hmotnost.
Podpora pacientů, aby dodržovali dietní omezení, pokyny pro cvičení a léčebné režimy pro srdeční selhání, by měla být prioritou lékárníka. Nedodržování terapeutických léků bylo spojeno se zvýšením úmrtnosti a může souviset s nežádoucími vedlejšími účinky léků. Lékárníci by měli sledovat a povzbuzovat pacienty, aby dodržovali své léky, aby snížili úmrtnost. Sledováním a vzděláváním pacientů a dalších zdravotnických pracovníků o nežádoucích účincích souvisejících s drogami mohou lékárníci pomoci zvýšit dodržování léků. Kromě toho, lékárníci musí být vědomi alternativ léky, jako jsou ACE inhibitory a diskutovat s ostatními poskytovateli zdravotní péče dávky v úmrtnosti spojené s nimi s cílem poskytnout optimální farmaceutické péče a snížit riziko úmrtnosti.
pacienti a poskytovatelé zdravotní péče si nemusí být vědomi souvislosti mezi běžnými léky a exacerbacemi srdečního selhání. Od některých běžných volně PRODEJNÝCH léků, včetně Nsaid, jsou kontraindikovány u pacientů se srdečním selháním, vzdělávání pacienta o tom, proč on nebo ona by se neměla brát tyto léky, je další důležitou roli pro lékárníky. Lékárníci musí sledovat pacienty a konzultovat s poskytovateli zdravotní péče a pacienty o škodlivých interakcích mezi léky a léky,které mohou vést k hospitalizaci.
1. Klein L, O ‚ Connor CM, Gattis WA, et al. Farmakologická léčba u pacientů s chronickým srdečním selháním a sníženou systolickou funkcí: přehled pokusů a praktických úvah. Jsem J Cardiol. 2003; 91 (suppl): 18F-40F.
2. Hunt SA, Abraham WT, Chin MH, et al. ACC/AHA 2005 pokyn aktualizace pro diagnostiku a léčbu chronického srdečního selhání u dospělých: zpráva z American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Psaní Výboru k Aktualizaci 2001 Pokyny pro Hodnocení a Řízení Srdeční Selhání). American College of Cardiology webové stránky. K dispozici na adrese: www.acc.org/clinical/guidelines/failure//index.pdf.
3. Francis GS, Gassler JP, Sonnenblick EH. Patofyziologie a diagnostika srdečního selhání. In: Fuster V, et al, eds. Hurst je srdce. 10.vydání. New York, NY: McGraw-Hill; 2001: 655-686.
4. Dei Cas L, Metra M, Nodari S, et al. Prevence a léčba chronického srdečního selhání u rizikových pacientů. Jsem J Cardiol. 2003; 91 (suppl): 10F-17F.
5. Chobanian AV, Bakris GL, Black HR, et al. Sedmá zpráva smíšeného Národního výboru pro prevenci, detekci, hodnocení a léčbu vysokého krevního tlaku. Hypertenze. 2003;42:1206-1252.
6. Frigerio M, Oliva F, TURAZZA FM, Bonow RO. Prevence a léčba chronického srdečního selhání při léčbě asymptomatických pacientů. Jsem J Cardiol. 2003; 91 (suppl): 4F-9F.
7. Colonna P, Sorino M, D ‚ Agostino C, et al. Nefarmakologická péče o srdeční selhání: poradenství, dietní omezení, rehabilitace, léčba spánkové apnoe a ultrafiltrace. Jsem J Cardiol. 2003; 91 (suppl): 41F-50F.
8. McConaghy JR, Smith SR. ambulantní léčba systolického srdečního selhání. Jsem Fam Lékař. 2004;70:2157-2164.
9. Young JB, Dunlap ME, Pfeffer MA, et al. Úmrtnost a nemocnost snížení s candesartan u pacientů s chronickým srdečním selháním a systolickou dysfunkcí levé komory: výsledky KOUZLO low-ejekční frakce levé komory studiích. Oběh. 2004;110:2618-2626.
10. Cohn JN, Tognoni G. randomizovaná studie blokátoru angiotensinových receptorů valsartanu u chronického srdečního selhání. N Engl J Med. 2001;345:1667-1675.
11. Poole-Wilson PA, Swedbery K, Cleland JG, et al. Srovnání karvedilolu a metoprololu na klinických výsledcích u pacientů s chronickým srdečním selháním v evropské studii carvedilol nebo metoprolol (COMET): randomizovaná kontrolovaná studie. Lanceta. 2003;362:7-13.
12. Pitt B, Zannad F, Remme WJ, et al. Účinek spironolaktonu na morbiditu a mortalitu u pacientů se závažným srdečním selháním. N Engl J Med. 1999;341:709-717.
13. Pitt B, Remme W, Zannad F, et al. Eplerenon, selektivní blokátor aldosteronu, u pacientů s dysfunkcí levé komory po infarktu myokardu. N Engl J Med. 2003;348:1309-1321.
14. Aldacton . Chicago, IL: Pharmacia Corporation; červenec 2003.
15. Ahmed A, Rich MW, Love TE, et al. Digoxin a snížení úmrtnosti a hospitalizace při srdečním selhání: komplexní post hoc analýza studie DIG. Eur Srdce J. 2006; 27: 178-186.
16. Vyšetřovací Skupina Digitalis. Vliv digoxinu na mortalitu a morbiditu u pacientů se srdečním selháním. N Engl J Med. 1997;336:525-533.
17. Taylor AL, Ziesche S, Yancy C, et al. Kombinace isosorbid dinitrátu a hydralazinu u černochů se srdečním selháním. N Engl J Med. 2004;351:2049-2057.
18. Bidile . Lucie Šafářová: Nitromed Inc. Srpna 2005.
19. De Smet PA. Bylinné prostředky. N Engl J Med. 2002;347:2045-2056.
20. Holubarsch CJ, Colucci WS, Meinertz T, et al. Přežití a prognóza: vyšetřování extraktu Crataegus WS 1442 u městnavého srdečního selhání (SPICE) – zdůvodnění, návrh studie a protokol studie. Eur J Srdce Selhat. 2000;2:431-437.
21. Bonadkar RA, Guarneri E. koenzym Q10. Jsem Fam Lékař. 2005;72:1065-1070.
22. Khatta M, Alexander BS, Krichten CM, et al. Účinek přípravku Coenyzme Q10 u pacientů s městnavým srdečním selháním. Ann Intern Med. 2000;132:636-640.
23. De Vries RJM, Van Veldhuisen DJ, Dunselman PHJM. Účinnost a bezpečnost blokátorů kalciových kanálů při srdečním selhání: zaměřte se na nedávné studie s dihydropyridiny druhé generace. Am Heart J. 2000; 139: 185-194.
24. Delea TE, Edelsberg JS, Hagiwara M, et al. Použití thiazolidindionů a riziko srdečního selhání u lidí s diabetem 2. typu. Péče O Diabetes. 2003;26:2983-2989.
25. Hollenberg NK. Úvahy o řízení dynamických problémů s tekutinami spojených s thiazolidindiony. Jsem Med. 2003; 115: 111S-115S.
26. Avandia . Research Triangle Park, NC: GlaxoSmithKline; srpen 2005.
27. Actos . Lincolnshire, IL: Takeda Pharmaceutical American Inc. Srpna 2004.
Chcete-li komentovat tento článek, kontaktujte [email protected].