US Pharm. 2006;7:58-68.
Herzinsuffizienz ist ein großes Gesundheitsproblem in den Vereinigten Staaten. Etwa fünf Millionen Menschen leiden an Herzinsuffizienz, und bei 550.000 Patienten wird jedes Jahr Herzinsuffizienz diagnostiziert.1,2 Herzinsuffizienz wird im Allgemeinen als eine Erkrankung älterer Menschen charakterisiert; Etwa 80% der mit Herzinsuffizienz hospitalisierten Patienten sind älter als 65 Jahre. Daher wird erwartet, dass die Inzidenz von Herzinsuffizienz mit zunehmendem Alter der Bevölkerung zunimmt.2 Herzinsuffizienz-bedingte Krankenhauseinweisungen stiegen zwischen 1990 und 1999 um etwa 25% auf mehr als eine Million. Im Jahr 2001 verursachte Herzinsuffizienz direkt 53.000 Todesfälle. Herzinsuffizienz-bedingte Todesfälle sind in den letzten Jahren gestiegen, was auf eine Zunahme des Überlebens aufgrund früherer kardiovaskulärer Ereignisse zurückzuführen ist.
Herzinsuffizienz ist ein klinisches Syndrom, bei dem funktionelle oder strukturelle Veränderungen im Herzen auftreten, die zu klinischen Symptomen wie Dyspnoe, Müdigkeit, eingeschränkter Belastungstoleranz, Lungenstauung und peripheren Ödemen führen.1-3 Viele bekannte Risikofaktoren wie koronare Herzkrankheit (KHK), Diabetes, Fettleibigkeit, Bluthochdruck und Kardiomyopathien in der Familienanamnese sind mit dem Auftreten und Fortschreiten der Herzinsuffizienz verbunden (Tabelle 1).4 Darüber hinaus ist eine Herzklappenerkrankung immer noch eine häufige Ursache für Herzinsuffizienz. Hypertonie geht der Herzinsuffizienz in etwa 90% der Fälle voraus und erhöht das Risiko einer Herzinsuffizienz um das Dreifache.5 CAD ist die häufigste Ursache für systolische Herzinsuffizienz. Myokardinfarkt (MI) ist bei fast 70% der Patienten für systolische Herzinsuffizienz verantwortlich. Zusätzliche Ätiologien im Zusammenhang mit systolischer Dysfunktion und Herzinsuffizienz umfassen dilatative Kardiomyopathien und ventrikuläre Hypertrophie.2,4

Pathophysiologie
Systolische Herzinsuffizienz ist mit einer Beeinträchtigung der linksventrikulären Kontraktilität verbunden, die insbesondere bei Anstrengung zu einer ineffizienten Herzleistung führt. Herzinsuffizienz beginnt normalerweise mit einer Verletzung oder Belastung des Myokards, die zu einer Veränderung der Struktur des Herzens führt. Die kardiale Remodellierung geht dem Auftreten von Symptomen um Monate oder sogar Jahre voraus. Wenn die Dilatation den Ventrikel in eine kugeligere Form bringt, beginnen hämodynamische Spannungen die Wände des versagenden Ventrikels zu belasten, was zu einer verminderten mechanischen Funktion und einem erhöhten regurgitanten Fluss durch die Mitralklappe führt.1-3
Das neurohormonale System spielt eine aktive Rolle bei der Beschleunigung des Herzumbaus. Patienten mit Herzinsuffizienz haben erhöhte Spiegel von Noradrenalin, Angiotensin II, Aldosteron, Endothelin, Vasopressin und Zytokinen. Die Aktivierung des Renin-Angiotensin-Aldosteron-Systems erhöht die periphere Vasokonstriktion, was zu einer erhöhten Nachlast und einem kardialen Umbau führt. Darüber hinaus verursacht die Aktivierung des sympathischen Nervensystems Tachykardie, was zu einem erhöhten myokardialen Sauerstoffbedarf führt. Ein erhöhter kardialer Sauerstoffbedarf ohne Änderungen der Versorgung kann zu einer erhöhten Myokardischämie und einer weiteren kardialen Remodellierung führen. Die Neurohormone können kardiotoxische Wirkungen auf die Zellen ausüben, was die Architektur und Leistungsfähigkeit des Herzens weiter verändern kann.2
Klinisches Erscheinungsbild
Die systolische Herzinsuffizienz ist ein Syndrom, das auf der Grundlage von Daten diagnostiziert wird, die aus einer gründlichen Anamnese stammen, einschließlich einer Bewertung der Symptomatik und körperlicher Befunde. Die meisten Patienten präsentieren sich auf eine von drei Arten: mit verminderter Belastungstoleranz, mit Flüssigkeitsretention oder ohne Symptome.2,6 Dyspnoe bei Anstrengung und Kurzatmigkeit sind die Hauptsymptome einer Herzinsuffizienz. Bei körperlicher Untersuchung können periphere Ödeme, Lungenstauung oder beide Symptome vorliegen.2
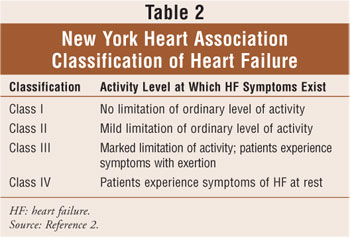
Die Klassifizierung der Herzinsuffizienz basiert auf der Kombination der vier Stadien der Herzinsuffizienz des American College of Cardiology / der American Heart Association (Tabelle 1), die von einem Risiko für Herzfunktionsstörungen (Stadium A) bis zu einer refraktären Herzinsuffizienz (Stadium D) reichen) und auf den Richtlinien der New York Heart Association (NYHA).2,6 Die NYHA-Klassifikation ist die am häufigsten verwendete Methode zur Quantifizierung des Grades der funktionellen Einschränkung durch Herzinsuffizienz (Tabelle 2). Insgesamt nimmt die funktionelle Klassifikation der Herzinsuffizienz im Laufe der Zeit aufgrund des Fortschreitens des kardialen Remodelings tendenziell ab.2
Der nützlichste diagnostische Test ist das umfassende zweidimensionale Echokardiogramm, das zusammen mit Doppler-Flow-Studien verwendet wird, um festzustellen, ob strukturelle und funktionelle Anomalien im Herzen vorliegen. Das transthorakale Echokardiogramm (TTE) ist eine nichtinvasive Ultraschalluntersuchung, die Bilder des Herzens mit Schallwellen erzeugt. Es enthält Informationen zur Schätzung der linksventrikulären Ejektionsfraktion (LVEF), der ventrikulären Abmessungen und Volumina, des Wandvolumens, der Herzkammergeometrie und der regionalen Wandbewegung. Bei Patienten mit systolischer Herzinsuffizienz beträgt die LVEF normalerweise weniger als 40%.2 Weitere Studien, die in Verbindung mit dem TTE zur Beurteilung der Ätiologie, des Schweregrads und möglicher arzneimittelbedingter Behandlungseffekte bei Herzinsuffizienz verwendet werden, umfassen eine Röntgenaufnahme des Brustkorbs zu Studienbeginn, eine 12-Kanal-Elektrokardiographie sowie Messungen des natriuretischen Peptids des Gehirns, der Serumelektrolyte und der Nierenfunktion. Diese Studien sind wichtig, da Angehörige der Gesundheitsberufe sie als Grundlage für die Bestimmung verwenden können, ob ein Patient eine Änderung des klinischen Status erfahren hat.2,6
BEHANDLUNG DER SYSTOLISCHEN HERZINSUFFIZIENZ
Nichtpharmakologisch
Die Kontrolle der Risikofaktoren wie Bluthochdruck, Diabetes mellitus, Dyslipidämien, atherosklerotische Gefäßerkrankungen und Schilddrüsenerkrankungen können das Fortschreiten der Herzinsuffizienz und des Herzumbaus verlangsamen.2,4,6 Patienten mit Herzinsuffizienz sollten Influenza- und Pneumokokken-Impfstoffe erhalten, um das Risiko von Begleiterkrankungen wie Atemwegsinfektionen zu verringern.2 Der bedeutendste modifizierbare Risikofaktor wären risikoreiche Verhaltensweisen wie Rauchen, Alkohol und illegaler Drogenkonsum.2,7
Natriumrestriktion (?2 gramm / Tag) hilft bei der Verringerung der Volumenüberlastung und kann die Verwendung von Diuretika verringern. Darüber hinaus ermöglicht das tägliche Wiegen den Patienten, den Volumenstatus zu beurteilen, auf dem die diuretische Dosisanpassung basieren kann. Jedoch haben keine Studien die Wirkung der diätetischen Natriumbeschränkung auf die Morbidität oder Mortalität untersucht.7,8 Es wurde gezeigt, dass körperliche Aktivität die Mortalität und Krankenhauseinweisungen bei Patienten mit stabiler Herzinsuffizienz verringert. Die Einschränkung der Bewegung fördert die körperliche Dekonditionierung, die zur Belastungsintoleranz eines Patienten beitragen kann. Schließlich spielt die Einhaltung der Diät und der therapeutischen Medikation eine wichtige Rolle bei der Prävention akuter Krankenhauseinweisungen.2,7
Pharmakologisch
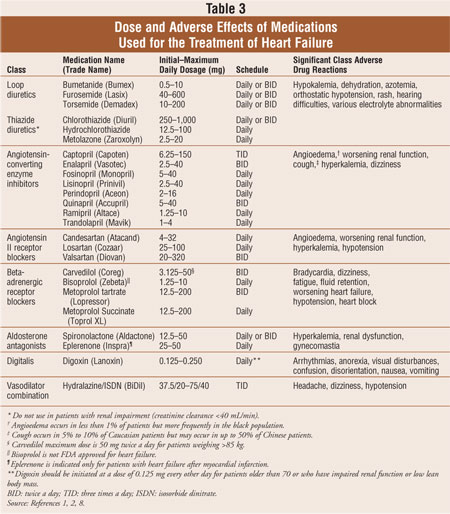
Die meisten Patienten mit Herzinsuffizienz werden mit einer Standardkombination aus drei Medikamenten behandelt: einem Schleifendiuretikum, einem Angiotensin-Converting-Enzym (ACE) -Hemmer oder einem Angiotensin-II-Rezeptorblocker (ARB) und einem beta-adrenergen Rezeptorblocker.1,2 Diuretika sind die Hauptstütze bei der Verringerung der Symptome einer Volumenüberlastung bei Herzinsuffizienz, während ACE-Hemmer, ARBs und Betablocker nachweislich die Morbidität und Mortalität senken.2 Aldosteronantagonisten sind als Zusatztherapie bei Patienten mit symptomatischer Herzinsuffizienz der NYHA-Klasse III oder IV oder nach frühem akutem MI bei Patienten mit eingeschränkter linksventrikulärer Funktion und klinischem Nachweis einer Herzinsuffizienz indiziert. Wenn Patienten weiterhin symptomatisch sind, kann Digoxin zum Standardmedikament hinzugefügt werden, um die Symptome zu reduzieren, Krankenhausaufenthalte zu verringern und die Belastungstoleranz zu verbessern. Arzneimittel zur Behandlung von Herzinsuffizienz werden in Tabelle 3 erörtert. Änderungen des Lebensstils und medikamentöse Therapien bei systolischer Herzinsuffizienz sollen die Morbidität und Mortalität verringern, das Fortschreiten des Herzumbaus verhindern und die Lebensqualität der Patienten verbessern.2
Diuretika:Die Hauptstütze der symptomatischen Behandlung der Volumenüberlastung bei Herzinsuffizienz, Diuretika, verringern die Flüssigkeitsretention, die zu Lungenstauung, peripherem Ödem, Jugularvenendistention und / oder erhöhtem Körpergewicht führt. Schleifendiuretika, die in der Henle-Schleife wirken, erhöhen die Natriumausscheidung im Serum um 20% bis 25%, verbessern die Elimination von freiem Wasser und behalten ihre Wirksamkeit bei Patienten mit eingeschränkter Nierenfunktion bei.1,2 Im Gegensatz dazu verringern Thiaziddiuretika die Natriumausscheidung um 5% bis 10%, verstärken die Elimination von freiem Wasser und verlieren ihre Wirksamkeit bei Patienten mit chronischer Nierenerkrankung (Kreatinin-Clearance < 40 ml / min). Schleifendiuretika sind die bevorzugten Mittel zur Behandlung von Herzinsuffizienz, aber Thiazide können bei Patienten mit leichter Flüssigkeitsretention und Bluthochdruck angewendet werden. Diuretika sowie ACE-Hemmer und Betablocker werden zur Anwendung bei allen Patienten mit Herzinsuffizienz im Stadium C empfohlen.2 Studien haben gezeigt, dass Diuretika die Herzfunktion, die Symptome und die Belastungsintoleranz bei Patienten mit Herzinsuffizienz verbessern. Die langfristigen Auswirkungen von Diuretika auf die Mortalität sind jedoch unbekannt.1,2,8
ACE-Hemmer: ACE-Hemmer reduzieren die Aktivität des Renin-Angiotensin-Aldosteron–Systems, indem sie die Umwandlung von Angiotensin I in Angiotensin II blockieren und eine Angiotensin-II-induzierte Vasokonstriktion verhindern. Sie hemmen auch die Aldosteronfreisetzung, was zu einer Abnahme der Natrium- und Flüssigkeitsretention führt. Diese kombinierten Effekte reduzieren sowohl die Vor- als auch die Nachlast und verlangsamen das Fortschreiten des kardialen Remodelings.1,2 ACE-Hemmer können auch eine zusätzliche Aktivität mit verstärkter Kinin- und Kinin-vermittelter Prostaglandinproduktion aufweisen.2 Über 30 klinisch kontrollierte Studien zur Bewertung der Wirksamkeit von ACE-Hemmern haben gezeigt, dass ACE-Hemmer das Sterberisiko und das kombinierte Sterberisiko und Krankenhausaufenthalte verringern. Alle Patienten mit linksventrikulärer systolischer Herzinsuffizienz sollten einen ACE-Hemmer erhalten, es sei denn, dies ist kontraindiziert (Angioödem, bilaterale Nierenarterienstenose, Serumkalium > 5, 5 mEq / l, Schwangerschaft, symptomatische Hypotonie oder instabiles Nierenversagen). ACE-Hemmer sollten in niedrigen Dosen eingeleitet und je nach Verträglichkeit der Nebenwirkungen langsam titriert werden.1,2,8
ARBs: Im Vergleich zu Studien mit ACE-Hemmern haben weniger klinische Studien die Anwendung von ARBs bei Patienten mit Herzinsuffizienz untersucht; daher sind diese Mittel Patienten mit nachgewiesener Intoleranz gegenüber ACE-Hemmern vorbehalten. ARBs blockieren selektiv Angiotensin II durch Bindung an den Angiotensin-Rezeptor. ARBs reduzieren die Schwere der Kinin-Nebenwirkungen wie Husten und Angioödem, obwohl Angioödeme mit diesen Mitteln berichtet wurden. Die Zugabe eines ARB zur Standardtherapie, einschließlich eines ACE-Hemmers, kann die Größe des linken Ventrikels und die Anzahl der Krankenhauseinweisungen verringern.2,8 Eine Studie zeigte, dass Candesartan, das einem ACE-Hemmer zugesetzt wurde, die kardiovaskulären Todesfälle verringerte.9 Eine andere Studie mit Valsartan bei Patienten mit MI und Herzinsuffizienz zeigte jedoch keinen Nutzen von Valsartan und einem ACE-Hemmer zusammen im Vergleich zu einem ACE-Hemmer allein.10 Die Verschreibung einer Kombination aus ACE-Hemmern, ARBs und Aldosteronantagonisten wird aufgrund des Risikos einer Hyperkaliämie nicht empfohlen. ARBs bleiben eine Alternative zu ACE-Hemmern bei der Behandlung von Herzinsuffizienz.2
Beta-adrenerge Rezeptorblocker: Es wurde gezeigt, dass drei Arten von Betablockern die Mortalität senken: Retardmetoprolol und Bisoprolol, die selektiv Beta-1-Rezeptoren blockieren, und Carvedilol, das Alpha-1-, Beta-1- und Beta-2-Rezeptoren blockiert.1,2,8 Im Vergleich dazu zeigte eine Studie, dass kurzwirksames Metoprolol im Vergleich zu Carvedilol eine geringere Wirkung hatte, die verwendete Metoprololdosis jedoch niedriger war als die empfohlene Zieldosis.11 Zusätzlich zur Standardtherapie haben Betablocker eine kombinierte Verringerung von Tod und Krankenhausaufenthalt bei Herzinsuffizienz gezeigt. Betablocker hemmen Nebenwirkungen des sympathischen Nervensystems und überwiegen die negativen inotropen Wirkungen.2 Insgesamt sollten Betablocker in sehr niedrigen Dosen eingeleitet, in Abständen von mindestens zwei Wochen langsam titriert und nicht abrupt abgesetzt werden, da das Risiko einer Verschlechterung der Herzinsuffizienz und einer akuten Dekompensation besteht.1,2
Aldosteronantagonisten: Aldosteronantagonisten blockieren den Aldosteronrezeptor im distalen Tubulus des Nephrons, was zu Kaliumretention, Natriumausscheidung und leichter Diurese führt. Aldosteronantagonisten werden bei Patienten mit mittelschwerer oder schwerer Herzinsuffizienz und kürzlicher Dekompensation oder bei Patienten mit linksventrikulärer Dysfunktion kurz nach einem MI empfohlen.2 Wenn einem ACE-Hemmer bei Patienten mit Herzinsuffizienz der NYHA-Klassen III und IV niedrig dosiertes Spironolacton zugesetzt wurde, verringerte sich die Gesamtmortalität der Patienten um 30%.12 Eine weitere Studie zeigte, dass Eplerenon innerhalb von 14 Tagen nach MI zu einer Verringerung der Mortalität bei Patienten mit LVEF um weniger als 40% führte, obwohl keine Daten zur Anwendung von Eplerenon bei der Behandlung von Herzinsuffizienz vorliegen, die auf andere Ursachen als MI zurückzuführen ist.13 Der prominenteste limitierende Faktor von Aldosteron-Antagonisten ist potenziell lebensbedrohliche Hyperkaliämie.2,14 Die Hyperkaliämie nimmt progressiv zu, wenn das Serumkreatinin 1,6 mg / dl überschreitet, obwohl Studien Aldosteronantagonisten bei Patienten mit Serumkreatinin der Einstiegsklasse von 2,0 bis 2,5 mg / dl untersucht haben. Darüber hinaus sollten Aldosteronantagonisten bei Patienten mit Serumkalium von mehr als 5,0 mEq pro Liter vermieden werden.2
Digoxin: Digoxin ist ein Herzglykosid, das die Kontraktilität des Herzens erhöht, indem es die Natrium-Kalium-Adenosintriphosphatase (ATPase) -Pumpe hemmt und so das intrazelluläre Kalzium erhöht. Digoxin wird zur symptomatischen Kontrolle bei Patienten mit leichter bis mittelschwerer Herzinsuffizienz der NYHA-Klasse II oder III.2 empfohlen In einer Post-hoc-Analyse verringerten Digoxin-Serumkonzentrationen zwischen 0, 5 und 0, 9 ng / ml die Krankenhauseinweisungen; Konzentrationen über 1 ng / ml waren jedoch mit einem Trend zu einer erhöhten Mortalität im Vergleich zu Placebo verbunden.15 Während Studien nicht gezeigt haben, dass Digoxin die Mortalität senkt, kann dieses Mittel Symptome und Belastungsintoleranz verbessern, Krankenhausaufenthalte reduzieren und die allgemeine Lebensqualität verbessern.2,8,16
Vasodilatator-Kombination: Die Empfehlung von Hydralazin und Isosorbiddinitrat (ISDN) in Kombination ist Patienten vorbehalten, die nachweislich keinen ACE-Hemmer oder ARB vertragen können. In einer kürzlich durchgeführten Studie mit einer Kohorte afroamerikanischer Patienten mit symptomatischer NYHA III- oder IV-Herzinsuffizienz führte die Zugabe von Hydralazin und ISDN-Kombination zur Standardtherapie (d. H. Ace-Hemmer, Diuretikum und Betablocker) zu einer Verbesserung des Überlebens um 43% und einer Verringerung des Risikos des ersten Krankenhausaufenthalts um 33% im Vergleich zu Placebo.17 Theoretisch kann die Kombination aus Hydralazin und ISDN die Bioverfügbarkeit von Stickoxid verbessern.2 Die Kombination ISDN und Hydralazin (BiDil) ist von der FDA nur für Afroamerikaner als Zusatztherapie zur Standardtherapie bei Herzinsuffizienz zugelassen.18 Hydralazin ist ein Arteriolen-Vasodilatator, der die Nachlast verringert, während ISDN ein venöser Vasodilatator ist, der die Vorlast verringert. Diese Kombination von Vasodilatatoren wird gegenüber ACE-Hemmern oder ARBs nicht bevorzugt, da sie unerträgliche Nebenwirkungen wie Kopfschmerzen oder Schwindel und Compliance-Probleme wie verpasste Dosen haben kann, aber sie kann als Zusatztherapie für die afroamerikanische Bevölkerung verwendet werden.2
Alternative Arzneimittel: Weißdornblätter mit Blüten, auch als Crataegus-Extrakt bekannt, wurden bei leichter Herzinsuffizienz (NYHA II) empfohlen. Durch In-vitro-Studien haben Weißdornblätter positive inotrope Wirkungen, gefäßerweiternde Eigenschaften und einen erhöhten koronaren Blutfluss gezeigt. Studien haben eine Verbesserung der subjektiven Symptome bei Patienten mit leichter Herzinsuffizienz gezeigt. Aufgrund der digitalisähnlichen Wirkungen sollten Patienten, die sowohl Crataegus-Extrakt als auch Digitalis einnehmen, engmaschig überwacht werden. Unerwünschte Nebenwirkungen waren gastrointestinale Symptome, Herzklopfen, Brustschmerzen und Schwindel.19,20
Ein weiteres alternatives Arzneimittel, das zur Behandlung von Herzinsuffizienz eingesetzt wurde, ist Coenyzme Q10, ein fettlösliches Vitamin. Einige Studien zeigten, dass Coenzym Q10 zu einer Verbesserung der Häufigkeit von Krankenhausaufenthalten, Dyspnoe und Ödemen führte.21 Eine randomisierte, doppelblinde, placebokontrollierte Studie zeigte jedoch keinen Unterschied zwischen Coenyzme Q10 und Placebo in Bezug auf LVEF, Belastungstoleranz oder maximalen Sauerstoffverbrauch bei Patienten mit Herzinsuffizienz.22 Dokumentierte Nebenwirkungen von Coenzym Q10 waren Magen-Darm-Beschwerden, Hypoglykämie und Hypotonie.21 Klinische kontrollierte Studien mit Crataegus-Extrakt und Coenyzme Q10 sind im Gange, um die Wirksamkeit und Sicherheit bei der Behandlung von Herzinsuffizienz zu bewerten.20,21
SCHÄDLICHE MEDIKAMENTE BEI HERZINSUFFIZIENZ
Mehrere Medikamentenklassen können Herzinsuffizienz verschlimmern und sollten vermieden werden. Antiarrhythmika, außer Amiodaron oder Dofetilid, können eine kardiodepressive und proarrhythmische Wirkung auf das Herz haben, was zu einer akuten Dekompensation führt.1,2 Kalziumkanalblocker der ersten Generation wurden mit erhöhten kardiovaskulären Ereignissen und einer Verschlechterung der Herzinsuffizienz in Verbindung gebracht. Die neueren, langwirksamen Kalziumkanalblocker Amlodipin und Felodipin scheinen sicher zu sein, aber keine Studien haben eine statistisch signifikante Reduktion der Mortalität gezeigt.2,8,23 Die Thiazolidindione wurden mit Gewichtszunahme und Flüssigkeitsretention in Verbindung gebracht, was möglicherweise zu Herzinsuffizienz führte oder eine akute Exazerbation der Herzinsuffizienz auslöste. Ödeme treten jedoch häufiger auf, wenn Thiazolidindione in Kombination mit einer Insulintherapie angewendet werden.24,25 Daher werden Thiazolidindione bei Patienten mit Diabetes mellitus und Herzinsuffizienz der NYHA-Klasse III oder IV nicht empfohlen.25-27 NSAIDs verursachen Natriumretention und periphere Vasokonstriktion, was zu einer akuten Exazerbation der Herzinsuffizienz führt. Darüber hinaus verringern sie die Wirksamkeit und erhöhen das Toxizitätsrisiko durch ACE-Hemmer und Diuretika. Es besteht die Möglichkeit einer Arzneimittelwechselwirkung, wenn Aspirin in Kombination mit ACE-Hemmern angewendet wird.2
ROLLE DES APOTHEKERS
Ein Verständnis der Vorteile der medikamentösen Therapie bei Herzinsuffizienz kann zu einer optimalen pharmazeutischen Versorgung führen. Apotheker können Patienten helfen, Hochrisikoverhalten wie Rauchen, Alkoholkonsum und illegalen und schädlichen OTC-Drogenkonsum zu identifizieren und zu lindern. Darüber hinaus müssen Apotheker die Patienten auf das Fortschreiten des Krankheitszustands, einschließlich Anzeichen und Symptome einer Herzinsuffizienz, überwachen und die Patienten dazu ermutigen, ihr Gewicht zu bestimmen.
Patienten zu ermutigen, diätetische Einschränkungen, Übungsrichtlinien und Medikamentenregime für Herzinsuffizienz einzuhalten, sollte die Priorität eines Apothekers sein. Die Nichteinhaltung therapeutischer Medikamente wurde mit einem Anstieg der Mortalität in Verbindung gebracht und kann mit unerwünschten Nebenwirkungen von Medikamenten zusammenhängen. Apotheker sollten Patienten überwachen und ermutigen, ihre Medikamente einzuhalten, um die Mortalität zu senken. Durch die Überwachung und Aufklärung von Patienten und anderen Angehörigen der Gesundheitsberufe über arzneimittelbedingte Nebenwirkungen können Apotheker dazu beitragen, die Einhaltung von Medikamenten zu erhöhen. Darüber hinaus müssen Apotheker Alternativen zu Medikamenten wie ACE-Hemmern kennen und mit anderen Gesundheitsdienstleistern die damit verbundenen Mortalitätsvorteile besprechen, um eine optimale pharmazeutische Versorgung zu gewährleisten und das Mortalitätsrisiko zu senken.
Patienten und Gesundheitsdienstleister sind sich möglicherweise des Zusammenhangs zwischen gängigen Medikamenten und Exazerbationen der Herzinsuffizienz nicht bewusst. Da einige gängige OTC-Medikamente, einschließlich NSAIDs, bei Patienten mit Herzinsuffizienz kontraindiziert sind, ist die Aufklärung des Patienten darüber, warum er oder sie diese Medikamente nicht einnehmen sollte, eine weitere wichtige Rolle für Apotheker. Apotheker müssen Patienten überwachen und sich mit Gesundheitsdienstleistern und Patienten über schädliche Wechselwirkungen zwischen Medikamenten und Krankheiten beraten, die zu Krankenhausaufenthalten führen können.
1. Klein L, O’Connor CM, Gattis WA, et al. Pharmakologische Therapie bei Patienten mit chronischer Herzinsuffizienz und verminderter systolischer Funktion: überprüfung von Versuchen und praktischen Überlegungen. In: Am J Cardiol. 2003;91(Ergänzung):18F-40F.
2. Hunt SA, Abraham WT, Chin MH, et al. ACC / AHA 2005 Guideline Update für die Diagnose und Behandlung von chronischer Herzinsuffizienz bei Erwachsenen: ein Bericht des American College of Cardiology / American Heart Association Task Force für Praxisrichtlinien (Schreibausschuss zur Aktualisierung der Richtlinien von 2001 für die Bewertung und Behandlung von Herzinsuffizienz). Website des American College of Cardiology. Erhältlich unter: www.acc.org/clinical/guidelines/failure//index.pdf .
3. Francis GS, Gassler JP, Sonnenschein EH. Pathophysiologie und Diagnose von Herzinsuffizienz. In: F., et al., eds. Hurst ist das Herz. 10. Aufl. New York, NY: McGraw-Hügel; 2001: 655-686.
4. Metra M, Nodari S, et al. Prävention und Behandlung von chronischer Herzinsuffizienz bei Risikopatienten. In: Am J Cardiol. 2003;91(Ergänzung):10F-17F.
5. Chobanian AV, Bakris GL, Schwarz HR, et al. Siebter Bericht des Joint National Committee zur Prävention, Erkennung, Bewertung und Behandlung von Bluthochdruck. Hypertonie. 2003;42:1206-1252.
6. Frigerio M, Oliva F, Turazza FM, Bonow RO. Prävention und Behandlung von chronischer Herzinsuffizienz bei asymptomatischen Patienten. In: Am J Cardiol. 2003;91(Ergänzung):4F-9F.
7. Colonna P, Sorino M, D’Agostino C, et al. Nichtpharmakologische Versorgung von Herzinsuffizienz: Beratung, diätetische Einschränkung, Rehabilitation, Behandlung von Schlafapnoe und Ultrafiltration. In: Am J Cardiol. 2003;91(Ergänzung):41F-50F.
8. McConaghy JR., Smith SR. Ambulante Behandlung der systolischen Herzinsuffizienz. Am Fam Arzt. 2004;70:2157-2164.
9. Young JB, Dunlap ME, Pfeffer MA, et al. Mortalitäts- und Morbiditätsreduktion mit Candesartan bei Patienten mit chronischer Herzinsuffizienz und linksventrikulärer systolischer Dysfunktion: Ergebnisse der CHARM-Studien zur linksventrikulären Ejektionsfraktion. Durchblutung. 2004;110:2618-2626.
10. Cohn JN, Tognoni G. Eine randomisierte Studie mit dem Angiotensin-Rezeptor-Blocker Valsartan bei chronischer Herzinsuffizienz. In: N Engl J Med. 2001;345:1667-1675.
11. Poole-Wilson PA, Swedbery K, Cleland JG, et al. Vergleich von Carvedilol und Metoprolol zu klinischen Ergebnissen bei Patienten mit chronischer Herzinsuffizienz in der europäischen Studie Carvedilol oder Metoprolol (COMET): randomisierte kontrollierte Studie. Lancet. 2003;362:7-13.
12. Pitt B, Zannad F, Remme WJ, et al. Die Wirkung von Spironolacton auf Morbidität und Mortalität bei Patienten mit schwerer Herzinsuffizienz. In: N Engl J Med. 1999;341:709-717.
13. Pitt B, Remme W, Zannad F, et al. Eplerenon, ein selektiver Aldosteronblocker, bei Patienten mit linksventrikulärer Dysfunktion nach Myokardinfarkt. In: N Engl J Med. 2003;348:1309-1321.
14. Aldacton . Chicago, IL: Pharmacia Corporation; Juli 2003.
15. Ahmed A, Rich MW, Liebe TE, et al. Digoxin und Reduktion der Mortalität und Hospitalisierung bei Herzinsuffizienz: eine umfassende Post-hoc-Analyse der DIG-Studie. Eur Herz J. 2006;27:178-186.
16. Die Digitalis Investigation Group. Die Wirkung von Digoxin auf Mortalität und Morbidität bei Patienten mit Herzinsuffizienz. In: N Engl J Med. 1997;336:525-533.
17. Taylor AL, Ziesche S, Yancy C, et al. Kombination von Isosorbiddinitrat und Hydralazin bei Patienten mit Herzinsuffizienz. In: N Engl J Med. 2004;351:2049-2057.
18. BiDil . Lexington, MA: Nitromed Inc.; August 2005.
19. In: De Smet PA. Pflanzliche Heilmittel. In: N Engl J Med. 2002;347:2045-2056.
20. Holubarsch CJ, Colucci WS, Meinertz T, et al. Überleben und Prognose: Untersuchung von Crataegus-Extrakt WS 1442 bei kongestiver Herzinsuffizienz (SPICE) – Begründung, Studiendesign und Studienprotokoll. Eur J Herz versagen. 2000;2:431-437.
21. Bonadkar RA, Guarneri E. Coenzym Q10. Am Fam Arzt. 2005;72:1065-1070.
22. Khatta M, Alexander BS, Krichten CM, et al. Die Wirkung von Coenyzme Q10 bei Patienten mit kongestiver Herzinsuffizienz. In: Ann Intern Med. 2000;132:636-640.
23. De Vries RJM, Van Veldhuisen DJ, Dunselman PHJM. Wirksamkeit und Sicherheit von Kalziumkanalblockern bei Herzinsuffizienz: Konzentrieren Sie sich auf neuere Studien mit Dihydropyridinen der zweiten Generation. Am Herz J. 2000;139:185-194.
24. Edelsberg JS, Hagiwara M, et al. Verwendung von Thiazolidindionen und Risiko einer Herzinsuffizienz bei Menschen mit Typ-2-Diabetes. Diabetes-Versorgung. 2003;26:2983-2989.
25. In: Hollenberg NK. Überlegungen zum Management fluiddynamischer Probleme im Zusammenhang mit Thiazolidindionen. Bin J Med. 2003;115:111S-115S.
26. Avandia . Research Triangle Park, NC: GlaxoSmithKline; August 2005.
27. Actos . Lincoln, IL: Takeda Pharmaceutical American Inc.; August 2004.
Um diesen Artikel zu kommentieren, kontaktieren Sie [email protected] .