Polysilikater
Ortosilikatjonen, SiO44 –
ortosilikatjonen finns inte i en mängd olika mineraler. Det är en mycket stark bas som inte kommer att kvarstå i vattenlösning. I naturen finns det i kombination med sura katjoner i olösliga salter.
| |
||
| fenacit | Be2SiO4 | & nbsp |
| willemite | Zn2SiO4 | & nbsp |
| zirkon | ZrSiO4 | & nbsp |
| granat | (M2+) 3 (m3+) 2 (SiO4) 3 | M2 + = Ca, Mg, Fe M3 + = Al, Cr, Fe |
oligomera Polysilikater
polymera silikatstrukturer kräver överbryggande (2-koordinat) oxygener. För att göra plats för ett överbryggande syre måste en oxid avlägsnas från ”mottagande” kisel.
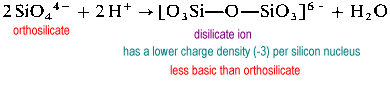
disilikatjonen är ovanlig i naturen. Det finns bara i det sällsynta mineralet thortveitite, Sc2Si2O7. Större strukturer som trisilikat och tetrasilikat är extremt snabba.
cykliska oligomera Polysilikater
istället för att bilda långa öppna kedjestrukturer, kommer kedjans ändar att länka eliminera oxidjoner.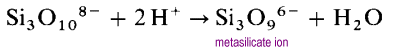
metasilikatjonen är en oligomer av den okända SiO32-Jonen. I dessa strukturer har varje kisel två överbryggande och två terminala syreatomer. Det finns en -2 laddningstäthet per kiselatom. De vanligaste cykliska polysilikaten är de cykliska trimererna, (SiO3)36-och de cykliska hexamererna (SiO3) 612 -.

den cykliska trimeren finns i mineralet benitoit, BaTi(Si3O9.

Kedjepolysilikater
linjära (1-D) polymerer med formel (SiO3)n2n – kan bildas via överbryggande oxygener. I dessa strukturer finns en laddning av -2 per kiselatom. En grupp mineraler som kallas pyroxenmineralerna har denna typ av struktur.
| |
|
| enstatit | MgSiO3 |
| diopsite | CaMgSi2O6 |
| spodimen | LiAlSi2O6 |
| pollucit | CsAlSi2O6 |
linjära kedjor kan kopplas sida vid sida om en oxidjon ersätts med en annan överbryggande syreatom. Om denna länkning sker vid alternativa SiO3-grupper i varje kedja, en dubbelkedjig struktur (Si4O11)n6n-resultat. I sådana strukturer finns en minskning av laddningen och antalet syreatomer per kiselatom.
krokidolit, ett asbestmineral med formeln Na2Fe5 (OH)22, är ett exempel. Detta mineral är fibröst i naturen och har Brand-och värmebeständiga egenskaper som härrör från anjonens långkedjiga struktur.
Ark Polysilikater
när sida-till-sida-länkning av kedjor fortsätter på obestämd tid elimineras fler oxider och en 2-D-polymer resulterar. Dessa 2-D polymerer kallas arksilikater och innehåller n4n-anjonen. Mineraler som innehåller denna struktur klyvs lätt i tunna ark.
| |
|
| micas | muskovit och biotit |
| lermineraler | montmorillonit, kaolinit, kina lera och vermikulit |
| talk | & nbsp |
| täljsten | & nbsp |
| krysotil asbest | & nbsp |
3-D polymera silikater
ark är kopplade till en 3D-polymer när alla oxidjoner elimineras (alla oxygener i strukturen överbryggar). Denna struktur innehåller oladdad oxid kiseldioxid n som inte längre är basisk utan snarare en sur oxid. Många vanliga mineraler innehåller denna struktur: kvarts, flint, jaspis, onyx, ametist, Citrin, agat och kalcedon.
successiva polymerisationssteg:
- resulterar i successiv minskning av o / Si-atomförhållandet
- 4:1 i ortosilikat
- 2:1 i kiseldioxid

 placera följande mineraler i ordning med ökande polymerisationsgrad. För att göra detta, beräkna o/Si-förhållandet (ju lägre förhållandet desto mer polymeriserat strukturen.
placera följande mineraler i ordning med ökande polymerisationsgrad. För att göra detta, beräkna o/Si-förhållandet (ju lägre förhållandet desto mer polymeriserat strukturen.
- pyrofyllit, Al2Si4O10 (OH)2
- grunerit, Fe7Si8O22 (OH) 2
- spessartit, Mn3Al2Si3O12
- bustamite, CaMn( SiO3)2
glas
när sur kiseldioxid reageras med basiska oxider vid mycket höga temperaturer (~1700 0C) och kyldes sedan för snabbt för polysilikatjonerna för att möjliggöra fomation av de ordnade polysilikatjonerna som finns i mineraler för att bilda. Resultatet är bildandet av ett amorft fast ämne eller glas. Glasögon kännetecknas av att de inte har någon bestämd fryspunkt.
enkelt glas tillverkas genom smältning (smältning) sand med natriumbikarbonat och kalksten (källor till basiska oxider Na2O och CaO). Under denna process bryts kisel-syrebroar.
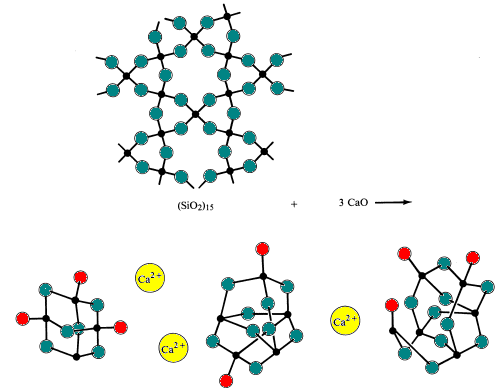
specialglas tillverkas genom att ändra sammansättningen av sura och basiska oxider i glaset.
- Pyrex ™ glas är ovanligt resistent mot termisk chock. För att göra det 10-25% B2O3, en sur oxid, införlivas i strukturen.
- färgade glasögon innehåller D-blockmetalloxider som en del av den grundläggande oxidkomponenten
- inkorporering av strontiumoxid ger ett glas som absorberar röntgenstrålarna från färg-TV-apparater
- de fina optiska egenskaperna som behövs i kameralinser kan erhållas genom införlivande av La2O3
Läs mer om glasögon här och på Corning Museums Glasresursplats.
Jordkemi
det faktum att alltmer polymeriserade polysilikatjoner har minskande laddningar per kisel vilket resulterar i sänkt basicitet har viktiga konsekvenser i markkemi.
ju mer basisk polysilikatanjon av ett mineral, desto lättare kommer det att reagera med svaga syror och genomgå förväxling.
regnvatten är något surt på grund av upplöst CO2 även i frånvaro av svavel och kväveoxider.
med tiden kommer regnvatten att reagera med de mindre polymeriserade silikatanjonerna för att ersätta oxidjoner med överbryggande syre vilket ger ett mer polymeriserat silikat. Oxiderna avlägsnas som vattenmolekyler.
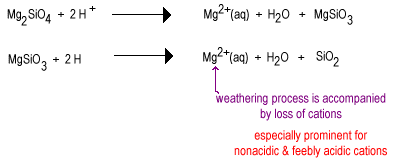
mellanstadiet av vittring har stora mängder lagersilikater såsom lera samt lite kvarts. Dessa jordar tenderar att hittas i tempererade områden under ett skydd av gräs eller träd. Sådana jordar är mindre bördiga än nybevattnade deserjord på grund av förlusten av det icke-sura växtnäringsämnet K+. Lagersilikater som finns i mellanliggande jordar kan fortfarande hålla katjoner på sina negativt laddade ytor som kan släppas när växten behöver dem. Dessa jordar finns i de fortfarande ganska bördiga majs-och vetebältena.
isomorf Substitution
Polysilikatjoner har negativa laddningar som måste motverkas av lämpliga katjoner. De terminala oxygenerna har negativt laddade ytor som approximerar nära packade ytor med negativ laddning. Katjonerna som behövs för att neutralisera polysilikatets negativa laddning är belägna i skikten mellan kedjorna eller skikten eller i de tetraedriska eller oktaedriska hålen som finns i 3D-gitteret.
de typer av katjoner som finns i en viss form av polysilikat beror på ”
- storleken på katjonerna
- laddningen av katjonerna
eftersom det finns en hel del uppsättningar joner som har samma laddning och mycket liknande radier, finns det liten anledning till att en av dessa matchade typer av joner föredras framför en annan när ett mineral bildas vid kylning av smält magma.
till exempel olivin, som har en idealisk sammansättning av Mg2SiO4, kan innehålla varierande procentsatser av isomorf undertextning av Fe2+ (radie 92 pm) i stället för ett lika stort antal Mg2+ joner (radie 86 pm).
första principen för isomorf Subsititution
andra Priciple av isomorf Substitution
isomorf substitution ökar antalet möjliga substitutioner i silikater.
exempel
- K+kan ersättas med de sällsynta RB+-och Tl+-jonerna samt de vanliga Ba2+
- Ca2+kan ersättas med Sr2+(132 pm), Na+(116 pm), Y3+(104 pm), La3+ (117 pm) och den sjätte perioden f-blockjoner (100-117 pm)
- Si4+ kan ersättas med den vanliga AL3+ Jonen (67 PM)
katjonerna i de flesta silikatmineraler ersätts i stor utsträckning vilket gör icke-ekonomiska malmer för de flesta element. Det finns diagonala förhållanden mellan element (särskilt under den andra perioden) till elementen en grupp till höger och en period nere på bordet.
 vilka av följande mineraler kan uppstå genom isomorfa substitutionsprocesser i leucit, K (AlSi2O6)?
vilka av följande mineraler kan uppstå genom isomorfa substitutionsprocesser i leucit, K (AlSi2O6)?
- K (YSi2O6)
- Rb (AlSi2O6)
- Ba (BeSi2O6)
- Ba (AlSi2O6)
tips: Det finns två grundläggande principer för joniska föreningar som måste observeras vid isomorf substitution:
- den totala laddningen för alla katjoner måste vara lika med den totala laddningen för alla anjoner.
- för att substitutionen ska vara isomorf måste det totala antalet katjoner som går in vara ungefär lika med den totala laddningen för alla katjoner som ersätts.