mål
formålet med disse retningslinjer er at lette beslutningstagningen i behandlingen af patienter med en ensom lungeknude (SPN).1-3 disse retningslinjer er ikke beregnet til at være stive, da behandlingen af SPN er et eksempel på, hvordan estimering af sandsynligheden for malignitet (PM), Adgang til de forskellige diagnostiske og terapeutiske teknikker og patientpræferencer arbejder sammen for at forme den optimale beslutning. Denne proces bør individualiseres i den kliniske indstilling og for hver enkelt situation. Da tilgængeligheden til nogle diagnostiske teknikker kan variere, afhængigt af indstillingen, foreslås en generel strategisk algoritme (Fig. 1) med to alternativer afhængigt af graden af tilgængelighed til positronemissionstomografi (PET) (Fig. 2 og 3). Anbefalingerne er klassificeret efter styrke (stærk 1, svag 2) baseret på forholdet mellem de forudsigelige fordele og risiciene for patienten; og kvaliteten af det videnskabelige bevis, så højt (a), moderat (B), lavt (C) eller meget lavt (D), ifølge KARAKTERSYSTEMET.4 En oversigt over disse anbefalinger2,4,6 er angivet i tabel 1. Den udvidede version af disse anbefalinger er tilgængelig som et online supplement sammen med yderligere tabeller og Tal (R) (tillæg 1).
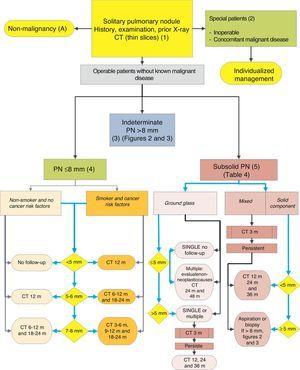
algoritme til styring af PN: initial klassificering og observation af SPN-8mm og subsolid SPN. m: måneder, PN: lungeknude; SPN: ensom lungeknude; CT: computertomografi, inklusive tynde sektioner. Opfølgning med CT med lav stråling, forudsat at der ikke påvises vækst. Tal og bogstaver i parentes henviser til afsnittene i teksten, hvor de diskuteres.
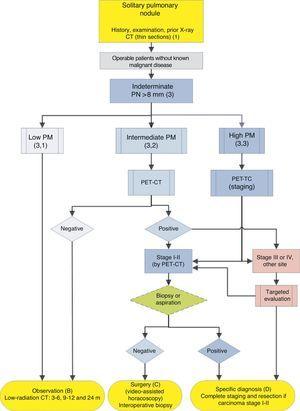
algoritme til styring af PN > 8mm: klinisk indstilling med nem adgang til PET-CT. m: måneder, PN: lungeknude; SPN: ensom lungeknude; PET-CT: positronemissionstomografi med computertomografi; PM: Sandsynlighed for malignitet; CT: brystcomputertomografi, inklusive tynde sektioner. Opfølgning med CT med lav stråling, forudsat at der ikke påvises vækst. Tal og bogstaver i parentes henviser til afsnittene i teksten, hvor de diskuteres.
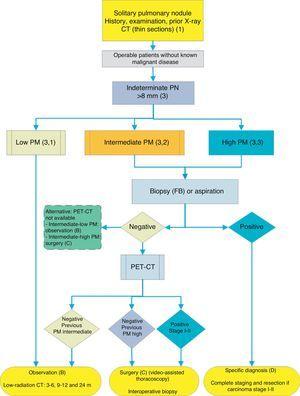
algoritme til styring af PN > 8mm: klinisk indstilling med vanskelig adgang til PET-CT eller præference for cytohistologisk undersøgelse af SPN. FB: fiberoptisk bronkoskopi og guidet biopsi; m: måneder; SPN: ensom lungeknude; PET-CT: positronemissionstomografi med computertomografi; PM: Sandsynlighed for malignitet; CT: brystcomputertomografi, inklusive tynde sektioner. Opfølgning med CT med lav stråling, forudsat at der ikke påvises vækst. Tal og bogstaver i parentes henviser til afsnittene i teksten, hvor de diskuteres.
anbefalinger til håndtering af ensom lungeknude.
| anbefaling | Gradea |
| SPN indledende evaluering | |
| alle beslutninger om styring af et SPN skal indeholde udtalelse og præferencer for den passende informerede patient | 1C |
| Evaluer stabilitet eller vækst i tidligere radiologiske undersøgelser, hvis de er tilgængelige | 1C |
| stabilitet i mere end 2 år i fast SPN og godartet forkalkning indikerer godignans og kræver ikke yderligere evaluering | 2C |
| CT, med tynde sektioner gennem læsion af interesse, er afgørende for den indledende evaluering af ubestemt SPN | 1B |
| SPN hos patienter med tidligere eller samtidig malignitet kræver individualiseret behandling og evaluering | 1C |
| SPN ‘er hos inoperable patienter kræver individualiseret behandling | 1C |
| SPN’ er vil blive klassificeret som faste knuder> 8 mm, faste knuder på 8 mm og subsolide knuder | 1B |
| faste knuder> 8mm | |
| skal klassificeres efter PM: lav ( (>65%) | 2C |
| SPN med lav PM: radiologisk observation | 2C |
| radiologisk observation: CT med lav stråling uden kontrast ved 3-6, 9-12 og 24 måneder | 2C |
| SPN med mellemliggende PM: PET-CT | 1B |
| negativ PET-CT: radiologisk observation | 2C |
| SPNs med mellemliggende PM: biopsi-aspiration er et acceptabelt alternativ | 2C |
| ingen histologisk diagnose: PET-CT | 1B |
| biopsi eller aspiration anbefales i tilfælde af uoverensstemmelse mellem klinisk PM og billeddannelsestest | 2C |
| mistænkt etiologi, der kræver medicinsk behandling (f. eks. tuberkulose) | |
| patienter, der nægter eller gør indsigelse mod diagnostisk kirurgi | |
| SPN med høj PM: ledelse i henhold til formodet diagnose af tidligt stadium karcinom | 2C |
| SPN med høj PM: FB med bronchial undersøgelse og transbronchial biopsi | 2D |
| ikke-diagnosticeret SPN med PM større end lav hos operable patienter: SPN resektion | 2C |
| anbefalet teknik: videoassisteret thoracoscopy | 1C |
| Interoperativ biopsi for at etablere type resektion | |
| Subcentimeter PNs forbundet med SPN bør ikke være kontraindikation for kurativ karcinomkirurgi, medmindre der er bekræftelse af metastase. | 2C |
| SPNmm | |
| Observationsstrategi efter anbefalinger fra Fleischner Society (Fig. 1) | 2C |
| lavdosis, ikke-kontrast CT-overvågning | 1C |
| Subsolid SPNs | |
| Intervention i henhold til anbefalinger fra Fleischner Society (tabel 2) | 1B til 2C |
| lavdosis, ikke-kontrast CT-overvågning | 1C |
FB: fibroskopi; PN: lungeknude; SPN: ensom lungeknude; PET: positronemissionstomografi; PM: Sandsynlighed for malignitet; CT: computertomografi.
anbefalingsklasse efter styrke (stærk 1 eller svag 2) og kvaliteten af videnskabelig dokumentation som høj (a), moderat (B), lav (C) eller meget lav (D) i henhold til KARAKTERSYSTEMET.
introduktion: koncept og etiologi
SPN er defineret som en enkelt, sfærisk, tydelig, radiologisk opacitet med en lang akse på 30 mm, primært omgivet af luftet lunge og uden tilknyttet atelektase, hilarforstørrelse eller pleural effusion.1-3 SPN ‘ er kan observeres på røntgenbillede af brystet eller computertomografi i brystet (CT) udført for at studere andre sygdomme eller til diagnostisk screening for lungekræft (LC).3,6,7 millimetriske knuder (8 mm i diameter) 1,2,6 og subsolide knuder (SSN ‘ er) 2,5 (Fig. 4), der kræver forskellig styring, kan 5-7 detekteres på CT (Fig. 1). SSN ‘ er inkluderer både malede glasknuder og delvist faste knuder, der kombinerer en malet glaskomponent med en fast komponent.2,5–7
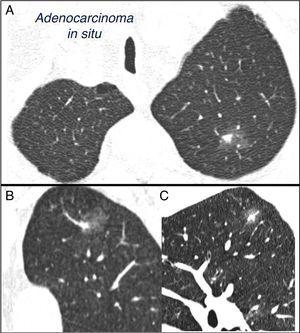
blandet subsolid ensom lungeknude i venstre øvre lap. Brystcomputertomografi med 2 mm tynde sektioner hos en patient med en ensom lungeknude i venstre øvre lobe. Aksial Skive (A) i øvre lapper og koronal (B) og sagittal (C) rekonstruktioner i venstre øvre lap. En 18 mm jordglas ensom lungeknude observeres med en 7 mm fast komponent i det indre. Resektion ved videoassisteret thoracoscopy afslørede adenocarcinom.
Nodler anslås at forekomme med en hastighed på 1 eller 2 pr.1000 røntgenstråler.1,3,8 forekomsten af knuder på CTs udført hos voksne rygere til LC-screening er meget høj, mellem 20% og 50%, og er generelt mindre end 10 mm i størrelse; forekomsten i successive årlige CTs er 10%.1,3,6,7
ved evaluering af SPNs med CT findes andre små knuder ofte. Når de er få, eller en er klart dominerende, bør de betragtes som uafhængige SPN ‘ er, da selv om situationen er LC, er ledsagende subcentimeter knuder ofte godartede.1,2,6,7 desuden er den ondartede knude i op til 20% af tilfældene ikke den største.7
SPN er den radiologiske manifestation af mange sygdomme3 (online Appendiks–tabel 1s). Imidlertid er de fleste knuder forårsaget af pulmonale maligniteter, granulomer og hamartomer.1 forekomsten af malignitet varierer mellem serier8,9: fra mellem 5% og 70% afhængigt af om tallene hentes fra sundhedskontrol eller undersøgelser af diagnostiske teknikker og i mindre grad i SPN ‘ er påvist i LC-screeningsprogrammer, hvor forekomsten er 1% -10% afhængigt af nodulestørrelse.3,7 PM for SPNs øges især hos patienter med tidligere tumorsygdom.3,10
de fleste maligne SPN ‘ er er LC, oftest adenocarcinomer og store cellecarcinomer.2,3 i ondartet SSN er de mest almindelige stammer i adenocarcinomspektret,5, 11, 12, der spænder mellem atypisk adenomatøs hyperplasi i de mindste knuder, adenocarcinom in situ, minimalt invasivt adenocarcinom og invasive adenocarcinomer, hvis en fast komponent er til stede, især i slimhindeknuder og dem med lepidisk vækst.5,11,12
diagnostiske teknikker i undersøgelsen af ensom pulmonal NoduleChest computertomografi
denne teknik er langt bedre end standard røntgen i evalueringen af SPNs.2,3 Det kan detektere andre knuder og mediastinale lymfadenopatier, diagnosticere pseudonoduler (ekstraparenchymale læsioner) og hjælpe med at planlægge nodulebiopsi eller aspiration. I nogle tilfælde kan det give en specifik diagnose, såsom arteriovenøse misdannelser, mycetomer, afrundet atelektase eller hamartomer. Derfor er CT vigtig som indeksundersøgelse til undersøgelse af SPNs.2
Noduleforbedring eller optagelse af kontrastmateriale viste en følsomhed på 98% for malignitet med en cutoff på > 15 Hounsfield-enheder (HU) og en specificitet på 58%.13 Dette gælder for sfæriske, homogene SPN ‘ er>8 mm uden fedt, calciumkavitation eller nekrose. Dette kan være værdifuldt i Centre med ekspertise inden for denne teknik, men på grund af introduktionen af PET er dets anvendelse ikke blevet udbredt.3
positronemissionstomografi
en af de vigtigste indikationer for PET-CT med 18F-D-glucose er undersøgelsen af SPNs. Gennemsnitlig følsomhed for faste SPN ‘ er>10–15mm er 0.93 (konfidensinterval 0,90-0,95) og gennemsnitlig specificitet er 0,8 (CI 0,74–0,85).2,14,15 falske negativer på PET-CT er forbundet med defekt teknik, tumordiameter7mm, carcinoide tumorer, subsolide knuder og nogle adenocarcinomer, især in situ, minimalt invasiv, lepidisk vækst eller slimhindeadenocarcinomer.2,3 falske positiver er mere almindelige og inkluderer inflammatoriske og infektiøse læsioner, såsom granulomer, tuberkulose, mycosis eller pneumonier.2,16
PET-CT er mest anvendelig i SPNs>8mm med mellemliggende PM: en negativ undersøgelse reducerer PM kraftigt.3 i en positiv PET-CT indikerer en større standardiseret optagelsesværdi (SUV) større tumoraggressivitet og en dårligere prognose for patienten, skønt dens reducerede specificitet og dermed chancen for en falsk positiv skal tages i betragtning.17,18 det kan også hjælpe med at vælge det mest effektive og tilgængelige sted for biopsi og hjælpe om nødvendigt med planlægning af strålebehandling.19 PET-CT bidrager til kræft staging2,3 ved at evaluere mediastinal og systemisk metastase, og anbefales i mange LC management retningslinjer.17,18,20 i disse anbefalinger anvendes PET-CT på to måder: som et værktøj til karakterisering af SPN og som en iscenesættelsesteknik i SPN ‘ er med høj PM.
Cytohistologisk prøveudtagning af ensom Lungeknudecomputeret tomografi, Radioskopi eller ultralydstyret fin nål Transthoracic Aspiration
en analyse af litteraturen om 48 undersøgelser viser god følsomhed, 86% (CI 84% -88%), til diagnose af malignitet og meget god specificitet, 99% (CI 98% -99%).21 i SPN ‘ er mindre end 15 mm er følsomheden lavere ved 70% -82%.2,22 i godartet sygdom er specificiteten også lavere.21 Den gennemsnitlige hastighed for pneumothoraks var 15%, hvoraf 7% krævede dræning.2,21,23 Transthoracic aspiration er kontraindiceret i tilfælde af dårlig patientsamarbejde, meget kompromitteret åndedrætsfunktion eller enkelt lunge eller hæmoragisk diatese og i nærvær af emfysem eller omfattende bullae i noduleområdet. Mellem 4% og 50% af resultaterne giver ikke en diagnose, og op til 20% er falske negativer.2 Hvis PM er høj, er antallet af sande negativer det samme som for falske negativer, så det er ikke nyttigt til at udelukke malignitet.2
fiberoptisk bronkoskopi og tilknyttede teknikker
i LC er det diagnostiske udbytte af CT-styret transbronchial aspiration (TBA) for at målrette knudeområderne i henhold til serien fra 20% til 80% og er lavere i SPNs mindre end 20 mm, hvor det gennemsnitlige udbytte er 30%.2 i godartede SPN ‘ er er udbyttet 10%. Denne teknik er mere effektiv i større centrale knuder (>20 mm) ved hjælp af et luftbronkogram.2,24 der er ringe risiko for TBA: pneumothoraks,2%, 2 og mere sjældent, hæmoptyse eller hæmatomer. Selvom det diagnostiske udbytte for SPNs er mindre end det, der opnås med transthoracic fin needle aspiration-biopsi (fnab), kan en endobronchial undersøgelse udføres inden planlægning af LC-operation.25 ultrafine bronkoskopier for bedre adgang til læsioner, styreskeder til placering af tang, radial sonde ultralyd endobronchoscopy, elektromagnetisk navigationsbronkoskopi og navigationsbronkoskopi er alle under evaluering, idet de er teknikker, der gør det muligt at lede tangene mod knuden og dermed forbedre udbyttet.2,26 disse teknikker er blevet sammenlignet i en meta-analyse26: det kombinerede udbytte var 70%, bedre end i tidligere radioskopi-styrede serier, og udbyttet af de individuelle teknikker varierede fra 68,5% til 73%, skønt der blev observeret stor variation og heterogenitet blandt undersøgelserne. Udbyttet var lavere i SPNs20mm, 61% mod 80% i > 20mm.kombination af teknikker kan forbedre udbyttet noget.2 som det fremgår af disse data, overgår ingen teknik især andre med hensyn til udbytte, og anbefalingen er, at hvert center skal bruge de teknikker, som både udstyr og ekspertise er tilgængelige for.
videoassisteret Thoracoscopy og Thoracotomy
SPNs kan resekteres ved hjælp af disse teknikker.2 Hvis SPN ‘ erne er små eller placeret dybt i parenchymen, kan de tidligere farves eller markeres med en krogtråd, generelt med CT-styret transthoracic punktering. Risikoen ved videoassisteret thoracoscopy er lav, og dødeligheden er meget sjælden (mindre end 1%), sygelighed er lav, og det diagnostiske udbytte er godt, svarende til thoracotomi, men med lavere dødelighed.2 Når SPN er LC, hvis patientens kliniske situation tillader det, indikeres anatomisk resektion: generelt anbefales lobektomi og mediastinal node dissektion.2,20,27
estimering af sandsynligheden for malignitet
maligne SPN ‘er adskiller sig fra godartede SPN’ er i visse kliniske og radiologiske aspekter, beskrevet mere detaljeret i den udvidede version af disse retningslinjer (se online supplement). De faktorer, der er tættest forbundet med malignitet, er størrelsen af SPN, marginfunktioner, tæthed, patientalder, akkumuleret tobaksforbrug, eksistensen af anden malignitet og påvisning af vækst.2,3,6,7,10,28-30 Central, laminær eller total forkalkning af SPN betragtes som et godt kriterium for godartethed,2,3 ligesom radiologisk stabilitet i mere end 24 måneder, hvilket indebærer en fordoblingstid på over 730 dage. Dette kriterium er ikke gyldigt for SSN, for hvilket observationen skal udvides til mindst 3 år.1-3, 5
de fleste klinikere estimerer PM intuitivt, men flere SPN–modeller og klassificeringsregler er blevet foreslået7,28-32, Og der er endda regnemaskiner tilgængelige online (Online Appendiks-tabel 2s) eller som en smartphone-applikation (MedCalc medical calculator). Tabel 2s i online-tillægget giver et sæt formler opnået fra forskellige logistiske modeller, og figur 1s er et gyldigt nomogram for SPN ‘ er i røntgenbillede af brystet.
denne estimering af PM styrer den efterfølgende diagnostiske proces.1,2,31 logisk set, når man forudsiger malignitet, gennemgås resultaterne af alle undersøgelsesteknikker,inklusive PET-CT-resultaterne,31, 32 biopsi-eller aspirationsresultaterne og evaluering af vækst, hvis passende billeder er tilgængelige.
sammen med PM skal de forudsigelige fordele og risici ved behandlingen vurderes. Der er en tærskel PM, der indikerer observation, dvs.enhver PM, for hvilken den mest rimelige mulighed er prospektiv observation af stabiliteten eller væksten af SPN; og en tærskel for kirurgi, for hvilken kirurgi klart anbefales, da sandsynligheden for kræft i det tidlige stadium er høj. Disse tærskler afhænger af de forventede fordele; for eksempel sandsynligheden for helbredelse eller behandlingsrespons i tilfælde af ondartet sygdom, de kirurgiske risici, der kan variere mellem patienter og patientens personlige holdning og præference.1
sekventiel evaluering af den ensomme lungeknude
målet med at evaluere en SPN er at diagnosticere og behandle SPN ‘ er, der repræsenterer aktiv sygdom, især LC, DA 5-års overlevelse er 70% -80% i sygdom i det tidlige stadium.20 et andet mål er at undgå at underkaste patienter med granulomer, hamartomer og andre godartede læsioner dyre og risikable behandlinger. Der er ingen enkelt accepteret procedure. Nøgleelementerne til evaluering er estimering af sandsynligheden for malignitet, tilgængelighed til forskellige diagnostiske tests og klinikernes ekspertise i disse teknikker og patientens præferencer.1,2
Fig. 1-3 viser den foreslåede sekventielle evaluering af SPN: Fig. 1 beskriver den indledende klassificering efter SPN-størrelse, densitet og soliditet eller subsoliditet, der adskiller patienter, der har brug for individualiseret behandling, og dem, der kan diagnosticeres fra starten. Fig. 2 og 3 beskriver den foreslåede strategi for ubestemte faste SPN ‘ er>8 mm, afhængigt af om adgang til PET-CT er let (Fig. 2) eller vanskeligere (Fig. 3).
klinisk og indledende radiologisk evaluering (1)
den indledende undersøgelse omfatter historie, undersøgelse og evaluering af de radiologiske træk sammen med sammenligning med alle tilgængelige tidligere røntgenstråler2, 31: anbefalingsklasse,1C.
hvis der ikke er tegn på stabilitet i > 2 år eller godartet forkalkning, er CT med tynde sektioner gennem den interesserede knude angivet2: anbefalingsklasse, 1b.
nogle knuder kan klassificeres i denne fase som godartede,hvis de ses at være stabile i mere end 2 år eller fra deres egenskaber på CT2, 31: anbefalingsklasse, 2C.
i ubestemt SPN ‘ er fortsætter overvågningen afhængigt af patientens egenskaber og de radiologiske træk ved knuden.
patienter i særlige situationer (2)
en patients situation kan betragtes som speciel på grund af en ændring i den etiologiske frekvens eller PM for SPN, eller fordi proceduren er begrænset til ikke-invasive teknikker på grund af kirurgiske risici.
patienter med tidligere eller samtidig malign sygdom. PM af lungeknuder, hvad enten det er enkelt eller flere,stiger meget hos disse patienter,3, 10, selvom de er små.6 muligheden for metastase er endnu større, hvis SPN ‘ erne ikke tidligere var til stede. Ikke desto mindre, når SPN ‘ erne er subcentimetriske, er op til en tredjedel godartede, så diagnosen skal bekræftes med biopsi, aspiration eller videoassisteret thoracoscopy, før man nægter potentielt helbredende behandlinger: anbefalingsklasse, 2C.2,10 SPN ‘ er hos immunkompromitterede patienter vil kræve individualiseret evaluering, og biopsi eller aspiration foretrækkes.33
hos inoperable patienter er evalueringen af SPN begrænset. Biopsi eller aspiration er indiceret i tilfælde med høj PM eller positive resultater på PET, til vejledning af kemoterapi eller strålebehandling, hvis behandling af LC er påkrævet: anbefalingsklasse, 2C.
ensom lungeknude>8 mm (3) (fig. 2 og 3)
det første trin er at klassificere patienten i henhold til den estimerede PM: lav (??5%), Mellem-eller høj (> 65%) 1,2,29,31: anbefalingsgrad, 1C.
lav sandsynlighed for malignitet (3, 1)
lav PM er den, der anslås til mindre end 5%.2,31 dette inkluderer SPN ‘er, der stadig er små (
mm), med forskellige margener, yngre patienter (2,28–32,34 i disse tilfælde anbefales radiologisk observation2,31: anbefalingsklasse, 2C.
også inkluderet er SPN’ er med mellemliggende PM og negativ PET-CT eller dem, der evalueres med FNAB, der viser ikke-malignitet2: anbefalingsklasse, 2C.
mellemliggende Sandsynlighed for malignitet (3, 2)
en PM på mellem 5% og 65% betragtes som mellemliggende.2,28 – 32,34 i disse tilfælde anbefales PET-CT, der er ikke-invasiv, lav risiko og med høj diskriminerende effekt (Fig. 2): anbefalingsklasse, 1b. et negativt resultat reducerer PM betydeligt, og observation kan anbefales; et positivt resultat øger PM og klassificerer det som højt.2,31
afhængig af tilgængelighed og ventetider for udførelse af PET-CT er en alternativ procedure CT-styret FNAB eller fiberoptisk bronkoskopi (FB)-TBA styret af radioskopi, ultralydendoskopi eller elektromagnetisk eller virtuel navigation (Fig. 3): grad af anbefaling, 2C. Biopsi-indstillingen anbefales især, når den kliniske PM og fund på billeddannelsestest er uoverensstemmende, når der er mistanke om etiologier, der kræver specifik medicinsk behandling (f. eks.tuberkulose), eller hvis patienten er ugunstig for operation2: anbefalingsgrad, 2C.
gentagelse af biopsi-eller aspirationsteknikker i tilfælde af indledende negativitet anbefales kun, når PM for SPN er høj, og diagnosen inden operationen anses for nødvendig, eller når kirurgi er kontraindiceret.
hvis resultatet er negativt, anbefales PET-CT (Fig. 3): anbefalingsgrad, 1b.hvis der ikke er nogen PET-CT tilgængelig, ville alternativet være overvågning med CT, især hvis FNAB var negativ eller operation.
høj sandsynlighed for malignitet (3, 3)
PM er høj hos patienter over 50 år med en historie med rygning eller radiologiske træk ved malignitet: SPN> 15 mm, spekulerede marginer eller heterogen densitet. SPN ‘ er, der er hypermetaboliske på PET-CT, dem, der er steget i størrelse eller ændret form, og dem med en cytologi eller lungebiopsi, der tyder på malignitet, er også af høj PM.2,28-32,34
i disse tilfælde anbefaler nogle forfattere direkte diagnostisk-terapeutisk kirurgi, og andre foretrækker biopsi teknikker.2,31 i den population, Der er valgt af denne algoritme, når patienter med andre kræftformer er udelukket, er de fleste SPN ‘ er lungekræft. Anbefalingen er således,at de administreres som sådan,2 med PET-CT anbefales som en metode til iscenesættelse17, 18: anbefalingsklasse, 2C.
histologisk diagnose før kirurgi kan bestemmes ved hjælp af FB-TBA, en teknik, der også tillader en evaluering af bronchialtræet, inden operationen udføres, eller af fnab. Et negativt resultat reducerer ikke PM tilstrækkeligt til at udelukke resektion af SPN. Effekten af forsøg på prækirurgisk diagnose af SPN med høj PM, i klinisk fase i eller II med CT og PET-CT, forudsat at patienten kan betjenes, er ikke undersøgt. Af denne grund tilbydes dette som en mulighed i algoritmen (Fig. 2), selvom prækirurgisk evaluering med FB er en standard praksis: anbefalingsgrad, 2C.
hvis PET-CT afslører mediastinale eller ekstrathoraciske optagelser, der tyder på metastase, skal disse evalueres inden resektionskirurgi.17,18 hvis SPN med høj PM er negativ på PET-CT, reduceres PM ikke tilstrækkeligt til at anbefale observation,2 og resektion via videoassisteret thoracoscopy anbefales: anbefalingsklasse, 2C. lavere optagelse antyder imidlertid en bedre prognose og mindre sandsynlighed for formidling, noget der kan tages i betragtning, hvis patienten har en stærk indsigelse mod operation.3,31
i den foreslåede strategi bør evalueringen af et SPN med høj PM afsluttes med en specifik diagnose eller diagnostisk terapeutisk resektion (Fig. 2 og 3).
ensom lungeknude mm (4)
forekomsten af disse SPN ‘ er er meget høj i CT-studier, og PM er lav, medmindre der er en historie med tidligere eller samtidig metastaserende tumor.2,6 de er vanskelige at få adgang til for at opnå biopsier og PET-CT og dynamisk CT har meget lav følsomhed.2,6 en observationsstrategi, der følger anbefalingerne fra Fleischner Society6 (Fig. 1) foreslås under hensyntagen til asymptomatiske patienter uden samtidig ondartet sygdom: anbefalingsklasse, 2C.
opfølgning udføres med lavdosis, ikke-kontrast CT6: anbefalingsklasse, 1C. igen skal patienten informeres, og hans/hendes præferencer skal tages i betragtning.2
Subsolid lungeknude (5)
disse er jordglasknuder, rene eller med en fast komponent5 (Fig. 4). Bestemmelse af en subsolid knude kræver tynde sektioner, fortrinsvis på 1 mm, da små faste SPN ‘ er i 5 mm CT-skiver kan forekomme som formalet glas.2,5
SSN ‘ er er vanskelige at få adgang til for biopsi eller aspiration, og følsomheden af PET-CT er lav.5,35 på den anden side er deres PM relativt høj, 15% eller mere for SPN i formalet glas og over 50% for en blandet knude.5 Det er også vanskeligere at fastslå ændringer i størrelse eller volumen af disse læsioner under overvågning, og maligniteter, der forekommer i denne form,kan være indolente i en længere periode, hvorfor observationsperioden skal være længere, 5 dvs.mindst 3 år.
da mange godartede etiologier er akutte eller subakutte processer, foreslås en indledende observationsstrategi med CT efter 3 måneder, da nogle SPN ‘ er kan forsvinde. Hvis de vedvarer, bestemmes strategien af størrelsen på SPN, hvis de har en fast komponent, og hvis de er enkelt eller flere (Fig. 1). Tabel 2 indeholder detaljerede anbefalinger som foreslået af Fleischner Society.5
håndtering af Subsolide knuder.
| grad af Anbefalinga | ||||
| formalet glas SPN | ||||
| ≤5mm | ingen opfølgning | 1C | ||
| >5mm | CT ved 3 måneder | vedvarende | årlig Ctfølg >3 år | 1B |
| delvist fast SPN (fast del) | ||||
| mm | CT efter 3 måneder | vedvarende | årlig Ctfølg >3 år | 2C |
| ≥5mm | CT ved 3 måneder | vedvarende | biopsi, resektion, PET-CT if fast del > 10mm | 1B |
| flere jordglas PN | ||||
| ≤5mm | overvej ikke-ondartede årsager | CT ved 2 og 4 år | 1C | |
| >5mm | CT ved 3 måneder | vedvarende | årlig Ctfølg > 3 år | 1B |
| multipel PN med fast komponent | CT 3 måneder | vedvarende | biopsi, resektion, især hvis fast del > 5mm | 1C |
PN: lungeknude; SPN: ensom lungeknude; PET: positronemissionstomografi; CT: computertomografi. Anbefalingsklassen er den, der er foreslået af Fleischner Society,5 baseret på KARAKTERSYSTEMET. Anbefalingerne fra American College of Chest Physicians2 reducerer styrken af anbefalingen med en klasse. CT til evaluering skal være fint skive og opfølgning lavdosis CT.
anbefalingsklasse efter styrke (stærk 1 eller svag 2) og kvaliteten af videnskabelig dokumentation som høj (a), moderat (B), lav (C) eller meget lav (D) i henhold til KARAKTERSYSTEMET.
endelige muligheder efter evaluering
- A.
diagnose af godignancy: Patienter med en specifik diagnose på CT, såsom hamartomer, arteriovenøse misdannelser, cystiske læsioner, afrundet atelektase, mycetomer, pseudonoduler eller forkalkede knuder, eller som har kriterier for godartethed, f. eks. dokumenteret stabilitet i mindst 2 år, i tilfælde af faste knuder eller mindst 3 år for subsolide knuder2, 3: anbefalingsklasse, 2C.
- B.
radiologisk observation: angivet i SPNs med lav PM eller med mellemliggende PM, når PET-CT er negativ, anbefalingsklasse, 2C. Dette kan også angives i udiagnosticeret SPNs, hvis risikoen for operation er meget høj, eller hvis patienten nægter operation: anbefalingsklasse, 2C.
for SPN>8 mm med lav PM anbefales CT-overvågning efter 3-6 måneder, igen efter 9-12 måneder og igen efter 24 måneder.2 der er specifikke strategier for SPN kur 8mm og SSN2, 5, 6 (Fig. 1 og tabel 2): grad af anbefaling, 2C. overvågning CTs skal udføres med lav dosis og ikke-kontrast: grad af anbefaling, 1C.
- C.
diagnostisk-terapeutisk kirurgi: Operable patienter med udiagnosticeret SPN og PM større end lav bør tilbydes resektion: anbefalingsklasse, 2C. selvom videoassisteret thoracoscopy er den valgte metode (anbefalingsklasse, 1C), vil hvert kirurgisk team beslutte den bedste tilgang. Intraoperativ biopsi anbefales til gennemførelse af passende resektion i tilfælde af LC: anbefalingsklasse, 1C.
- D.
specifik diagnose: dette er den etiologiske diagnose af SPN. Hvis LC diagnosticeres, anvendes specifikke lokale iscenesættelses-og behandlingsprotokoller.20
algoritmen kan ikke afsluttes uden at understrege, at den optimale beslutning skal indeholde udtalelsen og præferencerne for den passende informerede patient2: anbefalingsklasse, 1C.
interessekonflikt
forfatterne erklærer, at de ikke har nogen interessekonflikt.