a prosztaglandinok biológiai hatások széles skáláját mutatják, és hatásuk a természetben előforduló vegyületek közül a legváltozatosabb. E megfigyelés ellenére ez a lipidcsoport markáns szerkezet-aktivitás specifitást mutat, amelyet elsősorban a ciklopentanongyűrű-szubsztitúciók és a prosztánsav-oldalláncok telítetlenségének mértéke határoz meg. A prosztaglandinokra adott sejtválaszt a plazmamembrán receptorokkal való kölcsönhatásuk közvetíti.
a PG receptorokat kezdetben a természetes és szintetikus agonisták funkcionális aktivitása alapján osztályozták, az antagonistákat pedig a következő kategóriákba sorolták: DP, EP, FP, IP és TP. Az első betű a prosztaglandin típusát jelöli, a P betű pedig a ” prostanoid.”30 később a kötési analízissel és molekuláris klónozással végzett vizsgálatok megerősítették a különböző receptortípusok, valamint az EP (EP1–4) három vagy négy altípusának jelenlétét. A plazmamembrán prosztaglandin receptorok a G-fehérjéhez kapcsolt receptorok szupercsaládjába tartoznak, amelyet hét transzmembrán-átívelő régió jellemez.31 a prosztaglandin receptorok intracelluláris második hírvivői közé tartozik a cAMP, a protein-kináz C és a kalcium.30,31 a különböző receptorok figyelemre méltó specifitást mutatnak az eikozanoidra, legalább 100-szor előnyben részesítik a ligandumot. Magas koncentrációban a PGE2 és a PGF2a kölcsönhatásba lép a DP receptorral; hasonlóképpen a PGF2a aktiválja az EP receptort, míg a PGD2 és a PGE2 nagy koncentrációban lép kölcsönhatásba az FP receptorral. A legtöbb szövet receptorok keverékét tartalmazza, amely úgy tűnik, hogy egy adott prosztaglandin különböző dózisokban gyakran ellentétes hatásainak alapja.
a prosztaglandinok szerepe a Gonadotropin szekrécióban
a prosztaglandinoknak a gonadotropin-releasing hormon (GnRH) szekréció szabályozásában betöltött fiziológiai szerepére vonatkozó legfrissebb adatokat tettek közzé.32,33 számos jelentés azt sugallja, hogy a prosztaglandinok, különösen a PGE2, stimuláló hatást fejtenek ki a gonadotropin felszabadulására, amely hatást úgy tűnik, hogy a hipotalamusz szintjén fellépő hatás közvetíti. Kimutatták, hogy a PGE2 stimulálja a GnRH felszabadulását a hipotalamuszból, és az állatok endogén GnRH semlegesítésére antiszérummal történő előkezelése megakadályozza az LH PGE2 által kiváltott felszabadulását.34 ezenkívül úgy tűnik, hogy a PgE1 és a PGE2 a növekedési hormon felszabadulásának leghatásosabb stimulátorai a tenyésztett adenohipofízis sejtekből.35 a PGB, a PGA1, a PGA2, a PGB2, a PGF1 és a PGF2 szintén aktív stimulátorok, de hatásuk fiziológiás dózisoknál nem látható. Általában úgy tűnik, hogy a prosztaglandinok nem stimulálják a gonadotropin szekrécióját az agyalapi mirigy közvetlen hatásával.
további bizonyítékok arra utalnak, hogy a prosztaglandinok befolyásolhatják a gonadotropin szekrécióját (közvetlenül a hipotalamuszra hatva) prosztaglandin-szintetáz inhibitorokat, például indometacint alkalmazó vizsgálatokból származnak, amelyek nyilvánvalóan csökkentik a gonadotropin szekrécióját.36 az, hogy a prosztaglandinok hipotalamusz-felszabadító tényezők útján hatnak, két megfigyelés alapján nyilvánvaló:
- nőstény és hím patkányok LH-releasing hormon (LHRH) antiszérummal történő előkezelése rontotta a PGE2 (patkányonként 100 mg) azon képességét, hogy fokozza az LH szekréciót.36
- a PGE2 közvetlen beadása a patkány agykamrájába utánozta a prosztaglandinok intravénás hatását a gonadotropin szekréció stimulálására.36
további megállapítások meggyőző támogatást nyújtanak annak a koncepciónak, miszerint a PGE2 a medián eminencia szintjén hat az LHRH felszabadulásának kiváltására. Ezt az állítást tovább erősíti az a megállapítás, hogy a medián eminenciaszövet nagyobb mennyiségben tartalmaz endogén prosztaglandinokat, mint a bazális hipotalamusz régiók. Hím patkányokból nyert medián eminenciaszint fragmentumok in vitro inkubációjából nyert adatok azt mutatták, hogy a noradrenalin és a dopamin stimulálja az LHRH és a PGF2a egyidejű felszabadulását. Ezt a hatást az indometacin blokkolja, ami arra utal, hogy az intraneuronálisan előállított prosztaglandinok a katekolamin által stimulált LHRH felszabadulás mediátorai. Ezeket az érdekes megállapításokat részletesebben tárgyalja Ojeda és munkatársai.36
ovuláció és prosztaglandinok
miután felfedezték,hogy az indometacin és az aszpirin (a prosztaglandin szintézis inhibitorai) blokkolhatják az ovulációt,33, 37 azt javasolták, hogy a prosztaglandinok részt vesznek a petefészek follikuláris szakadásának folyamatában. Ezt az állítást tovább erősítette az a megállapítás, hogy a pgf2a antiszérum intraovarian injekciója szintén gátolta az ovulációt.38 jelenleg jelentős mennyiségű bizonyíték van arra, hogy a follikuláris prosztaglandin képződés fokozódik az ovuláció során, és hogy ez az emelkedés a gonadotropinoktól függ.39
a gonadotropinok középciklusbeli túlfeszültsége stimulálja a follikuláris eikozanoid bioszintézist egy cAMP által közvetített folyamat, amely a gén aktiválásától függ, de független a szteroidogenezistől. Úgy tűnik, hogy az LH a domináns fiziológiás hipofízis gonadotropin, amely felelős az ovuláció indukciójáért, és valószínűnek tűnik, hogy az LH hatását a tüszőrepedésre a proteolitikus enzimeket, oxigéngyököket és prosztaglandinokat szekretáló leukociták közvetítik. Az indometacin például blokkolja az ovulációt, amelyet általában nagy dózisok indukálnak humán koriongonadotropin in vivo. A prosztaglandinok közvetíthetik az LH stimuláló hatásait az “ovulációs enzimekre”, például a proteázra vagy a kollagenázra.40 fennáll annak a lehetősége is,hogy a prosztaglandinok kontraktilis választ válthatnak ki a tüszőfalban, 41 amely jelenleg ismert, hogy kontraktilis elemeket, például miozint és aktint tartalmaz. Úgy tűnik, hogy a plazminogén aktivátor vagy valamilyen más proteáz lényegében részt vesz a tüszőrepedésben, 42 és nyilvánvaló, hogy ennek a fehérjének a szekréciója összefügg a follikuláris prosztaglandin bioszintézisének LH által kiváltott emelkedésével, bár rámutattak arra, hogy ez a két esemény nem függ egymástól. A prosztaglandin hatásának lehetséges mechanizmusa a tüszőrepedésben a 6. ábrán látható.
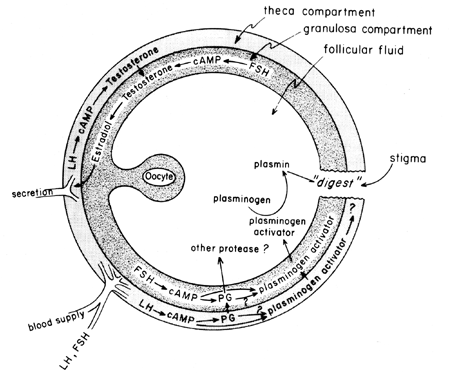 Fig. 6. A prosztaglandin hatásának lehetséges mechanizmusa a follikuláris szakadásban.(Behrman HR: prosztaglandinok a hypothalamo-hipofízisben és a petefészek működésében. Ann Rev Physiol 41:685, 1979)
Fig. 6. A prosztaglandin hatásának lehetséges mechanizmusa a follikuláris szakadásban.(Behrman HR: prosztaglandinok a hypothalamo-hipofízisben és a petefészek működésében. Ann Rev Physiol 41:685, 1979)
a prosztaglandinok szerepe a luteális funkcióban: Luteolízis és menstruáció
rejtély az a mechanizmus, amellyel az emberi sárgatest kialakulása után 10-12 nappal visszafejlődik. Mivel a korai megállapítás, hogy a pgf2a luteolitikus volt a patkányokban és sok más szubprimát fajban,43 jelentős kutatási erőfeszítéseket tettek a menstruációs szabályozás lehetőségének vizsgálatára a PGF2a – val.A PGF2a a corpus luteum funkcionális regresszióját indukálja egy receptor által közvetített folyamat, amely kezdetben független a petefészek vagy a luteális véráramlás változásaitól.32 perceken belül a PGF2a lebontja az aszkorbinsavat,44 leválasztja az elfoglalt LH receptort az adenilát-ciklázról, és csökkenti a gonadotropin szállítását a kapillárisokból a luteális sejtbe.
a vonatkozó szakirodalom áttekintése számos ellentmondó jelentést tár fel a PGF2a emberekre gyakorolt hatásairól. Néhány tanulmány a keringő progeszteron szintjének átmeneti csökkenését rögzítette a PGF2a által, 45 bár más vizsgálatok nem mutattak ki ilyen hatást normálisan ovuláló nőknél.46,47 tekintettel a feltételezett pgf2a receptorok létezésére a humán corpus luteumban, 48 azt indokolták, hogy a pgf2a intravénás infúziójával a luteolízis sikertelensége valószínűleg a gyors pulmonalis metabolizmus következménye. A pgf2a humán corpus luteumba történő közvetlen befecskendezésével járó későbbi vizsgálatok progeszteron megvonást váltottak ki, amelynek mélypontja egybeesett a korai menstruáció kezdetével.49 ezek az eredmények arra utalnak, hogy endogén petefészek prosztaglandinokra (vagy valamilyen más luteolitikus szerre) lehet szükség a luteális regresszióhoz. Ez megvalósíthatónak tűnik annak a megfigyelésnek a fényében, hogy az emberi luteális funkció függetlennek tűnik a méh kontrolljától, mivel sem a méh, sem a hüvely vagy a petevezeték veleszületett hiánya nem befolyásolja a petefészek ciklikusságát.51 Az emberi luteális szövet minden bizonnyal képes prosztaglandinok termelésére, amint azt az in vitro kísérletek52 mutatják; azonban a petefészek megnövekedett PGF2a szintjének a luteális regresszióval való korrelálására tett kísérletek a késői luteális fázisban nem voltak sikeresek.53 úgy tűnik, hogy az emberi menstruációs ciklusban a petefészek PGF2a termelése csak röviddel az ovuláció után fokozódik.54 az is nyilvánvaló azonban, hogy a pgf2a koncentrációja mindig magasabb a petefészek stroma szövetében a korai, középső és késői luteális fázisokban.
a PGF2a in vivo hatásaival ellentétben az in vitro vizsgálatok mind átmeneti, mind tartós luteolitikus hatást mutattak a humán luteális szövetben.55,56,57 általános egyetértés van abban, hogy a pgf2a által kiváltott luteolízis korai eseménye a patkány corpus luteumban végzett vizsgálatokból származó gonadotropin-érzékeny cAMP termelés megszüntetése.58,59 ez a hatályon kívül helyezés valószínűleg az adenil-cikláz intracelluláris Ca2+emelkedéssel történő közvetlen gátlása miatt következik be.60 az idegtudomány területéről származó legújabb bizonyítékok azt mutatják, hogy a prosztaglandinok serkentik az intracelluláris Ca2+ felszabadulását azáltal, hogy fokozzák a foszfoinozit diacil-glicerinné és inozitol-trifoszfáttá történő hidrolízisét.61 a laboratóriumi állatokon végzett eredményekkel összhangban kimutatták, hogy a humán corpus luteum regressziója az LH receptorok elvesztésével is összefügg.62
jól ismert, hogy sok faj újonnan kialakult sárgatestje refrakter a pgf2a63 litikus hatására; úgy tűnik, hogy ez a megfigyelés kiterjed az emberi sárgatestre is.64 Henderson és McNatty65 felvetették, hogy az újonnan kialakult sárgatest PGF2a receptorait valamilyen módon elfedhetik az elfoglalt LH receptorok, és hogy az LH fokozatos disszociációja a receptorától növelheti a sárgatest érzékenységét a PGF2a iránt. Alternatív hipotézist kínáltak más kutatók,65, akik azt sugallják, hogy az emberi corpus luteum érzékenysége a PGF2a-ra függhet a petefészek noradrenalin szintjétől, amelyek a luteális fázisban növekednek. Úgy tűnik, hogy a katekolaminok növekedése lehetővé teszi a PGF2a antigonadotrop hatását az emberi sárgatestre.66
prosztaglandinok a méhben
a myometriumtól eltérően, amely főleg OFJ 2-t termel, a nem terhes endometrium túlnyomórészt PGF2a-t és PGE2-t termel. A prosztaglandinok szintézise nagyobb a mirigyes epitéliumban, mint az endometrium stromájában, valamint a szekréciós fázisban, mint a ciklus proliferatív fázisában.67,68 ismert, hogy mind a pgf2a, mind a PGE2 specifikus receptorokkal való kölcsönhatásuk révén stimulálják a myometrium kontraktilitását, ami az intracelluláris Ca2+növekedéséhez vezet. A prosztaglandin által kiváltott méh hiperkontraktilitásának ilyen mechanizmusa szerepet játszik az elsődleges dysmenorrhoea patogenezisében. Dysmenorrhoeában szenvedő nők endometriumában és menstruációs folyadékában emelkedett PGF2a és PGE2 szinteket azonosítottak, és az antiprostaglandin szerek kimutatták, hogy ezeknél a betegeknél jelentősen csökkentik a fájdalmat.
különböző prosztaglandinok is termelődnek a méhnyakban, és mind a PGE, mind a PGF receptorhelyei jelen vannak a méhnyakban.69 a prosztaglandinok fokozott termelése vagy helyi beadása terhes nőknél a méhnyak érésével jár.69
prosztaglandinok és szülés
számos megfigyelés közvetetten utal a prosztaglandinok részvételére a szülésben. Ismeretes például, hogy az indometacin vagy más nem szteroid gyulladáscsökkentő gyógyszerek, például az aszpirin beadása meghosszabbítja a terhességet.69 ezenkívül a prosztaglandinokról, különösen a PGF2a-ról ismert, hogy a méh kontraktilitásának erős stimulátorai, és a gravid méh ciklikus összehúzódásait indukálják. Az emelkedett prosztaglandin-koncentrációk az emberek spontán vajúdásának kezdetével járnak. Ezenkívül a összehúzódások kezdetét megelőző időszakot a plazma PGF2a szintek jellemzik, amelyek egyenértékűek a nem terhes nők szintjével. A PGF2a elleni immunizálás szintén késlelteti a szülés kezdetét.70 prosztaglandint használnak a korai vajúdás és az abortusz kiváltására; valójában a prosztaglandin a választott gyógyszer a midtrimeszteri abortuszok elvégzéséhez.69,71
juhokon végzett kiterjedt vizsgálatok alapján úgy tűnik, hogy a méhben lokálisan szintetizált prosztaglandinok a méhösszehúzódások elősegítése érdekében közvetlenül a myometriumra hatnak. A helyi, placenta progeszteron csökkenése az ösztrogén növekedésével kombinálva Ca2 + felszabadulását eredményezi a törékennyé vált lizoszómákból. Ez a Ca2 + felszabadulás stimulálja a prosztaglandin szintézist a foszfolipáz aktivitás növelésével. Úgy tűnik, hogy az oxitocin elősegíti, nem pedig elindítja az ösztrogén és a progeszteron hatásait.72 a magzati membránok, a decidua vera és a myometrium mind részt vehetnek a prosztaglandinok képződésében.73,74
egy friss javaslat szerint az intrauterin szövetek prosztaglandintermelése tonikusan gátolt az emberi terhesség alatt, és hogy az ilyen gátlás fokozatosan megszűnik a kifejezés közeledtével. Bár a prosztaglandin szintézis tónusos gátlását befolyásoló mechanizmusokat nem sikerült megállapítani, számos antifoszfolipáz peptidet találtak a humán placentában, az amnionban,a 75-ben és a chorionban.76 egy másik lehetőség, hogy a prosztaglandin szintézist a szintézis gátlás eltávolításával párhuzamosan stimulálják. A prosztaglandinok fokozott szintézisének lehetséges jelei számos növekedési faktor és thrombocyta-aktiváló faktor. A magzati tüdő-és veseszövetek vérlemezke-aktiváló faktort választanak ki, amely képes stimulálni a prosztaglandin termelést az emberi amnion által.77
prosztaglandinok és a Ductus Arteriosus
a ductus arteriosus átjárhatóságának fenntartása (az értágulat relaxációja) kulcsfontosságú a magzat szöveteinek oxigénellátásának szabályozásában. Születés után a ductus arteriosus általában összehúzódik vagy elveszíti átjárhatóságát. A záródás mechanizmusa nem tisztázott, bár a vér oxigénfeszültségét fontos tényezőnek tartják (ábra. 7). A ductus arteriosus elsődleges funkciója a magzatban a bal-jobb artériás vér tolatásának bizonyos fokú fenntartása, ezáltal szabályozva a tüdőbe történő vénás visszatérés mennyiségét. A ductus záródása fontos fiziológiai folyamat, amely hiányos állapotban légzési distresszhez és cianózishoz/hypoxia—szindrómákhoz vezet, amelyek felelősek a magas morbiditásért és mortalitásért sok koraszülöttnél, akik szabadalmi ductus arteriosusban szenvednek. Emiatt nagy az érdeklődés a ductus arteriosus funkció szabályozásának mechanizmusa(I) iránt. Ez az érdeklődés különösen akut a prosztaglandin kutatás területén, amelyben ma már jelentős mennyiségű bizonyíték utal arra, hogy a prosztaglandinok részt vesznek a ductus arteriosus átjárhatóságának szabályozásában.
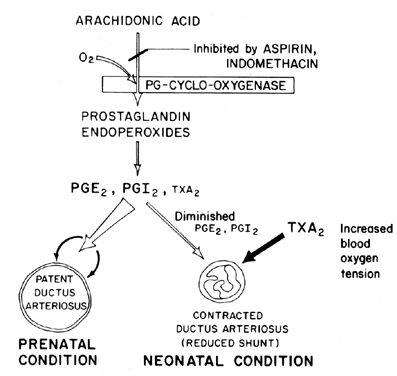 Fig. 7. A ductus arteriosus átjárhatóságának prosztaglandin modulációja a magzatban és az újszülöttben az oxigénfeszültség függvényében.
Fig. 7. A ductus arteriosus átjárhatóságának prosztaglandin modulációja a magzatban és az újszülöttben az oxigénfeszültség függvényében.
ez a bizonyíték a következő megfigyelési sorozaton alapul:
a ductus arteriosus a magzatban cardiopulmonalis állapotromlás és hialinmembrán betegség esetén prosztaglandin-szintetáz inhibitorok alkalmazásával lezárható.78
az indometacin indukálhatja a hipoxiás ér összehúzódását, amint azt az állatokra gyakorolt hatása rövid távon bizonyítja.79
a PGE2 (és PGE1) alkalmazása az izolált magzati bárány ductus arteriosus készítmények (kör alakú csíkok) relaxációját (átjárhatóságának elvesztését) idézi elő alacsony oxigéntartalmú környezetben (PO2 kevesebb, mint 14 Hgmm).80
valószínűnek tűnik, hogy az E sorozatú prosztaglandinok, valamint a prosztaglandin antagonisták és a prosztaglandin-szintetáz blokkolók (aszpirin) kívánatos nem sebészeti kezelésnek bizonyulhatnak koraszülöttek számára, akiknél potenciálisan halálos a ductus arteriosus. A legújabb bizonyítékok arra utalnak, hogy egyensúly van a ductus átjárhatósága és a szűkület között, amelyet a dilatáló prosztaglandinok (OFJ2 és PGE2) és a szűkítő prosztaglandin (TXA2) szintézise tart fenn. A bárány magzatában mind a ductus arteriosus, mind a tüdő szintetizálja a PGI2-t és a PGE2-t; ezután a kifejezés közeledtével a tüdő a TXA2 szintézis felé tolódik el.81 további információk állnak rendelkezésre a prosztaglandin ductus arteriosus funkció szabályozásában való részvételéről.82