prostaglandinas exibem uma ampla gama de efeitos biológicos, e suas ações estão entre as mais variadas de quaisquer compostos naturais. Apesar desta observação, Este grupo de lípidos apresenta uma marcada especificidade estrutura-actividade, que é determinada principalmente pelas substituições do anel ciclopentanona e pelo grau de não-maturação das cadeias laterais do ácido prostanóico. A resposta celular às prostaglandinas é mediada pela sua interacção com os receptores da membrana plasmática.Os receptores PG foram inicialmente classificados com base em atividades funcionais de agonistas naturais e sintéticos, e os antagonistas foram classificados nas seguintes categorias: DP, EP, FP, IP e TP. A primeira letra denota o tipo prostaglandina, E A letra P significa “prostanóide”.”30 Later, studies by binding analysis and molecular cloning confirmed the presence of distinct receptor types as well as three or four subtypes of EP (EP1–4). Os receptores de prostaglandinas da membrana plasmática pertencem à superfamília de receptores acoplados a proteínas G caracterizados por sete regiões transmembranares.Os segundos mensageiros intracelulares dos receptores das prostaglandinas incluem cAMP, proteína cinase C e cálcio.30,31 os vários receptores mostram notável especificidade para o eicosanóide, com pelo menos uma preferência de 100 vezes para o ligando. Em altas concentrações, PGE2 e PGF2a interagem com o receptor DP; similarmente, PGF2a irá ativar o receptor EP, enquanto PGD2 e PGE2 irão interagir com o receptor FP em altas concentrações. A maioria dos tecidos contém uma mistura de receptores, que parece ser a base para os efeitos frequentemente opostos de uma prostaglandina em doses diferentes.
papel das prostaglandinas na secreção de gonadotropina
foram publicados dados recentes que implicam um papel fisiológico das prostaglandinas na regulação da secreção de hormona libertadora de gonadotropina (GnRH).32,33 vários relatórios sugerem que as prostaglandinas, particularmente a PGE2, exercem influências estimulatórias na libertação de gonadotropina, um efeito que parece ser mediado por uma ação ao nível do hipotálamo. O PGE2 demonstrou estimular a libertação de GnRH do hipotálamo, e o pré-tratamento de animais com anti-soros para neutralizar a GnRH endogénea impede a libertação de LH induzida pelo PGE2.Além disso, a PGE1 e a PGE2 parecem ser os estimuladores mais potentes da libertação de hormona do crescimento das células adenohipofiseais cultivadas.35 PGB, PGA1, PGA2, PGB2, PGF1 e PGF2 também são estimuladores ativos, mas seus efeitos não são observados em doses fisiológicas. Em geral, as prostaglandinas parecem não estimular a secreção de gonadotropina por uma acção directa na hipófise.A evidência adicional que sugere que as prostaglandinas podem afectar a secreção de gonadotropina (actuando directamente no hipotálamo) é fornecida a partir de estudos que utilizam inibidores da prostaglandina sintetase, tais como a indometacina, que aparentemente reduzem a secreção de gonadotropina.36 Que as prostaglandinas atuam por meio de hipotalâmico liberador de fatores é evidente sobre a base de duas observações:
- pré-Tratamento de feminino e masculino de ratos com antiserum para LH-hormônio liberador (LHRH) prejudicada a capacidade de PGE2 (100 mg por rato) para aumentar a secreção de LH.36
- A administração directa de PGE2 no ventrículo do cérebro do rato imitou o efeito intravenoso das prostaglandinas na estimulação da secreção de gonadotropina.36
conclusões adicionais fornecem um apoio convincente para o conceito de que o PGE2 actua ao nível da mediana eminência para provocar a libertação de LHRH. Esta afirmação é ainda corroborada pela constatação de que o tecido de eminência mediana contém maiores quantidades de prostaglandinas endógenas do que as regiões hipotalâmicas basais. Os dados obtidos de incubações in vitro de fragmentos de eminência mediana obtidos de ratos machos demonstraram que a norepinefrina e a dopamina estimulam a libertação simultânea de LHRH e PGF2a. Este efeito é bloqueado pela indometacina, sugerindo que as prostaglandinas produzidas intraneuronalmente são os mediadores da libertação de LHRH estimulada pela catecolamina. Estes resultados interessantes são discutidos em maior detalhe em uma revisão por Ojeda e co-trabalhadores.36
ovulação e prostaglandinas
após a descoberta de que a indometacina e a aspirina (inibidores da síntese das prostaglandinas) poderiam bloquear a ovulação,33,37 foi sugerido que as prostaglandinas estavam envolvidas no processo de ruptura folicular do ovário. Esta afirmação foi reforçada ainda mais pela constatação de que a injeção intraovariana de antissoro PGF2a também inibiu a ovulação.Existe agora uma quantidade substancial de evidências indicando que a formação de prostaglandina folicular é aumentada durante a ovulação e que esta elevação depende das gonadotropinas.39
o pico médio do ciclo das gonadotropinas estimula a biossíntese folicular dos eicosanóides por um processo mediado pelo campo que é dependente da activação do gene, mas independente da esteroidogénese. A LH parece ser a gonadotropina pituitária fisiológica dominante responsável pela indução da ovulação, e parece provável que os efeitos da LH na ruptura folicular possam ser mediados por leucócitos que secretam enzimas proteolíticas, radicais de oxigénio e prostaglandinas. A indometacina, por exemplo, bloqueará a ovulação normalmente induzida por grandes doses de gonadotropina coriónica humana in vivo. As prostaglandinas podem mediar os efeitos estimuladores da LH nas enzimas ovulatórias, tais como a protease ou a colagenase.Há também a possibilidade de que as prostaglandinas possam provocar uma resposta contractil na parede folicular 41,que agora é conhecida por conter elementos contracteis, como a miosina e a actina. O activador do plasminogénio ou outra protease parece estar intrinsecamente envolvido na ruptura folicular 42 e é evidente que a secreção desta proteína está associada ao aumento induzido pela LH na biossíntese da prostaglandina folicular,embora tenha sido salientado que estes dois eventos podem não ser interdependentes. Na Figura 6 é mostrado um possível mecanismo de acção da prostaglandina na ruptura folicular.
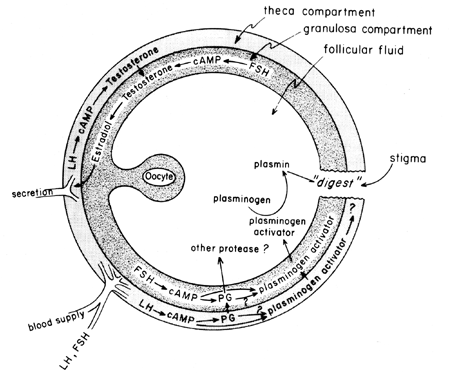 Fig. 6. Possível mecanismo de acção da prostaglandina na ruptura folicular.(Behrman HR: prostaglandinas nas funções hipotalamo-pituitária e ovárica. Ann Rev Physiol 41:685, 1979)
Fig. 6. Possível mecanismo de acção da prostaglandina na ruptura folicular.(Behrman HR: prostaglandinas nas funções hipotalamo-pituitária e ovárica. Ann Rev Physiol 41:685, 1979)
papel das prostaglandinas na função lútea: Luteólise e menstruação
o mecanismo pelo qual o corpo lúteo humano regride 10 a 12 dias após a sua formação é um mistério. Desde a descoberta inicial de que o PGF2a era luteolítico no rato e em muitas outras espécies subprimatárias 43,um grande esforço de pesquisa foi feito para investigar a possibilidade de regulação menstrual com o PGF2a.A PGF2a induz uma regressão funcional do corpo lúteo por um processo mediado pelo receptor, independente inicialmente de alterações no fluxo ovárico ou no sangue lúteo.Em minutos, PGF2a esgota o ácido ascórbico, 44 liberta o receptor LH ocupado do adenilato ciclase, e diminui o transporte de gonadotropina de capilares para a célula luteal.
uma revisão da literatura pertinente revela muitos relatórios contraditórios sobre os efeitos do PGF2a nos seres humanos. Alguns estudos registaram diminuições transitórias nos níveis circulantes de progesterona por PGF2a 45,embora outros estudos não tenham demonstrado tal efeito nas mulheres que ovulam normalmente.46, 47 tendo em conta a existência de receptores pgf2a putativos no corpo lúteo humano 48,argumentou-se que a falha em atingir a luteólise com perfusões intravenosas de PGF2a foi talvez devido ao rápido metabolismo pulmonar. Estudos subsequentes envolvendo a injecção directa de PGF2a no corpo lúteo humano induziram a retirada da progesterona, cujo valor mais baixo coincidiu com o início da menstruação precoce.Estes resultados sugerem que podem ser necessárias prostaglandinas ováricas endógenas (ou algum outro agente luteolítico) para a regressão lútea. Isto parece viável tendo em conta a observação de que a função lútea humana parece ser independente do controlo uterino, uma vez que nem a histerectomia 50 nem a ausência congénita do útero, vagina ou trompas de Falópio afectam a ciclicidade ovárica.O tecido lúteo humano é certamente capaz de produzir prostaglandinas, tal como demonstrado por experiências in vitro 52; no entanto, as tentativas de correlacionar o aumento dos níveis de PGF2a no ovário com regressão lútea na fase lútea tardia não foram bem sucedidas.Parece que a única altura em que a produção ovárica de PGF2a é aumentada no ciclo menstrual humano é pouco tempo após a ovulação.No entanto, também é evidente que as concentrações de PGF2a são sempre mais elevadas no tecido do estroma ovárico através das fases lúteo inicial, média e tardia.Em contraste com os efeitos in vivo da PGF2a, estudos in vitro demonstraram efeitos luteolíticos transitórios e sustentados no tecido luteal humano.55,56,57 é o consenso geral de que um evento precoce na luteólise induzida pela PGF2a é a revogação da produção de campos sensíveis à gonadotropina derivada de estudos no corpo lúteo do rato.58,59 é provável que esta revogação se deva a uma inibição directa da adenilciclase através de aumentos na Ca2+intracelular.60 evidências recentes do campo da neurociência indicam que as prostaglandinas estimulam a libertação de Ca2+ intracelular aumentando a hidrólise do fosfoinositol para diacilglicerol e trifosfato de inositol.Consistente com os achados em animais de laboratório, foi demonstrado que a regressão do corpo lúteo humano também está associada a uma perda de receptores LH.62
é bem conhecido que o corpo lúteo recém-formado de muitas espécies é refractário à acção lítica de PGF2a63; esta observação também parece estender-se ao corpo lúteo humano.Henderson e McNatty65 sugeriram que os receptores PGF2a no corpo lúteo recém-formado podem de alguma forma ser mascarados por receptores LH ocupados, e que a dissociação gradual de LH a partir de seu receptor pode aumentar a susceptibilidade do corpo lúteo a PGF2a. Foi oferecida uma hipótese alternativa por outros investigadores,65 que sugerem que a susceptibilidade do corpo lúteo humano à PGF2a pode depender dos níveis de noradrenalina ovárica, que aumentam durante a fase lútea. Este aumento das catecolaminas parece permitir o efeito antigonadotrópico do PGF2a no corpo lúteo humano.66
prostaglandinas no útero
ao contrário do miométrio, que produz principalmente PGI2, o endométrio não-pregante produz predominantemente PGF2a e PGE2. A síntese das prostaglandinas é maior no epitélio glandular do que no estroma do endométrio, e durante a fase secretória do que durante a fase proliferativa do ciclo.Sabe-se que 67,68 tanto PGF2a como PGE2, através da sua interacção com receptores específicos, estimulam a contractilidade miometrial, levando a um aumento na Ca2+intracelular. Tal mecanismo de hipercontractilidade uterina induzida pela prostaglandina tem sido implicado na patogénese da dismenorreia primária. Foram identificados níveis elevados de PGF2a e PGE2 no endométrio e líquido menstrual de mulheres com dismenorreia, e os agentes antiprostaglandinas demonstraram resultar numa redução acentuada da dor nestes doentes.
várias prostaglandinas também são produzidas no colo uterino, e os locais receptores para PGE e PGF estão presentes no colo uterino.O aumento da produção de prostaglandinas, ou da sua administração local, está associado à maturação cervical em mulheres grávidas.69
prostaglandinas e parto
algumas observações implicam indirectamente o envolvimento das prostaglandinas no parto. Sabe-se, por exemplo, que a administração de indometacina ou outros anti-inflamatórios não esteróides, como a aspirina, prolonga a gestação.Além disso, as prostaglandinas, particularmente PGF2a, são conhecidas por serem estimuladores potentes da contractilidade uterina e induzem contrações cíclicas do útero gravídeo. Concentrações elevadas de prostaglandinas estão associadas ao início do trabalho espontâneo em seres humanos. Além disso, o período de tempo que precede o início das contracções é caracterizado por níveis plasmáticos de PGF2a que são equivalentes aos das mulheres não grávidas. A imunização contra o PGF2a também atrasa o início do parto.70 prostaglandinas são agora usadas para induzir o parto precoce e o aborto; na verdade, a prostaglandina é a droga de escolha para realizar abortos no meio do parto.69,71
com base em estudos extensos em ovinos, parece que as prostaglandinas sintetizadas localmente no útero iniciam o trabalho de parto, actuando directamente no miométrio para promover as contracções uterinas. Uma diminuição na progesterona placentária local, combinada com um aumento no estrogénio, resulta na libertação de Ca2+ de lisossomas que se tornaram frágeis. Esta libertação de Ca2+ estimula a síntese das prostaglandinas, aumentando a actividade da fosfolipase. A oxitocina parece facilitar, ao invés de iniciar, os efeitos de estrogênio e progesterona.72 membranas fetais, decidua vera e myometrium podem participar na formação de prostaglandinas.73, 74
uma proposta recente é a de que a produção de prostaglandinas pelo tecido intra-uterino é inibida tónico durante a gravidez humana, e que essa inibição é progressivamente removida à medida que se aproxima o termo. Embora não tenham sido estabelecidos os mecanismos que produzem a inibição tônica da síntese das prostaglandinas, foram encontrados vários péptidos antifosfolipase na placenta humana, amnião,75 e corião.Outra possibilidade é que a síntese das prostaglandinas seja estimulada em paralelo com a remoção da inibição da síntese. Os sinais potenciais para uma maior síntese das prostaglandinas são vários factores de crescimento e um factor de activação das plaquetas. Os tecidos pulmonares e renais fetais segregam o factor de activação das plaquetas, que é capaz de estimular a produção de prostaglandinas por amnião humano.77
prostaglandinas e o canal arterial
a manutenção da patência (relaxamento da vasodilatação) do canal arterial é fundamental no controlo da oxigenação dos tecidos no feto. Após o nascimento, o ductus arteriosus normalmente torna-se constrito ou perde a sua patência. O mecanismo pelo qual este fechamento ocorre não é claro, embora se acredite que a tensão do oxigênio no sangue seja um fator importante (Fig. 7). A principal função do canal arterial no feto é manter algum grau de manobras do sangue arterial esquerda-a-direita, controlando assim a quantidade de retorno venoso aos pulmões. O encerramento do canal no termo é um processo fisiológico importante que, se incompleto, leva à dificuldade respiratória e a cianose/hipoxia—síndromes que são responsáveis pela elevada morbidade e mortalidade em muitas crianças prematuras que sofrem de canal arterial patente. Por esta razão, existe um grande interesse no(s) mecanismo (s) de controlo da função ductus arteriosus. Este interesse é particularmente agudo no domínio da investigação sobre as prostaglandinas, em que existem actualmente provas consideráveis que sugerem o envolvimento das prostaglandinas no controlo da patência do canal arterial a prazo.
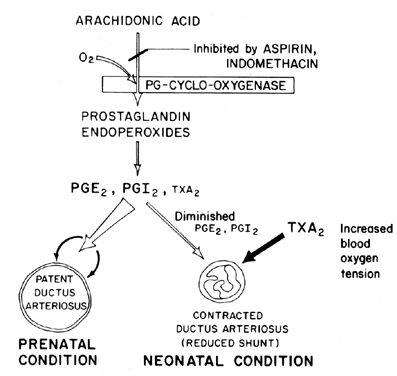 Fig. 7. Esquema de modulação de prostaglandina da patência do canal arterial no feto e do recém-nascido em função da tensão do oxigénio.
Fig. 7. Esquema de modulação de prostaglandina da patência do canal arterial no feto e do recém-nascido em função da tensão do oxigénio.
esta prova baseia-se na seguinte série de observações::
o canal arterial no feto com deterioração cardiopulmonar e doença da membrana hialina podem ser fechados através da administração de inibidores da prostaglandina sintetase.78
a indometacina pode induzir a contracção do vaso hipóxico, como demonstrado pelos seus efeitos em animais a curto prazo.79
a administração de PGE2 (e PGE1) induz um relaxamento (perda de patência) das preparações de canal arterial de borrego fetal isoladas (faixas circulares) num ambiente de baixo oxigénio (PO2 inferior a 14 mmHg).80
parece provável que as prostaglandinas da série E, juntamente com antagonistas da prostaglandina e bloqueadores da prostaglandina-sintetase (aspirina), possam ser tratamentos não cirúrgicos desejáveis para lactentes pré-termo com canal arterial potencialmente fatal. Evidências recentes sugerem um equilíbrio entre a patência do canal e a constrição que é mantida pela síntese de prostaglandinas dilatantes (PGI2 e PGE2) e constrição da prostaglandina (TXA2). No feto de cordeiro, tanto o canal arterial como o pulmão sintetizam PGI2 e PGE2.; então, à medida que o termo se aproxima, o pulmão muda para a síntese TXA2.Está disponível Informação adicional sobre o envolvimento da prostaglandina no controlo da função ductus arteriosus.82