Introducción
El cloro es uno de los desinfectantes más utilizados para la desinfección del agua. El cloro se puede aplicar para la desactivación de la mayoría de los microorganismos y es relativamente barato. El cloro está disponible comercialmente como cloro gaseoso (CL2) y como hipoclorito de sodio líquido o en polvo (NaOCl).
Tanto el cloro gaseoso (CL2) como el hipoclorito de sodio (NaOCl) tienen propiedades desinfectantes muy limitadas. Es la formación de subproductos de cloro como el Ácido Hipocloroso (HOCL), el ion hipoclorito (OCL -), el Ácido Clorhídrico (HCL) y el Oxígeno (O) que inhiben las propiedades desinfectantes.
Cloro gaseoso
El cloro gaseoso (CL2)está disponible comercialmente y se utiliza principalmente para desinfectar el agua de la red.
Cuando se añade cloro gaseoso (CL2) al agua (H2O) se produce la siguiente reacción de hidrólisis:
Cl2 + H2O = H+ + Cl- + HOCl
Hipoclorito de sodio
Se produce hipoclorito de sodio añadiendo Cloro gaseoso (CL2) a la sosa cáustica (NaOH). Cuando esto se hace, el hipoclorito de sodio (NaOCl), el agua (H2O) y la sal (NaCl) se producen de acuerdo con la siguiente reacción:
Cl2 + 2NaOH + → NaOCl + NaCl + H2O
El cloro reacciona con hidróxido de sodio a Hipoclorito de sodio (NaOCl). El hipoclorito de sodio se conoce como lejía. El blanqueador (NaOCl) no se puede combinar con ácidos. Cuando el NaOCl entra en contacto con los ácidos, el hipoclorito se vuelve inestable, lo que hace que se escape el cloro gaseoso venenoso (CL2).
Hypochlorous Acid and Hypochlorite Ion formation
Hypochlorous Acid (HOCL) and Hypochlorite Ion (OCL-) are the by-products of Sodium Hypochlorite (NaOCL) in water (H2O). NaOCL reacts with water (H2O) to Hypochlorous Acid (HOCl) and Hypochlorite Ions (OCl-).
NaOCl + H2O → HOCl + NaOH-
Hypochlorous Acid formation
Hypochlorous Acid (HOCL) is the by-product of gaseous Chlorine (CL2) in Water. Gaseous Chlorine (CL2) reacts with water to Hypochlorous Acid (HOCL).
Cl2 + H2O – > HOCl + H + + Cl –
Formación de oxígeno
Dependiendo del valor de pH, el Ácido hipocloroso (HOCL) expira a Iones de hipoclorito (OCL-).
Cl2 + 2H2O -> HOCl + H3O + Cl – HOCl + H2O -> H3O+ + OCl-
Esto se descompone en átomos de cloro y oxígeno:
OCl- -> Cl- + O
La eficacia de la desinfección está determinada por el pH.
La desinfección se llevará a cabo de manera óptima cuando el pH esté entre 5 y 7, ya que entonces se encuentra un máximo de HOCL.
HOCL reacciona más rápido que OCl- ; HOCL es 80-100% más efectivo que OCL -. HOCL no se evapora y no causa corrosión severa como el CL2. El CL2 expuesto al aire puede ser muy explosivo y debe evitarse la evaporación. Por esta razón, el pH ideal está entre 6 y 7, ya que no hay CL2 presente.
El nivel de HOCL disminuirá cuando el valor de pH sea superior a 5. El nivel de HOCL disminuirá cuando el valor de pH sea inferior a 5. Con un valor de pH de 6,5, el nivel de HOCL es superior al 90%, mientras que la concentración de OCL es inferior al 10%.
Cloro libre disponible
El cloro libre disponible (FAC) es cloro que está presente en forma de Ácido hipocloroso, iones de hipoclorito o como cloro elemental disuelto. FAC incluye todas las especies de cloro que no se combinan con amoníaco (u otros compuestos nitrogenados) para formar cloraminas. Es ‘ libre ‘en el sentido de que aún no ha reaccionado con nada, y’ disponible ‘ en el sentido de que puede reaccionar y reaccionará si es necesario.
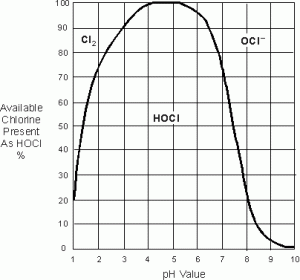
Un valor de pH de 6 a 7 es el rango de pH más efectivo y seguro, debido a la ausencia de gas de cloro. Por lo tanto, cuando se menciona el Cloro Libre Disponible, se asume que el Cloro Libre Disponible consiste únicamente en HOCL y OCL-
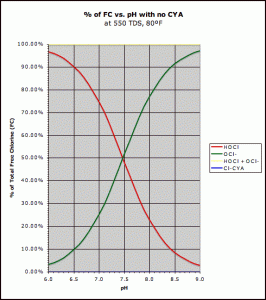
Compuestos de cloro libres disponibles en relación con el pH .El Ácido Hipocloroso (rojo) y el Ion Hipoclorito (verde)
La superioridad del Ácido Hipocloroso en comparación con el Ion Hipoclorito
El Ácido Hipocloroso (HOCl, que es eléctricamente neutro) y los Iones Hipoclorito (OCl, eléctricamente negativos) formarán Cloro Libre Disponible (FAC) cuando se unen entre sí. Esto da como resultado la desinfección. Ambas sustancias tienen un comportamiento muy distintivo.
La pared celular de los microorganismos patógenos está cargada negativamente por la naturaleza. Como tal, la pared celular solo penetra por el Ácido Hipocloroso neutro (HOCL), no por el ion hipoclorito cargado negativamente (OCL-).
HOCL puede penetrar capas de limo, paredes celulares y capas protectoras de microorganismos y, como resultado, mata eficazmente a los patógenos. Los microorganismos morirán o sufrirán de fallas reproductivas.
El Ácido Hipocloroso de pH neutro (HOCL) puede penetrar en las paredes celulares de microorganismos patógenos, mientras que el ion hipoclorito cargado negativamente (OCL-) no puede penetrar en las paredes celulares.
Además de la neutralidad de HOCL, es un desinfectante mucho más reactivo y mucho más fuerte que OCL-, ya que HOCL se divide en ácido clorhídrico (HCl) y oxígeno de aire atómico (O). El oxígeno es un desinfectante muy potente.
El agua electrolizada neutra (HOCL) garantiza una desinfección óptima
Las propiedades desinfectantes del cloro en el agua se basan en la formación y el poder oxidante del oxígeno y el HOCL. Estas condiciones ocurren cuando el pH está entre 6 y 7.
El agua Electrolizada Neutra (NUEVA) producida in situ a partir de un sistema AQUAOX tiene un pH de 6,5. A este pH, más del 90% del cloro libre disponible es HOCL, menos del 10% de OCL y no se forma CL2. La resistencia del cloro libre Disponible (FAC) en NEW está preestablecida en 300+ppm. Para hacer una solución con más de 300 ppm de FAC a partir de lejía disponible comercialmente (NaOCl), se diluye en agua (H2O).
El problema de diluir lejía en agua es doble:
1) El volumen para diluir lejía es muy pequeño. Pequeñas diferencias en el volumen de lejía añadida al agua causan diferencias significativas en términos de pH y Cloro Libre Disponible (FAC).
2) El hecho de que el agua tenga niveles de pH naturalmente diferentes, hace que la adición del mismo volumen de lejía aún resulte en un pH diferente. Aunque en cada dilución se pueden medir más de 300 ppm de FAC, el pH de la mezcla y, en consecuencia, la cantidad de compuestos activos HOCL y OCL – pueden variar considerablemente.
Por lo tanto, las propiedades desinfectantes con lejía varían, mientras que las propiedades desinfectantes de las NUEVAS se mantienen estables. Como resultado, NEW puede superar las propiedades desinfectantes de la lejía en 300 veces.
Seguridad
Al producir HOCL acidificando NaOCl, los precios relativamente altos y la posibilidad de reacciones secundarias limitan el uso de ácidos orgánicos débiles; el uso de ácidos inorgánicos más baratos provoca la descarga de cloro gaseoso y un aumento del nivel de toxicidad. Debido a ello, el método anterior solo se utiliza para el tratamiento del agua, donde los valores de concentración de cloro residual no exceden 0.5-5mg/l.
La dilución de cloro gaseoso en agua para producir HOCL de acuerdo con la ecuación exige medidas de seguridad especiales y solo se usa para desinfectar grandes volúmenes de agua, donde la concentración de cloro activo está por debajo de 10-15mg/l. Hoy en día, todas las empresas que fabrican cloro gaseoso detuvieron la producción de cloro gaseoso y comenzaron la fabricación de NaOCl exclusivamente por consideraciones de seguridad.
El agua electrolizada neutra in situ producida por AQUAOX Systems es un método único de síntesis de HOCL sin reactivos. Nos gustaría señalar una vez más que la calidad única del sistema AQUAOX es la posibilidad de regulación de pH dirigida en el 6.0-7.rangos 0, mientras se trabaja con soluciones de cualquier mineralización, mientras que los electrolitos de soluciones de cloruro de sodio tienen una actividad biocida idéntica si la concentración de pH y FAC son iguales.
Para obtener más información, póngase en contacto con [email protected]